1. 领域背景与文献引入
文献英文标题:Improved hematopoietic differentiation of human pluripotent stem cells via estrogen receptor signaling pathway;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:人类多能干细胞造血分化调控、雌激素受体信号通路
人类造血干细胞(HSC)的增殖与分化受内在因子与微环境信号的共同调控,领域发展关键节点包括人类多能干细胞(hPSC)体外造血分化模型的建立,以及Notch、Wnt、Hedgehog等经典信号通路在造血分化中调控作用的阐明,为体外造血调控提供了核心理论基础。当前研究热点聚焦于挖掘新的造血分化调控因子,尤其是内分泌系统与造血系统的交互作用,而未解决的核心问题在于,雌激素(E2)在人类造血系统中的调控作用尚未明确——尽管啮齿类动物研究已证实雌激素可调控造血干细胞的增殖与分化,但缺乏合适的人类实验模型,无法验证该调控机制在人类造血分化中的保守性与特异性。基于此,本研究以人类多能干细胞为体外模型,旨在明确雌激素对人类造血分化的调控作用及分子机制,填补人类造血内分泌调控领域的研究空白。
2. 文献综述解析
作者以“物种差异-模型局限-研究空白”为核心评述逻辑,系统梳理了雌激素调控造血的研究进展,重点对比啮齿类动物与人类研究的差异,明确本研究的必要性。
现有研究中,啮齿类动物研究已证实,雌激素可通过调控造血生长因子(如SCF、IL-3)水平影响骨髓造血功能,在小鼠中,雌激素可促进短期造血干细胞(ST-HSC)进入S期以增强增殖能力,且ER-α缺陷会导致长期(LT)和短期(ST)造血干细胞数量减少,ER-α信号通路还可特异性促进红细胞生成;这些研究的优势在于明确了雌激素在啮齿类造血中的调控作用与受体亚型特异性,局限性在于无法直接外推至人类造血系统,且缺乏对人类早期造血分化阶段(如成血血管细胞形成)的研究数据。
本研究的创新价值在于,首次采用人类多能干细胞体外造血分化模型,验证了雌激素对人类早期造血分化的调控作用,明确了ER-α的特异性介导功能,并进一步在人脐带血造血祖细胞中验证了该调控机制的普遍性,弥补了人类造血内分泌调控研究的模型缺陷与数据空白。
3. 研究思路总结与详细解析
本研究的整体框架为“表达检测-功能验证-机制解析-普遍性验证”闭环,研究目标是明确雌激素对人类多能干细胞造血分化的调控作用及分子机制,核心科学问题是雌激素是否通过雌激素受体亚型特异性调控人类早期造血分化,技术路线为:首先检测ER-α在hPSC造血分化各阶段的表达模式,然后验证雌激素对造血分化的促进作用,再通过受体激动剂/拮抗剂明确ER-α的介导功能,最后在人脐带血造血祖细胞中验证该调控机制的普遍性。
3.1 ER-α在造血分化过程中的表达模式检测
实验目的是明确ER-α在人类多能干细胞造血分化各阶段的表达特征,以及与造血表型的关联;方法细节包括采用免疫细胞化学染色检测无饲养层培养的诱导多能干细胞(hiPSC)中ER-α与OCT4的共表达,通过流式细胞术分析未分化hiPSC及分化各阶段细胞中ER-α与造血标志物(CD34、CD45)的表达分布;结果解读:免疫细胞化学染色显示ER-α在未分化hiPSC中高表达,流式细胞术结果表明ER-α在分化的OCT4阴性细胞中持续存在,且造血表型细胞(CD34+、CD45+)仅在ER-α阳性细胞亚群中被检测到,提示ER-α与造血分化命运密切相关;实验所用关键产品:BD Biosciences的OCT4抗体、Santa Cruz的ER-α抗体、BD Biosciences的CD34-FITC、CD45-APC流式抗体、BD FACSCanto II流式细胞仪。
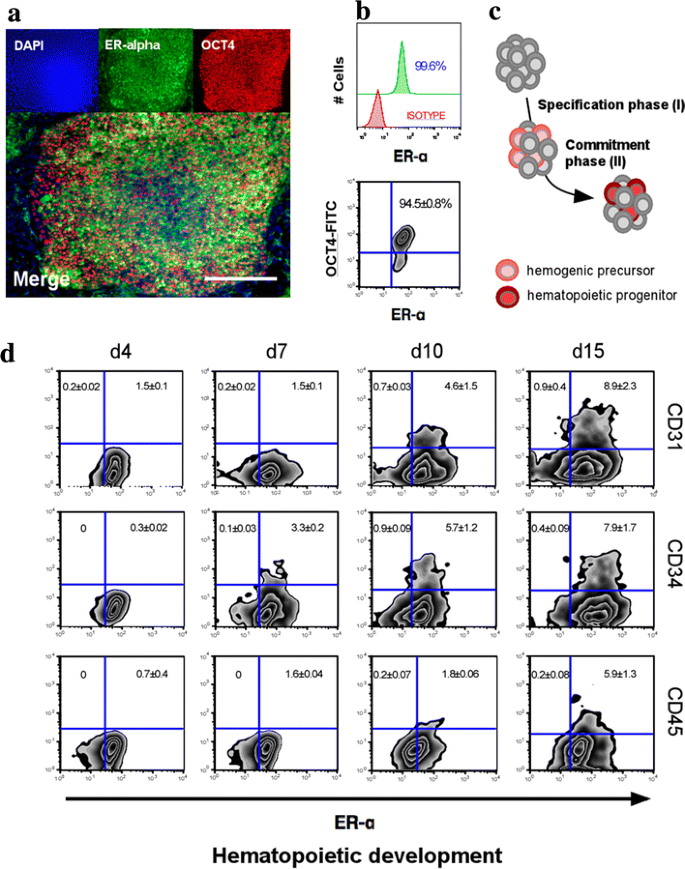
3.2 雌激素对多能干细胞造血分化的功能验证
实验目的是验证雌激素是否可促进人类多能干细胞的造血分化输出,以及是否依赖雌激素受体信号;方法细节包括在造血分化培养基中添加不同浓度(10^-8 M、10^-7 M)的雌激素,结合优化的人类生长因子(hGFs)处理,或单独添加雌激素,同时设置ER拮抗剂ICI 182,780处理组、ER-α siRNA敲低组,分阶段(造血规格阶段:0-7天、造血定型阶段:7-15天)处理以明确雌激素作用的时间窗口;结果解读:10^-8 M雌激素与hGFs协同作用,使造血祖细胞(CD34+CD45+)和成熟血细胞(CD34-CD45+)数量增加约2倍(n=3,P<0.01),单独添加雌激素无显著效果;ER拮抗剂可完全阻断雌激素的造血促进效应,ER-α siRNA敲低显著减少造血分化输出;持续处理两个阶段的造血促进效果优于单阶段处理,提示雌激素需持续激活才能发挥最大调控作用;实验所用关键产品:Sigma的雌激素(E2)、Tocris的ICI 182,780、Dharmacon的ER-α siRNA、STEMCELL Technologies的甲基纤维素培养基。
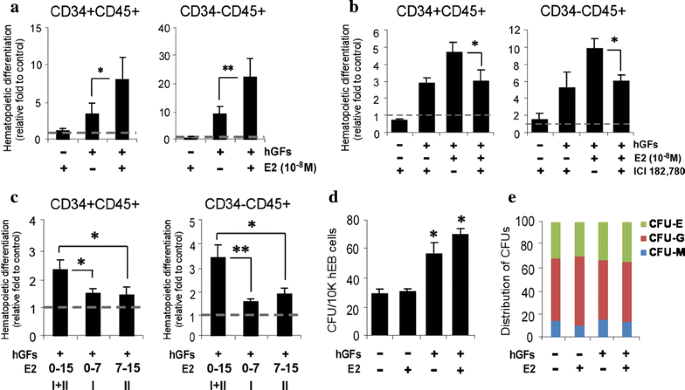
3.3 雌激素受体亚型的特异性功能验证
实验目的是明确介导雌激素造血调控作用的受体亚型(ER-α或ER-β);方法细节包括采用ER-α选择性激动剂PPT(100 nM)和ER-β选择性激动剂DPN(100 nM)分别处理多能干细胞,检测成血血管细胞集落形成及造血祖细胞的CFU形成能力,同时检测红细胞标志物的表达;结果解读:PPT处理可显著增加成血血管细胞集落数量及CFU数量,效果与雌激素处理相当,而DPN处理无显著效果;雌激素处理使红细胞标志物CD235a+CD45-、CD235a+CD71+细胞比例显著升高(n=3,P<0.05),提示ER-α是介导雌激素促进造血分化(尤其是成血血管细胞形成与红细胞生成)的关键亚型;实验所用关键产品:Sigma的PPT和DPN、BD Biosciences的CD235a-PE、CD71-APC抗体。
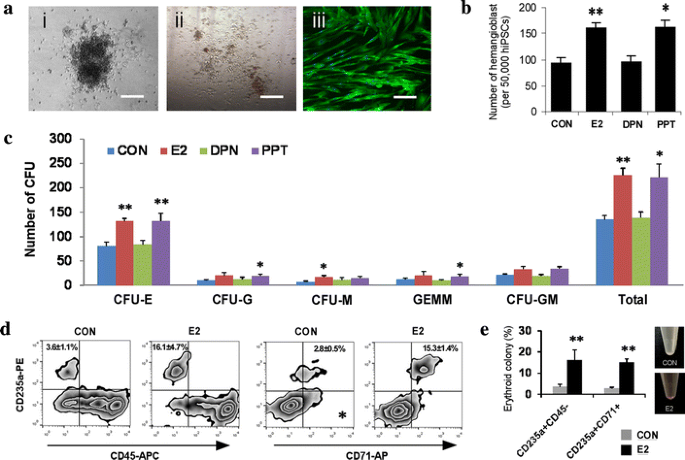
3.4 雌激素调控造血的普遍性验证
实验目的是验证雌激素对人类原发性造血祖细胞的调控作用,明确该机制的普遍性;方法细节包括通过免疫磁珠分离人脐带血(hUCB)中的CD34+造血祖细胞,添加雌激素培养5天和10天,检测细胞增殖情况及CFU形成能力;结果解读:雌激素处理10天后,CD34+造血祖细胞数量增加约2倍(n=3,P<0.01),CFU数量在培养5天和10天均显著升高,且ER-α阳性细胞比例在雌激素处理组维持在较高水平,提示雌激素的造血调控作用在原发性造血祖细胞中同样存在;实验所用关键产品:STEMCELL Technologies的StemSep分离系统、Sigma的Stemline II培养基。
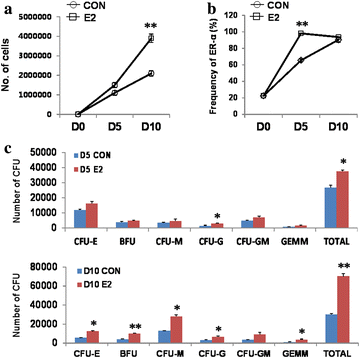
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为雌激素受体α(ER-α),属于核蛋白/细胞表面标志物,其筛选与验证逻辑为“表达关联-功能验证-普遍性验证”的完整链条:首先通过流式细胞术发现造血表型细胞仅存在于ER-α阳性细胞亚群中,随后通过受体激动剂/拮抗剂、siRNA敲低验证其功能必要性,最后在人脐带血造血祖细胞中验证其表达与功能的保守性。
研究过程详述:该Biomarker的来源包括人类多能干细胞分化细胞及人脐带血CD34+造血祖细胞,验证方法涵盖免疫细胞化学染色、流式细胞术、受体特异性激动/拮抗实验、siRNA功能缺失实验;特异性数据显示,造血表型细胞(CD34+、CD45+)仅在ER-α阳性细胞中存在,敏感性数据方面,雌激素处理后ER-α阳性细胞中造血祖细胞比例较对照组升高约1倍(n=3,P<0.01)。
核心成果提炼:ER-α作为功能性Biomarker,其信号通路的激活可显著促进成血血管细胞形成、造血祖细胞扩增及红细胞生成,风险比(HR)相关数据未在原文中提供;该Biomarker的创新性在于,首次在人类造血分化模型中明确ER-α是雌激素调控造血的特异性介导因子,且该调控机制在多能干细胞与原发性造血祖细胞中均保守,为人类造血内分泌调控提供了新的靶点与理论依据。
