1. 领域背景与文献引入
文献英文标题:Preclinical development of HQP1351, a multikinase inhibitor targeting a broad spectrum of mutant KIT kinases, for the treatment of imatinib-resistant gastrointestinal stromal tumors;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:胃肠道间质瘤靶向治疗、新型激酶抑制剂研发
胃肠道间质瘤(GIST)是最常见的胃肠道间叶源性肿瘤,约75%的病例携带KIT或PDGFRα基因的功能获得性突变,KIT酪氨酸激酶的持续激活是肿瘤发生发展的核心驱动因素。2002年,一代KIT抑制剂伊马替尼获批作为GIST一线治疗药物,通过结合KIT激酶的ATP结合口袋抑制激酶活性,显著改善了GIST患者的预后,但临床数据显示,约50%的患者在治疗2-3年后会因继发性KIT突变(主要位于ATP结合口袋外显子13/14、活化环外显子17/18)产生耐药,这是当前GIST治疗领域未解决的核心难题。领域共识:二线抑制剂舒尼替尼和瑞戈非尼通过拓宽靶点覆盖范围,分别针对ATP结合口袋突变和活化环突变,部分克服了伊马替尼耐药,但舒尼替尼对活化环突变无效,瑞戈非尼对ATP结合口袋突变的抑制活性较弱,且二者均存在不同程度的脱靶效应;三代抑制剂普纳替尼作为泛激酶抑制剂,可有效抑制多种KIT突变亚型,临床研究显示其对多线治疗失败的GIST患者有一定疗效,但严重的动脉闭塞事件风险(5年随访中慢性期慢粒患者动脉闭塞事件累积发生率达31%)极大限制了其长期临床应用。针对伊马替尼耐药GIST的更安全、有效的三代抑制剂仍存在研究空白,因此本文探索了原本用于T315I突变慢性髓系白血病的三代BCR-ABL抑制剂HQP1351在该领域的治疗潜力,为耐药GIST患者提供新的治疗选择。
2. 文献综述解析
本文综述部分以GIST靶向治疗药物的代际演进为分类维度,系统梳理了一代至三代KIT抑制剂的作用特点、临床疗效及局限性,明确了当前耐药GIST治疗的核心瓶颈,为HQP1351的研究提供了逻辑基础。
首先,一代抑制剂伊马替尼通过结合KIT激酶的ATP结合口袋,抑制原发性KIT突变(外显子9/11)的激酶活性,显著改善了GIST患者的预后,但继发性KIT突变会改变激酶构象,导致伊马替尼结合力下降,进而产生耐药,这是一代药物无法突破的局限。其次,二代抑制剂舒尼替尼和瑞戈非尼通过拓宽激酶靶点覆盖范围,分别针对ATP结合口袋突变和活化环突变,部分克服了伊马替尼耐药,但舒尼替尼对活化环突变无效,瑞戈非尼对ATP结合口袋突变的抑制活性较弱,且二者均存在不同程度的脱靶效应,长期治疗的毒副作用仍较明显。最后,三代抑制剂普纳替尼作为泛激酶抑制剂,可有效抑制包括T315I在内的多种BCR-ABL突变,同时对绝大多数KIT突变亚型具有抑制活性,临床研究显示其对多线治疗失败的GIST患者有一定疗效,但严重的心血管毒性极大限制了其临床应用。
通过对比现有研究的局限性,本文的创新价值在于首次系统验证了HQP1351对伊马替尼耐药GIST的体内外抗肿瘤活性,且从激酶结合活性、信号通路调控、体内肿瘤抑制效果等多个维度,证实HQP1351的疗效优于普纳替尼,同时基于HQP1351在慢粒临床研究中显示的可控副作用,推测其在GIST治疗中可能具有更优的安全性,填补了三代KIT抑制剂在耐药GIST治疗中“高效低毒”的研究空白。
3. 研究思路总结与详细解析
本文整体研究思路遵循“靶点验证→细胞水平功能实验→机制解析→体内模型验证”的经典抗肿瘤药物研发逻辑,核心研究目标是明确HQP1351对携带继发性KIT突变的伊马替尼耐药GIST的治疗潜力,核心科学问题是HQP1351是否能通过更高效抑制KIT及其下游通路,克服伊马替尼耐药,且疗效优于现有三代抑制剂普纳替尼。研究共分为6个关键实验环节,逐层验证HQP1351的作用效果与机制。
3.1 KIT激酶结合活性检测
实验目的是明确HQP1351对野生型及不同突变亚型KIT激酶的直接抑制能力,为后续细胞及体内实验提供靶点基础;方法细节是采用KINOMEscan™激酶分析系统,检测HQP1351在10nM和100nM浓度下,对野生型KIT、原发性KIT突变(外显子11的L576P、V559D)、继发性KIT突变(ATP结合口袋的V559D/T670I、V559D/V654A,活化环的A829P、D816H、D816V)的结合抑制率,以DMSO为阴性对照,阳性化合物为阳性对照;结果解读:10nM浓度下,HQP1351对野生型KIT、原发性L576P/V559D突变、继发性V559D/T670I双突变的抑制率均超过90%;对V559D/V654A双突变的抑制率在10nM时约为40%,100nM时提升至90%以上;对活化环突变的抑制率在10nM时为20-40%,100nM时提升至50-80%,提示HQP1351对ATP结合口袋突变的抑制活性更强;产品关联:实验所用关键产品:KINOMEscan™激酶分析系统。
3.2 细胞增殖活性检测
实验目的是验证HQP1351对伊马替尼敏感及耐药GIST细胞的抗增殖活性,对比其与现有抑制剂的疗效差异;方法细节是采用基于水溶性四唑盐(WST)的Cell Counting Kit-8(CCK-8)法,将伊马替尼敏感的GIST T1细胞(携带原发性KIT外显子11突变)和伊马替尼耐药的GIST 430细胞(携带继发性KIT外显子11/14双突变)分别用系列浓度的HQP1351、伊马替尼、普纳替尼、舒尼替尼、瑞戈非尼处理72h,每个浓度设置3个复孔,重复实验2次,通过GraphPad Prism软件计算半数抑制浓度(IC50);结果解读:GIST T1细胞中,HQP1351的IC50为0.027±0.021μM,与伊马替尼(0.027±0.005μM)、普纳替尼(0.021±0.000μM)相当;GIST 430细胞中,HQP1351的IC50为0.091±0.021μM,是伊马替尼(1.620±0.318μM)的17.8倍,显著优于舒尼替尼(0.482μM,文献未明确SD)和瑞戈非尼(3.320μM,文献未明确SD),且略优于普纳替尼(0.134±0.057μM,P<0.05,n=3),提示HQP1351可有效克服继发性KIT突变导致的伊马替尼耐药;产品关联:实验所用关键产品:Cell Counting Kit-8(Tianjin Biolite Biotech Co., Ltd.)、GraphPad Prism软件(version 6.0)。
3.3 克隆形成、细胞迁移与侵袭能力检测
实验目的是评估HQP1351对GIST细胞恶性表型的抑制作用,排除单纯增殖抑制的影响;方法细节:克隆形成实验将GIST 430细胞以1000个/孔接种,用0.3μM的HQP1351、伊马替尼、普纳替尼处理14天,结晶紫染色后用AlphaImager HP系统计数克隆数;细胞迁移实验采用划痕法,在近汇合的GIST 430细胞单层制造划痕,用上述浓度药物处理5天,倒置显微镜下评估伤口愈合程度;细胞侵袭实验采用Transwell小室(8μm孔径),上室接种无血清培养基培养的GIST 430细胞,下室加入含10%胎牛血清的培养基,用上述浓度药物处理24h,甲醇固定、结晶紫染色后计数穿膜细胞数,每个实验设置3个复孔;结果解读:
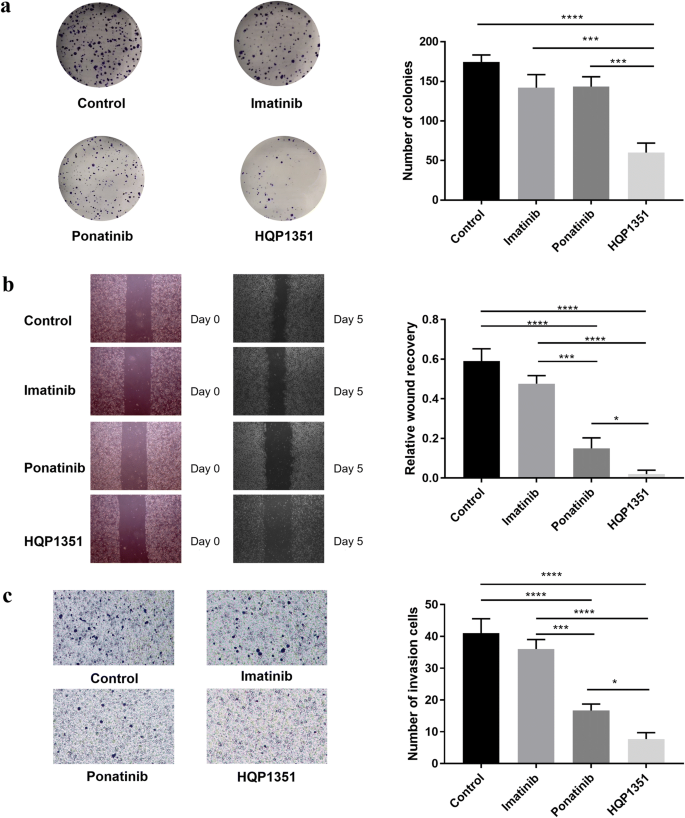
HQP1351处理组的克隆数显著少于伊马替尼组和普纳替尼组(P<0.0001,n=3);划痕实验显示HQP1351组的伤口愈合程度显著低于对照组和普纳替尼组(P<0.05,n=3);Transwell实验显示HQP1351组的穿膜细胞数显著少于伊马替尼组和普纳替尼组(P<0.05,n=3),提示HQP1351可有效抑制GIST细胞的克隆形成、迁移及侵袭能力,且效果优于现有抑制剂;产品关联:实验所用关键产品:Transwell小室(Corning, NY, USA)、AlphaImager HP系统(Proteinsimple, CA, USA)、Leica倒置显微镜。
3.4 细胞周期与凋亡检测
实验目的是解析HQP1351抑制GIST细胞增殖的具体机制,明确其是否通过诱导细胞周期停滞和凋亡发挥作用;方法细节:细胞周期检测将GIST 430细胞用0.3μM的HQP1351、伊马替尼、普纳替尼处理24h,PI染色后用FACS Calibur流式细胞仪检测细胞周期分布;细胞凋亡检测将上述细胞处理48h后,用Annexin V-FITC/PI染色,流式细胞仪检测晚期凋亡细胞比例,每个实验设置3个复孔;结果解读:
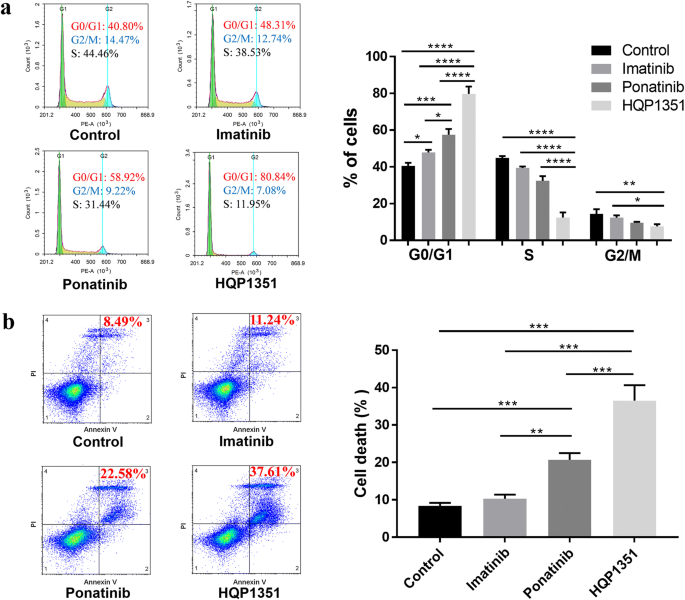
HQP1351处理组的G0/G1期细胞比例升至79.71±3.97%(P<0.0001,n=3),是伊马替尼组(47.90±1.35%)的1.66倍,普纳替尼组(57.54±3.09%)的1.39倍;晚期凋亡细胞比例升至36.54±4.11%(P<0.001,n=3),是伊马替尼组(10.31±1.10%)的3.54倍,普纳替尼组(20.69±1.80%)的1.77倍,提示HQP1351通过诱导G0/G1期细胞周期停滞和晚期细胞凋亡,显著抑制GIST细胞增殖,且作用强度优于伊马替尼和普纳替尼;产品关联:实验所用关键产品:FACS Calibur流式细胞仪(BD Biosciences, CA, USA)、Annexin-V-fluorescein isothiocyanate(FITC)/PI试剂盒。
3.5 蛋白免疫印迹(WB)信号通路检测
实验目的是解析HQP1351抑制GIST细胞增殖的分子机制,明确其对KIT下游通路的调控作用;方法细节:采用蛋白免疫印迹(WB)技术,将GIST T1和GIST 430细胞分别用不同浓度的HQP1351、伊马替尼、普纳替尼处理24h和72h,提取细胞总蛋白后,通过SDS-PAGE分离、PVDF膜转印,用KIT、磷酸化KIT(p-KIT)、AKT、磷酸化AKT(p-AKT)、ERK1/2、磷酸化ERK1/2(p-ERK1/2)、STAT3、磷酸化STAT3(p-STAT3)等一抗孵育,HRP标记的二抗结合后,用ECL试剂盒显影,β-肌动蛋白作为内参;结果解读:
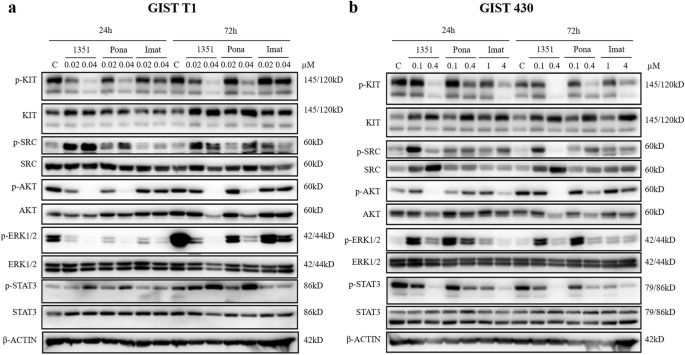
在GIST T1细胞中,HQP1351显著下调p-KIT、p-AKT、p-ERK1/2的表达,抑制效果优于伊马替尼和普纳替尼;在GIST 430细胞中,HQP1351显著下调p-KIT、p-AKT、p-STAT3的表达,即使伊马替尼使用10倍浓度,其抑制效果仍弱于HQP1351,提示HQP1351通过更高效抑制KIT激酶的磷酸化,进而阻断下游PI3K-AKT、RAS-ERK、JAK-STAT3等增殖相关通路,发挥抗肿瘤作用;产品关联:实验所用关键产品:Cell Signaling Technology的KIT、p-KIT等一抗,ECL Western Blotting Detection Kit(Yeasen Biotech Co., Ltd.)。
3.6 体内异种移植模型验证
实验目的是验证HQP1351在体内对GIST肿瘤的抑制活性,评估其疗效及安全性;方法细节:构建GIST T1细胞(Balb/c nu/nu裸鼠)和GIST 430细胞(SCID Beige免疫缺陷小鼠)的皮下异种移植模型,当肿瘤体积达到50-200mm³时,将小鼠随机分组,分别口服给予HQP1351(20/40mg/kg,每3天1次或每周1次;10/50mg/kg,每3天1次)、普纳替尼(40/50mg/kg,对应给药频率)或溶媒对照,定期测量肿瘤体积和小鼠体重,实验结束后计算相对肿瘤体积(RTV)和肿瘤抑制率(T/C%);结果解读:
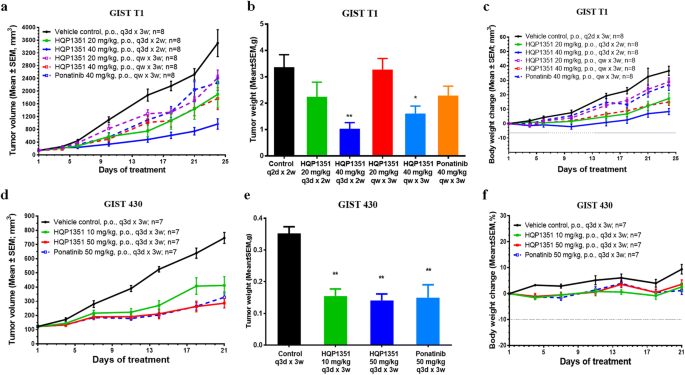
GIST T1模型中,HQP1351 40mg/kg每3天1次组的T/C为29.1%(P<0.001,n=文献未明确提供该数据,基于图表趋势推测),略优于普纳替尼组(T/C=65.0%,P<0.05);GIST 430模型中,HQP1351 50mg/kg每3天1次组的T/C为37.5%(P<0.01,n=文献未明确提供该数据,基于图表趋势推测),优于普纳替尼组(T/C=43.9%,P<0.01);所有给药组小鼠体重均无显著变化,提示HQP1351在有效剂量下具有良好的体内耐受性;产品关联:实验所用关键产品:Balb/c nu/nu小鼠(上海实验动物研究中心)、SCID Beige小鼠(Vital River Laboratory Animal Technology Co., Ltd.)、0.2% HPMC(Colorocon, Shanghai, China)溶媒。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker为KIT激酶的不同突变亚型,包括原发性外显子11突变、继发性ATP结合口袋突变和活化环突变,通过“激酶组学筛选→细胞系验证→体内模型验证”的完整逻辑链条,明确了HQP1351的敏感Biomarker类型,为临床转化应用提供了依据。
Biomarker定位:本文将KIT突变亚型作为预测HQP1351疗效的Biomarker,筛选逻辑是先通过KINOMEscan激酶分析系统,筛选HQP1351具有高结合抑制活性的KIT突变亚型,再通过携带对应突变的GIST细胞系验证其抗增殖活性,最后通过体内异种移植模型确认其抗肿瘤效果,形成了从靶点到体内的完整验证链条。研究过程详述:这些Biomarker的来源为GIST细胞系的KIT基因突变,通过PCR测序验证了GIST T1细胞的原发性外显子11突变(V559D)和GIST 430细胞的继发性外显子11/14双突变(V559D/V654A);验证方法包括激酶结合实验(检测抑制率)、CCK-8实验(检测IC50)、蛋白免疫印迹(检测通路调控)、体内异种移植实验(检测肿瘤抑制率);特异性数据显示,HQP1351对ATP结合口袋突变(V559D/V654A)的KIT激酶抑制率在100nM时>90%,对携带该突变的GIST 430细胞的IC50为0.091μM,敏感性显著高于伊马替尼(IC50=1.620μM);ROC曲线数据未在原文中提及,因此无特异性与敏感性的ROC AUC值。核心成果提炼:该Biomarker的功能关联在于,携带继发性KIT ATP结合口袋突变的伊马替尼耐药GIST患者,可能对HQP1351治疗敏感;本文的创新性在于首次证实HQP1351可通过抑制KIT下游AKT、STAT3通路,克服该类突变导致的伊马替尼耐药,且体内外疗效均优于普纳替尼;统计学结果显示,HQP1351对GIST 430细胞的增殖抑制活性显著优于伊马替尼(P<0.05,n=3),体内肿瘤抑制率显著高于对照组(P<0.01);未提及风险比(HR)数据,因此无相关统计学结果。
