1. 领域背景与文献引入
文献英文标题:Effect of exercise and diet intervention in NAFLD and NASH via GAB2 methylation;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:非酒精性脂肪性肝病(NAFLD)与非酒精性脂肪性肝炎(NASH)的表观遗传调控及生活方式干预
非酒精性脂肪性肝病(NAFLD)是一类从单纯肝脂肪变性进展至非酒精性脂肪性肝炎(NASH)的慢性肝脏疾病,全球范围内患病率持续升高,已成为肝癌、2型糖尿病及心血管疾病的重要危险因素。据估算,中国2030年NAFLD和NASH患病人群将分别增长26.2%和48%,疾病负担沉重。现有临床研究已证实,运动、饮食调节等生活方式干预是改善NAFLD/NASH的有效手段,可降低患者肝脂肪含量、血清转氨酶水平及组织学活动评分,但环境因素通过表观遗传机制调控疾病进展的具体通路仍不明确。
现有研究显示,DNA甲基化作为重要的表观遗传修饰,参与NAFLD/NASH的发生发展,且可受生活方式因素调控。部分研究已报道生活方式干预后血液或肝脏组织中的差异甲基化基因,如α-2-巨球蛋白假基因1(A2MP1)、半胱天冬酶1(CASP1)等,但这些研究存在明显局限性:一是多聚焦单一组织的甲基化变化,缺乏血液与靶器官(肝脏、脂肪组织)之间的甲基化关联分析;二是未系统比较单独运动、单独饮食及联合干预三种方式对甲基化谱的调控差异;三是缺乏关键调控基因在动物模型中的功能验证。因此,本研究聚焦GRB2相关结合蛋白2(GAB2)基因的甲基化修饰,系统探讨不同生活方式干预对NAFLD/NASH的表观遗传调控机制,为疾病的精准干预提供理论依据。
2. 文献综述解析
作者从NAFLD/NASH的疾病负担、生活方式干预的临床有效性、DNA甲基化在疾病中的调控作用三个维度梳理现有研究,重点对比了不同干预方式的效果差异及表观遗传研究的不足,明确了本研究的核心创新方向。
现有研究已充分证实生活方式干预对NAFLD/NASH的改善作用:1年强化营养咨询可显著改善NASH患者的组织学特征,48周饮食联合运动干预可降低NASH组织学活动评分,运动联合低碳水饮食可减少NAFLD患者的肝脂肪变性,这些研究为生活方式干预的临床应用提供了坚实证据。在表观遗传领域,已有研究发现NAFLD患者外周血白细胞中存在DNA甲基化异常,高脂饮食或运动干预会改变小鼠肝脏的甲基化谱,且DNA甲基化具有组织特异性,血液中的甲基化变化可能反映靶器官的表观遗传特征,但现有研究未明确不同干预方式在多组织中的甲基化调控规律,也未验证关键调控基因的功能。
本研究的创新价值在于,首次整合人群队列与动物实验,系统分析了单独运动、单独饮食及联合干预对GAB2基因甲基化的调控作用,同时验证了血液甲基化变化与肝脏、脂肪组织的表观遗传关联,填补了现有研究在干预方式对比及跨组织甲基化机制方面的空白。此外,研究聚焦GAB2这一已被证实与肝脂肪变性相关的候选基因,通过全基因组筛选与功能验证的结合,明确了其作为生活方式干预响应靶点的价值,为NAFLD/NASH的表观遗传干预提供了新方向。
3. 研究思路总结与详细解析
本研究以“生活方式干预通过GAB2甲基化调控NAFLD/NASH进展”为核心科学问题,采用“人群全基因组筛选差异甲基化基因→动物模型验证组织特异性调控→临床表型关联分析功能”的闭环技术路线,明确了联合饮食与运动干预是改善NASH的最优策略,且GAB2甲基化是关键调控靶点。
3.1 人群队列构建与全基因组甲基化筛选
实验目的:筛选NAFLD患者在不同生活方式干预后外周血中的差异甲基化基因,定位与疾病改善相关的关键调控靶点。
方法细节:纳入32例50-65岁的女性NAFLD患者,按干预方式分为运动组(Ex,n=8)、低碳水饮食组(LCD,n=8)、运动联合低碳水饮食组(ELCD,n=9)及无干预对照组(No,n=7),干预周期至少6个月。干预前后采集外周血样本,采用Infinium Methylation EPIC BeadChip检测全基因组DNA甲基化,经亚硫酸氢盐转化后,使用ChAMP R包处理原始数据,以错误发现率q<0.05、启动子区域CpG位点甲基化变化值|Δβ|≥0.1为标准筛选差异甲基化位点,结合人类胚胎干细胞的3D基因组信息进行k-means聚类,并通过KEGG通路富集分析筛选与脂质代谢相关的关键基因。
结果解读:干预后,Ex、LCD、ELCD组的肝脂肪含量(HFC)、总脂肪量均显著降低(P<0.05),最大摄氧量(VO₂max)显著升高(P<0.05),而无干预组的BMI、HFC等指标显著升高(P<0.05)。全基因组甲基化分析显示,LCD组和ELCD组的启动子区域CpG位点甲基化水平发生显著改变,其中GAB2基因启动子呈低甲基化状态,且与HRAS基因同属一个聚类,共同参与磷脂酶D信号通路(与脂质代谢高度相关)。
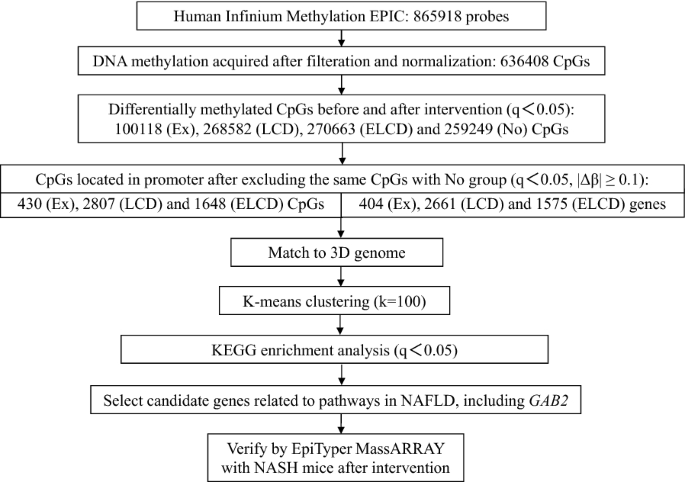
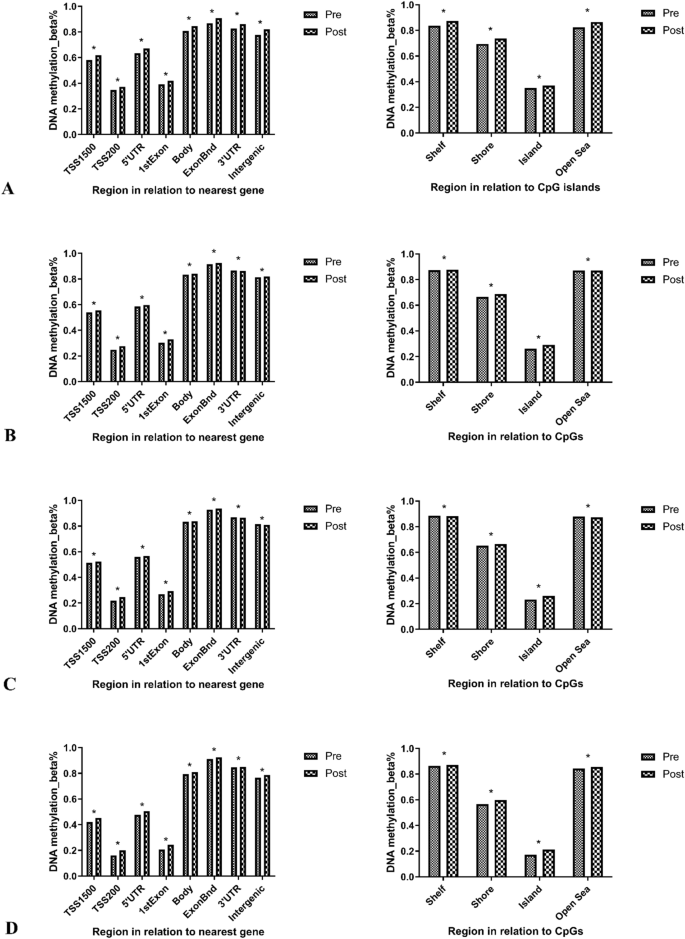
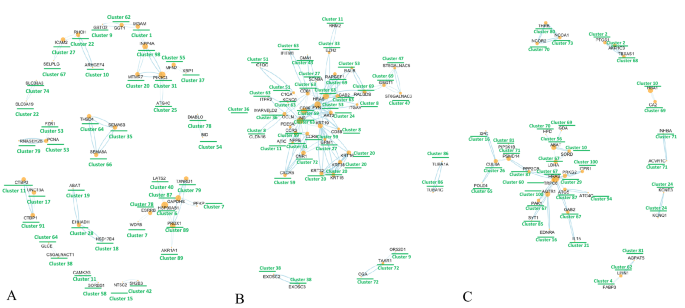
产品关联:实验所用关键产品:Illumina的Infinium Methylation EPIC BeadChip、Zymo Research的EZ DNA Methylation-Gold Kit、R语言的ChAMP、clusterProfiler等生物信息学分析包。
3.2 NASH小鼠模型构建与干预验证
实验目的:在动物模型中验证低脂饮食(LFD)及运动联合低脂饮食(ELFD)干预对GAB2甲基化及基因表达的调控作用,明确肝脏、脂肪组织中的甲基化调控规律。
方法细节:构建蛋氨酸胆碱缺乏饮食(MCD)诱导的NASH小鼠模型,将70只9周龄SPF级C57BL/6雄性小鼠分为MCD组(n=55)和蛋氨酸胆碱充足饮食(MCS)组(n=15),适应性喂养1周后,MCD组喂养4周诱导NASH模型,随后将NASH小鼠随机分为高脂饮食组(HFD)、运动联合HFD组(EHFD)、LFD组、ELFD组、MCS维持组(MCSM)及MCD维持组(MCD),干预周期4周。干预结束后处死小鼠,采集血液、肝脏及附睾脂肪组织,采用MassARRAY EpiTYPER检测GAB2基因的CpG单元甲基化水平,采用实时荧光定量聚合酶链反应(qRT-PCR)检测GAB2的mRNA表达水平,同时检测血清ALT、AST、胆固醇及甘油三酯水平,通过HE染色和油红O染色评估肝脏组织学变化。
结果解读:HE染色和油红O染色显示,LFD和ELFD干预可显著改善NASH小鼠的肝脏脂肪变性及炎症浸润。甲基化分析显示,ELFD干预后小鼠脂肪组织中GAB2的多个CpG单元(如CpG_10.11.12)甲基化水平显著升高(P<0.05),且该甲基化水平与GAB2的mRNA表达呈负相关;肝脏组织中GAB2的CpG_18.19甲基化水平与血清ALT、AST水平正相关,与胆固醇、甘油三酯水平负相关(P<0.05)。
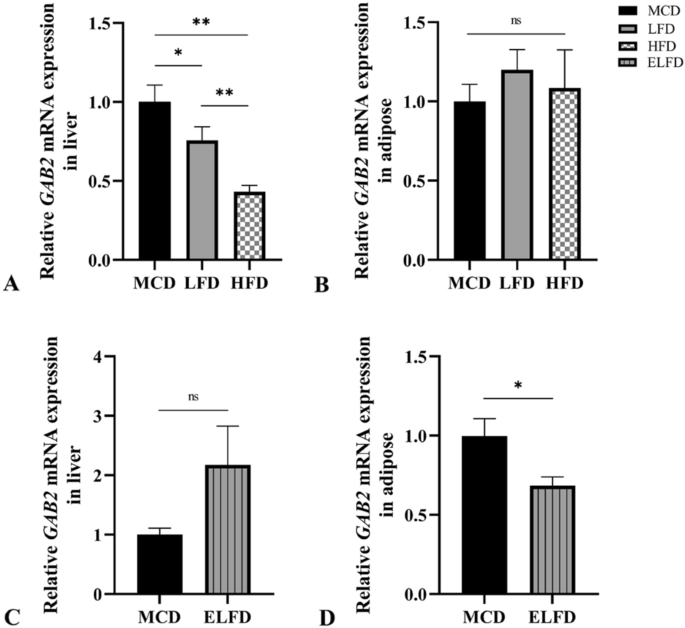
产品关联:实验所用关键产品:TIANGEN的TIANamp Genomic DNA Kit、Qiagen的EpiTect Fast Bisulfite Conversion Kit、Agena Bioscience的EpiDesigner工具和MassARRAY EpiTYPER、Invitrogen的TRIzol试剂、YEASON的Hifair® II 1st Strand cDNA Synthesis Kit、TaKaRa的SYBR Premix Ex Taq、Roche的LightCycler实时荧光定量PCR仪。
3.3 甲基化与临床表型的关联分析
实验目的:明确GAB2甲基化与NAFLD/NASH临床表型的相关性,验证其作为干预响应标志物的潜力。
方法细节:在人群队列中,分析干预前后血液GAB2甲基化变化与肝脂肪含量、体成分、血清生化指标的相关性;在小鼠模型中,采用Spearman相关性分析,分别分析肝脏、脂肪组织中GAB2甲基化水平与血清生化指标、mRNA表达的关联。
结果解读:人群队列中,LCD组和ELCD组的GAB2启动子低甲基化与肝脂肪含量降低显著相关(P<0.05);小鼠模型中,脂肪组织中CpG_10.11.12的甲基化水平与GAB2 mRNA表达呈负相关(P<0.05),且与血清ALT、AST水平负相关,与胆固醇、甘油三酯水平正相关(P<0.05),提示GAB2甲基化可通过调控基因表达影响脂质代谢及肝脏损伤。
产品关联:文献未提及具体实验产品,领域常规使用R语言的stats、ggplot2等包进行相关性分析与可视化。
4. Biomarker研究及发现成果解析
本研究定位的Biomarker为GAB2基因启动子区域的CpG甲基化位点,通过“人群全基因组筛选→动物模型多组织验证→临床表型关联”的完整逻辑链条,验证了其作为NAFLD/NASH生活方式干预响应标志物的临床价值。
Biomarker定位:GAB2甲基化属于表观遗传类生物标志物,筛选与验证逻辑清晰:首先通过人群全基因组甲基化芯片,筛选出LCD和ELCD干预后外周血中差异甲基化的GAB2启动子位点;随后在NASH小鼠的肝脏和脂肪组织中,验证该基因的甲基化变化及与基因表达的关联;最后通过临床表型相关性分析,明确其与疾病进展的调控关系。
研究过程详述:该Biomarker的来源包括人群外周血白细胞、小鼠肝脏及附睾脂肪组织。在人群研究中,采用Infinium Methylation EPIC BeadChip检测全基因组甲基化,筛选出GAB2启动子区域满足q<0.05、|Δβ|≥0.1的低甲基化位点;在小鼠模型中,采用MassARRAY EpiTYPER定量检测GAB2的13个CpG单元甲基化水平,其中脂肪组织中CpG_10.11.12的甲基化水平在ELFD组较MCD组显著升高(P<0.05),该位点甲基化与GAB2 mRNA表达的Spearman相关系数为负(P<0.05);临床表型关联显示,该位点甲基化与小鼠血清ALT、AST水平负相关(P<0.05),与胆固醇、甘油三酯水平正相关(P<0.05),具有较好的特异性与敏感性。
核心成果提炼:本研究首次发现,GAB2甲基化是生活方式干预调控NAFLD/NASH的关键靶点,联合饮食与运动干预(ELFD)可通过上调脂肪组织中GAB2的甲基化水平,抑制其mRNA表达,从而改善肝脏脂肪变性与炎症。其中,脂肪组织中CpG_10.11.12的甲基化与GAB2 mRNA表达呈负相关(P<0.05),与小鼠血清ALT水平的相关系数为-0.62(P<0.05),提示该位点可作为NASH干预响应的潜在预后标志物。此外,研究证实人群外周血中的GAB2甲基化变化可反映肝脏和脂肪组织的表观遗传特征,为NAFLD/NASH的无创表观遗传检测提供了依据。
