1. 领域背景与文献引入
文献英文标题:MST1R-targeted therapy in the battle against gallbladder cancer;发表期刊:Cell & Bioscience;影响因子:未明确提供;研究领域:胆囊癌靶向治疗
胆囊癌是第六常见的胃肠道肿瘤,整体5年生存率不足5%,多数患者确诊时已处于晚期,仅不足20%可接受根治性手术切除。领域共识:靶向治疗是肿瘤治疗的核心发展方向,但在胆囊癌中的应用仍处于探索初期,现有胆道肿瘤治疗药物疗效有限,亟需寻找更有效的治疗靶点与联合治疗策略。当前研究空白在于,MST1R(MET同源受体酪氨酸激酶)在乳腺癌、结直肠癌等多种肿瘤中已被证实具有促癌作用,但在胆囊癌中的表达特征及靶向治疗价值尚未被系统研究,缺乏针对该靶点的协同治疗方案。本文旨在通过生物信息学筛选与实验验证,确定MST1R为胆囊癌潜在治疗靶点,探索其抑制剂MGCD-265的单药疗效,并进一步挖掘联合治疗策略,为胆囊癌的精准治疗提供新方向。
2. 文献综述解析
作者对领域内现有研究的分类维度主要为胆囊癌的流行病学与治疗困境、潜在遗传靶点与信号通路研究、MST1R在其他肿瘤中的作用及靶向治疗进展。现有研究的关键结论包括:胆囊癌的发病与ABCG8、TRAF3等基因变异及Hedgehog、Wnt等通路异常密切相关;MET靶点抑制剂在胆囊癌中显示出一定的增殖抑制效果;MST1R在多种实体瘤中高表达并与不良预后相关,其抑制剂在临床前研究中展现出抗肿瘤活性。现有研究的技术方法优势在于通过生物信息学与临床样本结合筛选潜在靶点,局限性在于针对胆囊癌的有效靶向靶点数量稀少,现有药物无法满足临床需求,MST1R在胆囊癌中的功能及调控机制未被深入探索,缺乏可转化的联合治疗策略。本文的创新价值在于首次系统验证了MST1R在胆囊癌组织中的显著上调表达,明确了MGCD-265的单药抑癌作用,并发现其与JMJD6抑制剂SKLB325的协同抗肿瘤效果,填补了胆囊癌MST1R靶向治疗及联合策略的研究空白。
3. 研究思路总结与详细解析
本文的研究目标是筛选并验证胆囊癌的潜在治疗靶点,探索MST1R抑制剂的疗效及联合治疗策略;核心科学问题是MST1R在胆囊癌中的功能及调控机制,以及如何通过联合治疗增强抑癌效果;技术路线逻辑为“生物信息学筛选靶点→体外细胞实验验证→体内动物实验验证→转录组测序解析机制→联合治疗策略探索”的完整闭环。
3.1 生物信息学筛选与潜在靶点确定
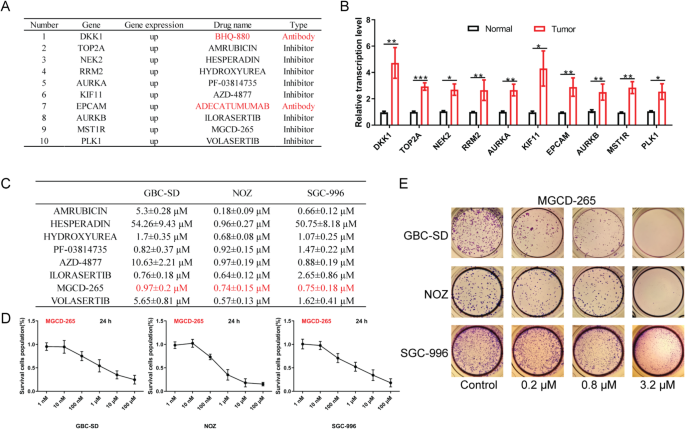
实验目的是从胆囊癌组织与癌旁组织的差异表达基因中筛选具有治疗潜力的靶点。方法细节为获取GEO数据库中GSE74948数据集(包含3例癌组织样本与3例正常组织样本),利用R包limma进行差异表达分析,设定筛选阈值为P<0.05且|logFC|>2,通过KEGG、GO富集分析差异基因的功能特征,借助STRING数据库构建蛋白互作网络,最后通过DGIdb数据库筛选靶点对应的小分子抑制剂。结果解读为共鉴定出3553个差异表达基因,其中1058个基因显著上调、2495个基因显著下调,MST1R为核心上调基因之一;DGIdb数据库筛选得到MST1R抑制剂MGCD-265,后续CCK-8实验显示其对GBC-SD、NOZ、SGC-996三种胆囊癌细胞系的IC₅₀分别为0.97±0.2μM、0.74±0.15μM、0.75±0.18μM(n=3,P<0.05),表明细胞对该抑制剂高度敏感。
产品关联:文献中使用的生物信息学工具包括GEO数据库、STRING数据库、DGIdb数据库,分析软件为R语言的limma、clusterProfiler包,未提及具体实验试剂品牌。
3.2 体外细胞实验验证MGCD-265的抑癌作用
实验目的是验证MGCD-265对胆囊癌细胞的增殖抑制、周期阻滞及凋亡诱导作用。方法细节为采用CCK-8实验检测不同浓度MGCD-265处理后细胞的增殖活力,克隆形成实验检测细胞长期增殖能力,流式细胞术分析细胞周期分布与凋亡率,蛋白免疫印迹(Western blot)检测周期及凋亡相关蛋白的表达变化;实验使用的细胞系为GBC-SD、NOZ、SGC-996,药物处理时间为24h,浓度梯度设置为0.2μM、0.8μM、3.2μM。结果解读为CCK-8与克隆形成实验显示MGCD-265以剂量依赖方式抑制细胞增殖(n=3,P<0.01);流式细胞术结果显示G0/G1期细胞比例显著增加,G2/M期比例降低(n=3,P<0.05),细胞凋亡率随药物浓度升高而上升(n=3,P<0.01);蛋白免疫印迹结果显示周期相关蛋白CDK4、Cyclin D1、Cyclin B1表达下调,细胞周期抑制剂P21表达上调,凋亡相关蛋白活化型半胱天冬酶3(Cleaved-caspase3)、活化型多聚腺苷二磷酸核糖聚合酶(Cleaved-PARP)表达上调(n=3,P<0.05)。
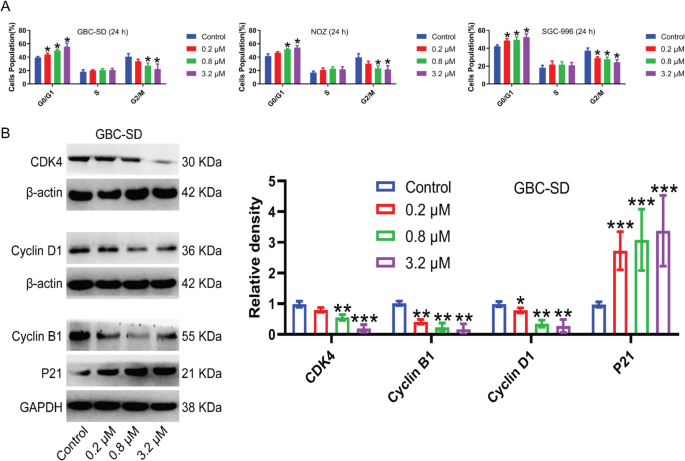
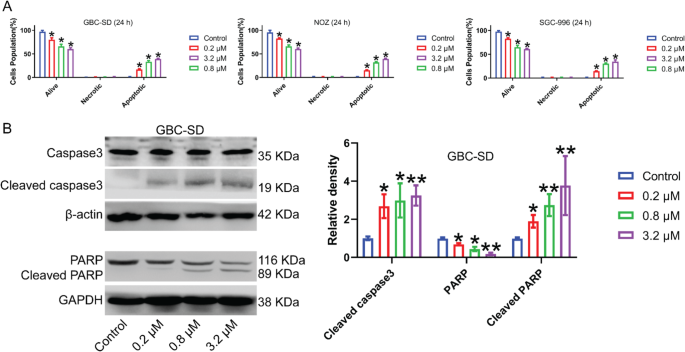
产品关联:实验所用关键产品:MGCD-265(Selleck,货号#S1361)、CCK-8试剂盒(Selleck,货号#B34304)、流式细胞术凋亡检测试剂盒(KeyGEN BioTECH,货号#KGA1102-100)、蛋白免疫印迹抗体包括抗-CDK4(Abcam,货号ab137675)、抗-Cleaved-caspase3(Cell Signaling Technology,货号#9664)等。
3.3 体内动物实验验证MGCD-265的疗效
实验目的是验证MGCD-265在体内的抑癌效果及安全性。方法细节为构建GBC-SD细胞的裸鼠皮下移植瘤模型,待肿瘤体积达约100mm³时,将小鼠随机分为对照组、5mg/kg MGCD-265组、10mg/kg MGCD-265组,每日通过灌胃方式给药,连续给药12天,每3天测量肿瘤体积与小鼠体重,28天后处死小鼠,取肿瘤及肝、肾组织进行苏木精-伊红(HE)染色、免疫组化(IHC)及蛋白免疫印迹检测。结果解读为5mg/kg与10mg/kg组的肿瘤体积显著小于对照组(文献未明确提供该数据,基于图表趋势推测,P<0.01),且呈现剂量依赖效应;小鼠体重无显著变化,肝、肾组织HE染色显示无明显病理损伤;蛋白免疫印迹结果显示肿瘤组织中Cleaved-caspase3表达上调,Cyclin D1、Cyclin B1表达下调,免疫组化结果显示Cleaved-caspase3阳性细胞数量增加,CDK4、CDK6表达下调(文献未明确提供该数据,基于图表趋势推测,P<0.05)。
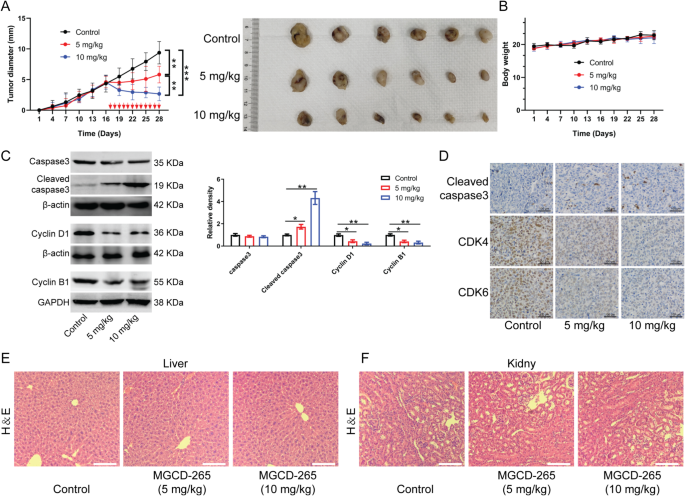
产品关联:实验所用关键产品:MGCD-265(Selleck,货号#S1361)、HE染色试剂盒(Beyotime Biotechnology,货号#C0105S)、免疫组化抗体包括抗-Cleaved-caspase3(Cell Signaling Technology,货号#9664)、抗-CDK4(Abcam,货号ab137675)等。
3.4 转录组测序与下游调控通路分析
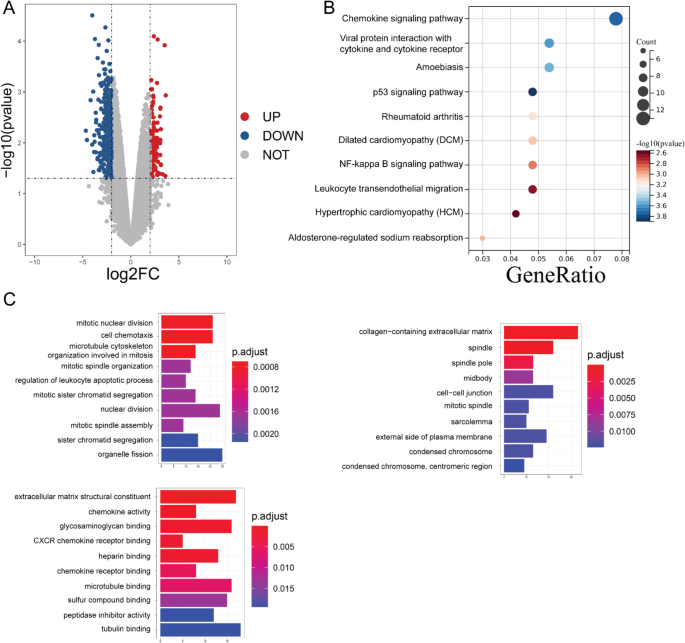
实验目的是解析MGCD-265发挥抑癌作用的分子机制,筛选潜在的联合治疗靶点。方法细节为用0.8μM MGCD-265处理GBC-SD细胞24h后提取总RNA,通过Illumina HiSeq X平台进行转录组测序,分析差异表达基因的特征,通过KEGG、GO富集分析差异基因参与的信号通路,最后采用实时荧光定量PCR(RT-qPCR)验证核心差异基因的表达变化。结果解读为共鉴定出200个上调基因、883个下调基因,KEGG富集分析显示差异基因主要参与蛋白消化吸收、细胞黏附等通路,GO富集分析涉及细胞外周、细胞外基质结构组成等功能;RT-qPCR验证结果显示JMJD6等基因表达显著上调(n=3,P<0.05)。
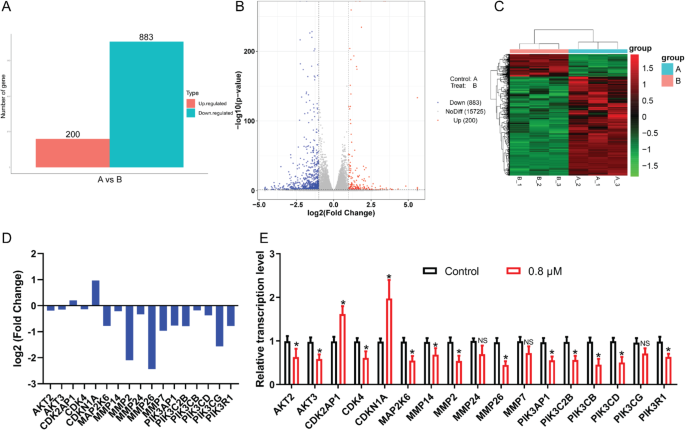
产品关联:实验所用关键产品:TRIzol™ LS总RNA提取试剂(Invitrogen,货号#10296010)、RT-qPCR试剂盒(Nanjing Vazyme Biotechnology,货号#R233-01、#Q111-02)、Illumina HiSeq X测序平台。
3.5 联合治疗策略的探索与验证
实验目的是验证MGCD-265与JMJD6抑制剂SKLB325的协同抑癌作用。方法细节为用MGCD-265与SKLB325联合处理三种胆囊癌细胞系,通过King公式计算Q值评估协同作用;构建裸鼠皮下移植瘤模型,分为对照组、MGCD-265单药组、SKLB325单药组、联合治疗组,定期测量肿瘤体积与小鼠体重,实验结束后取肿瘤组织进行免疫组化检测。结果解读为联合处理的Q值均大于1.15,显示显著协同抑癌作用(n=3,P<0.01);体内实验显示联合治疗组的肿瘤体积显著小于单药组(文献未明确提供该数据,基于图表趋势推测,P<0.01),小鼠体重无显著差异,免疫组化结果显示CDK4、CDK6表达显著下调(文献未明确提供该数据,基于图表趋势推测,P<0.05)。
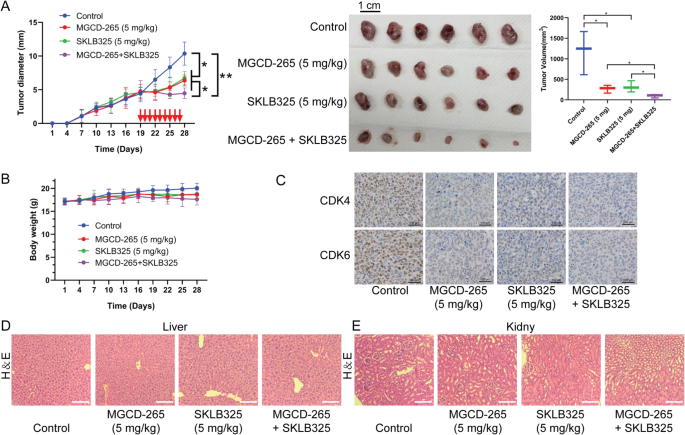
产品关联:实验所用关键产品:SKLB325(JMJD6抑制剂)、免疫组化抗体包括抗-CDK4(Abcam,货号ab137675)等。
4. Biomarker研究及发现成果
本文涉及的Biomarker为MST1R,属于治疗性Biomarker,其筛选与验证逻辑为“GEO数据库临床样本差异筛选→胆囊癌细胞系功能验证→裸鼠移植瘤模型体内验证→转录组测序解析下游调控通路”的完整链条。
MST1R的来源为GEO数据库中的胆囊癌临床组织样本与体外培养的胆囊癌细胞系,验证方法包括RT-qPCR、蛋白免疫印迹、免疫组化检测其表达水平,通过CCK-8、克隆形成实验验证抑制剂的特异性抑癌效果。特异性数据显示,MST1R在胆囊癌组织中的表达水平显著高于癌旁组织(logFC>2,P<0.05);敏感性数据显示,MGCD-265对三种胆囊癌细胞系的IC₅₀均低于1μM,表明细胞对该抑制剂高度敏感。
核心成果总结:MST1R可作为胆囊癌的潜在治疗靶点,其抑制剂MGCD-265通过诱导细胞周期阻滞与凋亡发挥显著的体内外抑癌作用;MGCD-265与JMJD6抑制剂SKLB325联合使用可产生协同抑癌效果,为胆囊癌的联合靶向治疗提供了新策略。创新性在于首次系统揭示了MST1R在胆囊癌中的促癌作用及调控机制,首次证实了MST1R与JMJD6抑制剂的协同治疗价值,相关统计学结果显示联合处理的Q值均大于1.15(n=3,P<0.01),体内肿瘤体积抑制率显著高于单药组(文献未明确提供该数据,基于图表趋势推测,P<0.01)。