1. 领域背景与文献引入
文献英文标题:KSRP-PMR1-exosome association determines parathyroid hormone mRNA levels and stability in transfected cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:甲状旁腺激素(PTH)mRNA转录后调控、RNA降解机制。
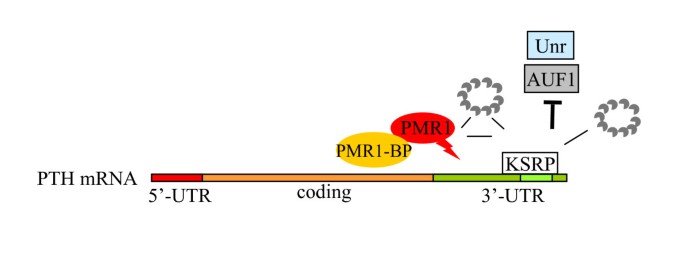
甲状旁腺激素(PTH)是调控血清钙磷稳态和骨代谢的核心激素,其基因表达主要在转录后水平受到精准调控,其中PTH mRNA 3"-非翻译区(3"-UTR)的AU富集元件(ARE)是关键调控位点。领域共识:目前已知多种反式作用蛋白可结合ARE元件调控PTH mRNA稳定性,其中AU富集结合因子1(AUF1)和N-ras上游蛋白(Unr)发挥稳定mRNA的作用,而KH型剪接调控蛋白(KSRP)通过招募外切体复合物(exosome)介导PTH mRNA的3"-5"外切降解。然而,现有研究主要聚焦于外切核酸酶介导的降解途径,对于ARE元件是否能通过招募内切核酸酶参与mRNA降解的机制尚未明确,这一空白限制了对PTH基因转录后调控网络的全面理解,也无法解释ARE介导的mRNA快速降解的动力学过程。针对这一研究空白,本研究旨在探究内切核酸酶是否参与PTH mRNA的降解,以及KSRP、外切体和内切酶的协同作用机制,为RNA转录后调控的研究提供新的范式。
2. 文献综述解析
作者以RNA调控蛋白的功能差异(稳定/降解)和RNA降解的途径类型(外切/内切)为核心分类维度,系统梳理了PTH mRNA转录后调控及ARE介导的RNA降解领域的研究进展,明确了现有研究的核心结论、技术优势与局限性,并在此基础上提出了本研究的创新方向。
现有研究已证实PTH mRNA的稳定性主要由其3"-UTR的ARE元件调控,AUF1和Unr通过直接结合ARE元件形成稳定复合物,抑制mRNA的降解;KSRP则通过其KH结构域招募外切体复合物,启动PTH mRNA的3"-5"外切降解过程,这一结论已在体外降解实验和细胞实验中得到验证,技术上采用的甲状旁腺提取物体外降解实验(IVDA)和细胞转染模型具有较高的特异性,能直接反映PTH mRNA的调控机制。同时,ARE元件作为多种不稳定mRNA的保守调控位点,已知的降解途径还包括XrnI介导的5"-3"外切降解,少数内切核酸酶如多聚体核糖核酸酶1(PMR1)被发现参与白蛋白等特定mRNA的降解,但PMR1是否参与PTH mRNA的调控尚未见报道。现有研究的局限性在于,对PTH mRNA降解的研究仅关注外切途径,缺乏对内切酶参与的机制探讨,且KSRP是否能协同内切酶和外切体共同调控mRNA稳定性的分子机制尚未明确,无法全面解释ARE介导的mRNA快速降解的动力学过程。
通过对比现有研究的未解决问题,本研究的创新点在于首次发现内切核酸酶PMR1参与PTH mRNA的降解过程,且该过程依赖于ARE元件、KSRP和外切体的协同作用,突破了以往仅关注外切降解的研究局限,揭示了ARE介导的mRNA降解的新机制——即同时涉及内切切割与外切降解的协同作用,为RNA转录后调控的研究提供了新的范式。
3. 研究思路总结与详细解析
本研究的核心目标是明确PTH mRNA降解的全新分子机制,核心科学问题为PMR1是否参与PTH mRNA的降解,以及KSRP、外切体与PMR1之间的相互作用及功能协同关系,技术路线遵循“假设提出→细胞水平验证→分子相互作用验证→功能依赖验证→机制模型构建”的闭环逻辑,系统解析了PMR1介导的PTH mRNA降解机制。
3.1 PMR60对PTH mRNA及蛋白水平的特异性调控验证
实验目的:验证活性形式的PMR1(PMR60)是否能特异性降低PTH mRNA及蛋白水平,并明确ARE元件的调控作用。
方法细节:采用人胚肾293(HEK293)细胞作为模型,通过钙磷共转染法将Myc标记的PMR60表达质粒与大鼠/人PTH表达质粒共转染,同时设置人生长激素(GH)mRNA、荧光素酶mRNA、内源性L32核糖体蛋白mRNA作为阴性对照;转染48小时后,通过Northern blot检测mRNA表达水平,采用ELISA试剂盒检测细胞培养基中分泌的PTH蛋白水平;构建缺失ARE元件的PTH mRNA表达质粒,验证ARE元件的必要性;构建含PTH mRNA 63nt ARE元件的GH报告基因(GH63),验证ARE元件的充分性。
结果解读:Northern blot结果显示,PMR60过表达可使大鼠和人PTH mRNA水平显著降低(n=3-4,P<0.05),而对GH mRNA、L32 mRNA的表达水平无显著影响;ELISA结果显示,PTH蛋白的分泌水平随mRNA水平同步降低(n=2-3,P<0.05);缺失ARE元件的PTH mRNA不受PMR60的调控,而含ARE元件的GH63 mRNA被PMR60显著下调,说明PMR60通过ARE元件特异性调控PTH mRNA的稳态水平。
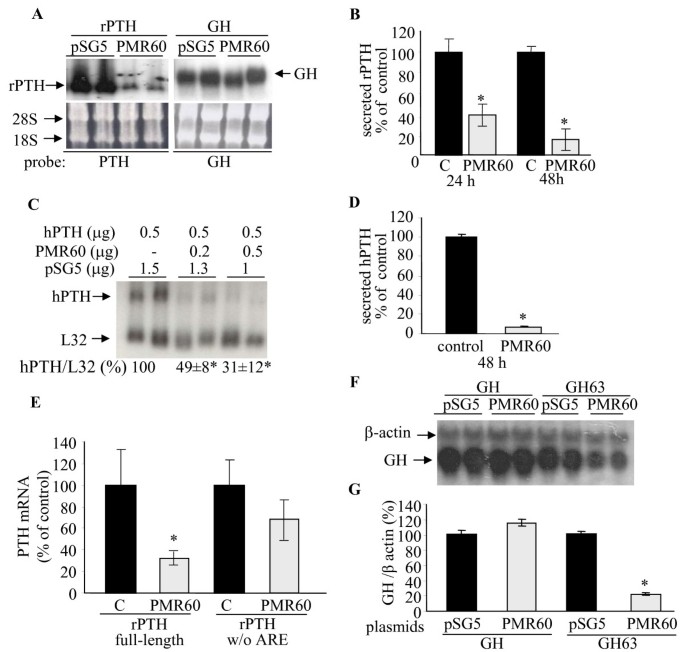
实验所用关键产品:Sigma的Ca-P转染试剂盒、Invitrogen的Lipofectamine 2000转染试剂、Immunotopics的大鼠/人完整PTH ELISA试剂盒、Cell Signaling的抗Myc抗体、Sigma的抗Flag、抗α-微管蛋白、抗GFP抗体。
3.2 PMR60与PTH mRNA的直接结合及体外切割验证
实验目的:验证PMR60是否直接结合PTH mRNA,并对其进行特异性内切切割。
方法细节:将催化失活的PMR60⁰(避免mRNA被切割)与PTH、荧光素酶表达质粒共转染HEK293细胞,通过IgG亲和纯化PMR60⁰复合物,采用RT-PCR检测复合物中结合的mRNA;同时从转染细胞中纯化活性PMR60,与体外转录的³²P标记的PTH mRNA、GH mRNA共孵育,通过琼脂糖凝胶电泳和放射自显影检测切割产物;采用3"末端标记的PTH mRNA,通过尿素-PAGE电泳检测具体的切割位点。
结果解读:RT-PCR结果显示,PMR60⁰可特异性结合PTH mRNA,而不结合荧光素酶mRNA,证明PMR60与PTH mRNA存在直接相互作用;体外切割实验显示,活性PMR60可特异性切割PTH mRNA,而对GH mRNA无切割作用;3"末端标记实验显示,切割位点位于PTH mRNA 3"末端约70nt处,对应ARE元件区域的UG二核苷酸位点,与PMR1的偏好切割位点一致。
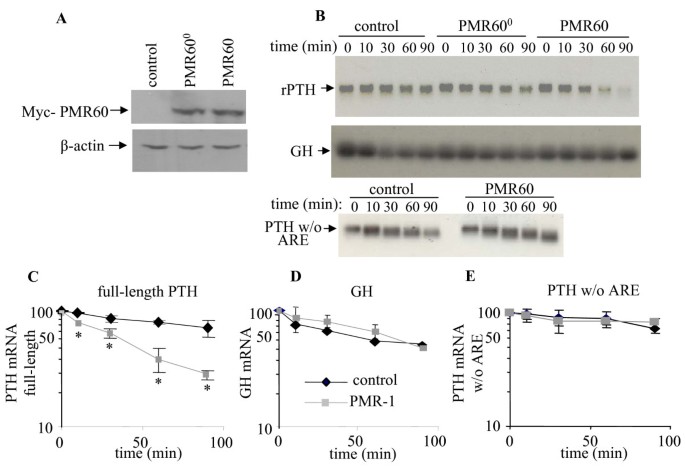
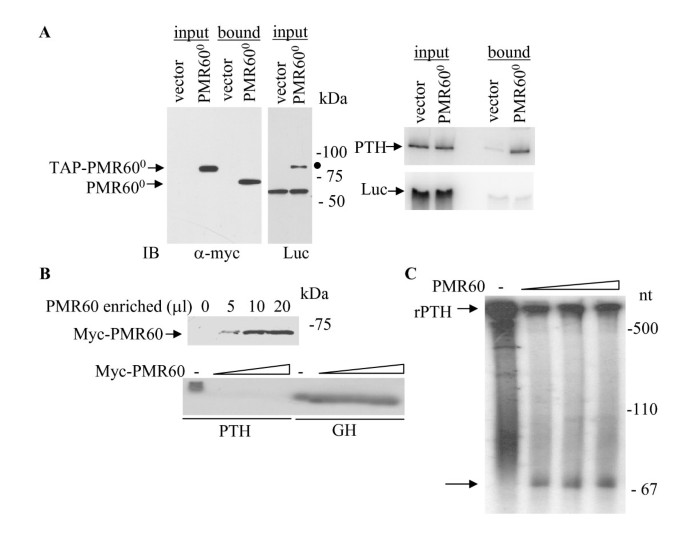
文献未提及具体实验产品,领域常规使用RNA体外转录试剂盒、放射自显影试剂、尿素-PAGE凝胶制备试剂等。
3.3 PMR60与KSRP、外切体的相互作用验证
实验目的:验证PMR60是否与KSRP、外切体组分存在直接相互作用,并明确相互作用的结构域。
方法细节:将PMR60与Flag标记的KSRP全长或KH结构域缺失突变体(KH1-4、KH3-4)共转染HEK293细胞,通过TAP标签亲和纯化复合物,采用免疫印迹检测相互作用;将PMR60⁰与Flag标记的外切体组分Rrp4共转染Cos-1细胞,通过免疫共沉淀检测相互作用;同时用RNase A和T1处理细胞提取物,验证相互作用是否依赖RNA。
结果解读:免疫印迹结果显示,PMR60与内源性KSRP及外源性KSRP全长、KH1-4结构域、KH3-4结构域均能形成稳定复合物,且该相互作用在RNase处理后仍存在,说明不依赖RNA;免疫共沉淀结果显示,PMR60⁰与外切体组分Rrp4特异性结合,证明PMR60可与KSRP、外切体形成三元复合物。
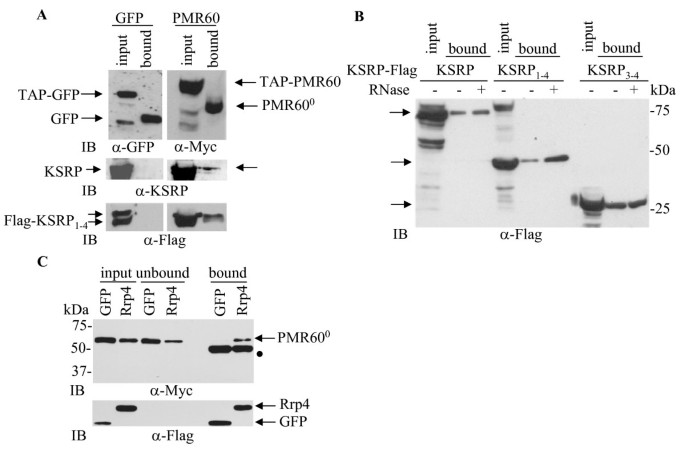
实验所用关键产品:Sigma的抗Flag抗体、自制的抗KSRP抗体。
3.4 KSRP和外切体在PMR60介导的PTH mRNA降解中的功能验证
实验目的:验证KSRP和外切体是否为PMR60调控PTH mRNA所必需的功能组分。
方法细节:采用QIAGEN的siRNA寡核苷酸分别敲低HEK293细胞中的KSRP、外切体组分Rrp46,同时转染PMR60和PTH表达质粒;转染72小时后,通过免疫印迹检测蛋白敲低效率,通过Northern blot检测PTH mRNA的表达水平。
结果解读:免疫印迹结果显示,Rrp46的敲低效率约为70%,KSRP的敲低效率约为60%;Northern blot结果显示,敲低Rrp46可显著升高PTH mRNA水平(n=3,P<0.05),并完全逆转PMR60介导的PTH mRNA下调;敲低KSRP可显著升高PTH mRNA水平(n=3,P<0.05),并部分逆转PMR60介导的PTH mRNA下调,说明KSRP和外切体均参与PMR60介导的PTH mRNA降解过程,其中外切体是必需组分,KSRP发挥协同作用。
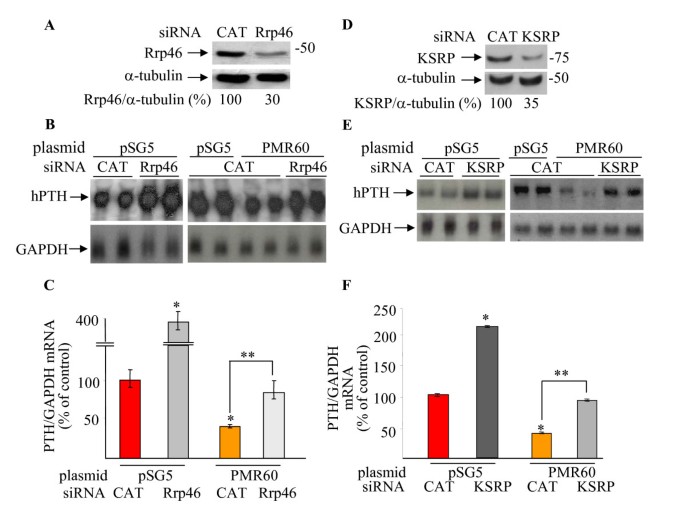
实验所用关键产品:QIAGEN的siRNA寡核苷酸、Invitrogen的Lipofectamine 2000转染试剂。
4. Biomarker研究及发现成果解析
本研究中涉及的核心Biomarker为PTH mRNA 3"-UTR的ARE元件,以及KSRP-PMR1-外切体形成的RNA降解复合物,其筛选与验证遵循“元件功能验证→分子相互作用验证→功能依赖验证”的完整逻辑链条。
ARE元件来源于PTH mRNA的3"-UTR区域(63nt),验证方法包括缺失突变实验、报告基因实验、体外切割实验;RNA降解复合物的验证方法包括蛋白-蛋白相互作用实验、siRNA功能敲低实验。特异性与敏感性数据显示,ARE元件缺失后,PMR60对PTH mRNA的调控作用完全消失(n=5,P<0.05),证明ARE元件是PMR60调控的特异性靶点;KSRP的KH3-4结构域是与PMR60结合的必需区域,该相互作用的特异性通过缺失突变实验得到验证;敲低外切体组分Rrp46可完全阻断PMR60的调控作用,敲低KSRP可部分阻断,说明复合物的功能具有高度的依赖性。
本研究的核心成果在于首次揭示了ARE介导的PTH mRNA降解的全新机制,即KSRP作为接头蛋白,同时招募内切核酸酶PMR1和外切体复合物到PTH mRNA的ARE元件上,PMR1首先对PTH mRNA进行内切切割,随后外切体对切割后的片段进行3"-5"外切降解,两者协同作用快速降低PTH mRNA的水平。该Biomarker的功能关联为:ARE元件作为PTH mRNA稳定性的核心调控位点,其与KSRP、PMR1、外切体的相互作用直接决定了PTH mRNA的半衰期;创新性在于首次在PTH mRNA调控中发现内切与外切核酸酶的协同作用,突破了以往仅关注外切降解的研究局限。统计学结果显示,PMR60过表达使PTH mRNA水平降低约50%(n=3,P<0.05),敲低Rrp46使PTH mRNA水平升高约2倍(n=3,P<0.05),敲低KSRP使PTH mRNA水平升高约1.5倍(n=3,P<0.05)。