1. 领域背景与文献引入
文献英文标题:Aggresomes do not represent a general cellular response to protein misfolding in mammalian cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(蛋白质错误折叠与细胞应激反应)
蛋白质错误折叠导致的蛋白聚集体形成是阿尔茨海默病、帕金森病、朊病毒病等神经退行性疾病,以及α1-抗胰蛋白酶缺乏症、家族性淀粉样心肌病等系统性疾病的核心病理特征。领域共识:早期细胞模型研究通过过表达疾病相关突变蛋白,发现错误折叠蛋白会在细胞中心体附近形成近核聚集体(aggresome),并提出聚集体形成是细胞应对错误折叠蛋白的通用保护性反应,其形成依赖微管网络、组蛋白去乙酰化酶6(HDAC6)调控及蛋白酶体功能。然而临床病理观察显示,并非所有蛋白质错误折叠疾病都以聚集体为显著病理特征,这一细胞模型与临床现象的矛盾成为领域未解决的核心问题:聚集体是否真的是错误折叠蛋白在细胞内的必然产物?针对这一认知空白,本研究通过多细胞系对比实验,系统验证错误折叠蛋白的聚集体形成模式,为理解疾病病理多样性提供实验依据。
2. 文献综述解析
作者以“研究模型的层级差异”为分类维度,梳理了领域内关于聚集体形成的研究:首先是细胞模型研究,过表达多种疾病相关突变蛋白(如帕金森病的α-突触核蛋白、朊病毒病的朊蛋白)均能诱导聚集体形成,这类研究明确了聚集体的形态特征(近核定位、波形蛋白笼状包裹)及调控机制(依赖HDAC6、微管网络),证明细胞具备聚集体形成的分子基础,但研究多局限于特定细胞系或特定蛋白,未验证聚集体形成的通用性;其次是动物模型研究,部分神经退行性疾病模型中发现类聚集体结构,如肌萎缩侧索硬化小鼠模型中的突变超氧化物歧化酶聚集体,为聚集体与疾病的关联提供了体内证据,但模型与人类病理的对应性仍需验证;最后是临床病理研究,明确指出并非所有人类神经退行性疾病都以聚集体为主要病理特征,这与细胞模型的普遍结论存在显著差异,但现有研究未解释这一差异的机制。
现有研究的局限性在于,未系统对比不同细胞系中错误折叠蛋白的聚集体形态,也未明确聚集体形成的细胞特异性调控因素。本研究的创新价值在于,首次通过跨细胞系的系统实验,证明错误折叠蛋白可形成聚集体或分散型聚集体两种形态,且聚集体并非错误折叠蛋白的必然产物,直接填补了领域内对聚集体形成通用性的研究空白,解释了细胞模型与临床病理的差异根源。
3. 研究思路总结与详细解析
本研究的核心目标是验证聚集体是否为哺乳动物细胞应对错误折叠蛋白的通用反应,核心科学问题是错误折叠蛋白的聚集体形态是否具有细胞系依赖性,技术路线遵循“假设提出→多细胞系验证→调控因素筛选→功能差异分析→结论推导”的闭环逻辑,通过构建错误折叠蛋白表达体系、对比不同细胞系的聚集体形态、验证关键调控因子、分析聚集体功能差异,系统解答科学问题。
3.1 错误折叠蛋白表达体系构建与多细胞系形态观察
实验目的:构建可可视化的错误折叠蛋白表达模型,观察不同哺乳动物细胞系中错误折叠蛋白的聚集体形态差异。
方法细节:构建融合增强型绿色荧光蛋白(EGFP)的胞质型朊蛋白(CyPrP^EGFP)及另一种经典聚集体形成蛋白GFP-250的表达载体,采用Lipofectamine 2000转染小鼠神经母细胞瘤N2a、人宫颈癌细胞Hela、猴成纤维细胞COS-7、人肝癌细胞Huh-7等6种细胞系,转染24小时后通过荧光显微镜观察聚集体的定位与形态。
结果解读:在N2a细胞中,CyPrP^EGFP和GFP-250均形成典型的近核聚集体(图1A);而在Hela、COS-7、Huh-7等细胞系中,两种蛋白均形成无近核定位的分散型聚集体(图1A)。蔗糖梯度离心结果显示,聚集体与分散型聚集体的密度存在显著差异(图1C);时间动态观察显示,N2a细胞在转染24小时后聚集体成为主要形态,而超过80%的Hela细胞在转染96小时后仍维持分散型聚集体(n=3,每组计数细胞>200)(图1E)。
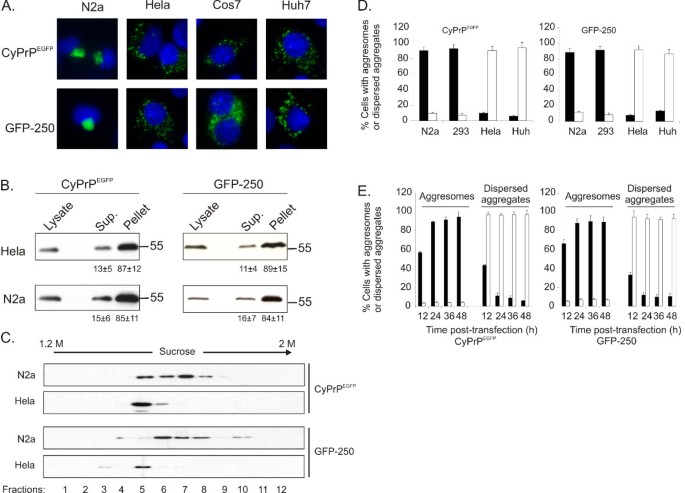
产品关联:实验所用关键产品:Chemicon的抗朊蛋白单克隆抗体(克隆3F4)、Molecular Probes的抗α-微管蛋白单克隆抗体、Sigma的抗波形蛋白单克隆抗体、Invitrogen的Lipofectamine 2000转染试剂。
3.2 聚集体形态的调控因素验证
实验目的:验证蛋白表达水平、蛋白酶体功能、HDAC6活性及微管网络对聚集体形态的调控作用。
方法细节:采用四环素调控表达载体,通过添加不同浓度四环素调节CyPrP^EGFP的表达水平;使用蛋白酶体抑制剂环氧霉素和MG132处理细胞;使用HDAC6抑制剂tubacin和scriptaid及其无活性结构类似物处理细胞;使用微管解聚剂nocodazole处理细胞,观察不同处理下聚集体形态的变化。
结果解读:无论表达水平高低,N2a细胞中均形成聚集体,Hela细胞中均形成分散型聚集体(图3);蛋白酶体抑制剂处理未诱导Hela细胞中分散型聚集体向聚集体转化;HDAC6抑制剂可完全抑制N2a细胞中聚集体的形成,但对Hela细胞的分散型聚集体无影响(图2A);微管解聚剂nocodazole可抑制N2a细胞的聚集体形成,但不影响Hela细胞的分散型聚集体(图2A)。免疫荧光结果显示,N2a细胞中聚集体周围存在波形蛋白的笼状包裹结构,而Hela细胞中波形蛋白分布无明显变化(图2B)。
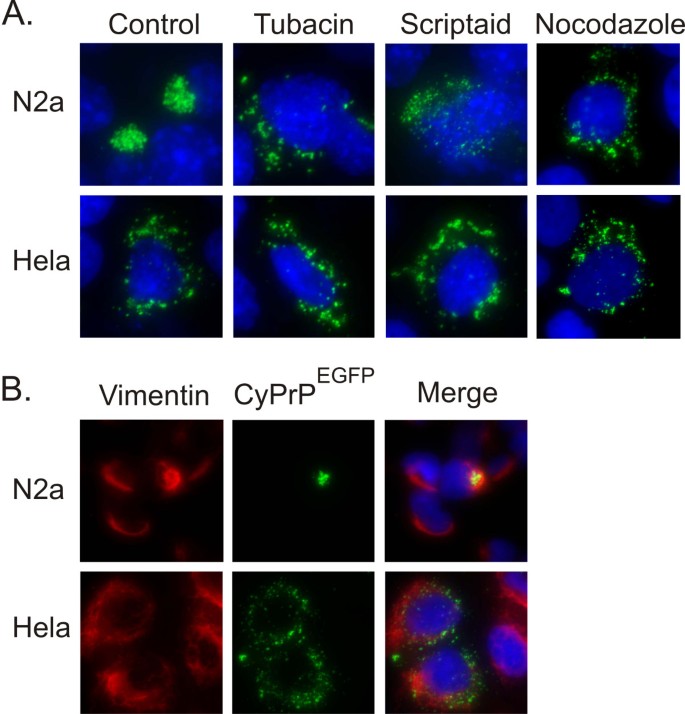
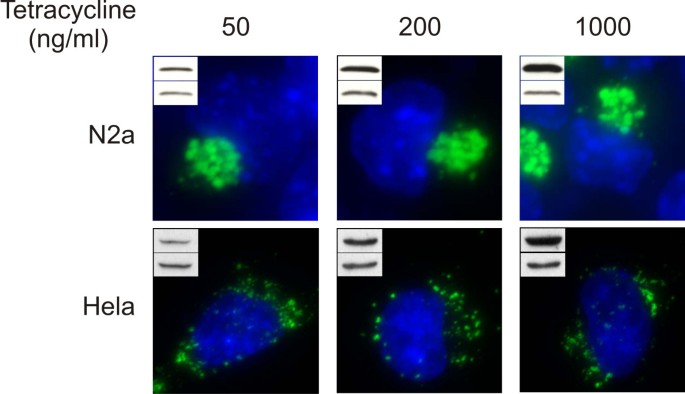
产品关联:文献未提及部分实验产品的具体品牌,领域常规使用四环素调控表达系统、蛋白酶体抑制剂、HDAC6抑制剂、微管解聚剂等试剂。
3.3 聚集体的分子组装与细胞功能差异分析
实验目的:对比聚集体与分散型聚集体的分子组装特征及对细胞生理功能的影响。
方法细节:构建融合四聚体荧光蛋白DsRed2及单体荧光蛋白mOrange的CyPrP融合蛋白,转染细胞后观察荧光信号以判断蛋白分子的组装空间限制;通过原位杂交检测聚腺苷酸(poly(A)+)RNA的分布,通过35S代谢标记检测细胞蛋白质翻译水平。
结果解读:CyPrP^DsRed2在两种细胞系中均无荧光信号,但免疫荧光可检测到聚集体,而CyPrP^mOrange则显示正常荧光信号(图4),说明两种聚集体中CyPrP分子的空间排列均限制了四聚体DsRed2的正确组装;N2a细胞中聚集体可诱导poly(A)+RNA聚集并显著抑制蛋白质翻译,而Hela细胞中分散型聚集体对poly(A)+RNA分布及蛋白质翻译无明显影响(图5)。

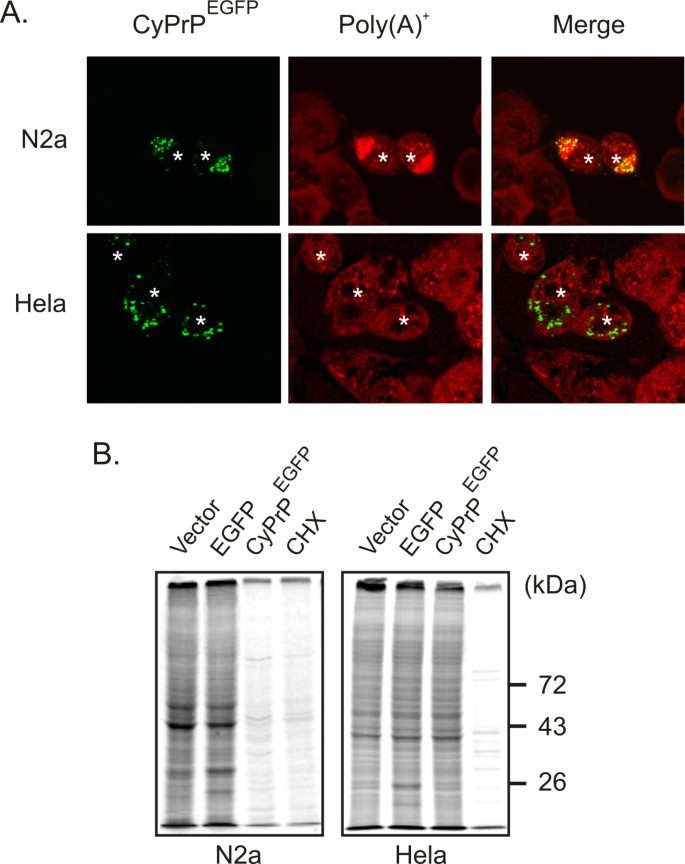
产品关联:实验所用关键产品:Perkin-Elmer的35S标记混合物、Molecular Probes的Alexa Fluor 633标记链霉亲和素。
4. Biomarker研究及发现成果
Biomarker定位
本文未聚焦疾病诊断、预后或疗效预测类生物标志物的研究,而是针对细胞内错误折叠蛋白聚集体这一功能分子实体,系统验证其形态多样性、调控机制及功能差异,属于细胞应激反应机制的基础研究范畴。
研究过程详述
本研究以胞质型朊蛋白(CyPrP)为模式错误折叠蛋白,在6种不同哺乳动物细胞系中观察其聚集体形态,明确错误折叠蛋白可形成聚集体或分散型聚集体两种形态,且形态具有细胞系依赖性;通过调控表达水平、抑制蛋白酶体功能、抑制HDAC6活性及解聚微管等实验,证明聚集体形成依赖HDAC6及微管网络,而分散型聚集体的形成不受这些因素调控;通过荧光蛋白融合实验,证明两种聚集体的分子组装空间限制特征相似,但对细胞内RNA分布及蛋白质翻译功能的影响存在显著差异。
核心成果提炼
本研究的核心成果是首次证明聚集体并非哺乳动物细胞应对错误折叠蛋白的通用反应,错误折叠蛋白的聚集体形态具有细胞系特异性,且不同形态聚集体对细胞生理功能的影响存在差异。这一发现解释了“为何并非所有人类蛋白质错误折叠疾病都以聚集体为显著病理特征”的领域矛盾,为理解疾病病理多样性提供了实验依据。研究所有实验数据均来自至少3次独立重复实验,每组计数细胞超过200个,结果具有统计学可靠性。
