1. 领域背景与文献引入
文献英文标题:Assessment of changes in autophagic vesicles in human immune cell lines exposed to nano particles;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:纳米毒理学与免疫细胞自噬调控。
领域共识:纳米材料在医学诊断、药物递送及消费品领域的应用呈指数增长,其生物相容性评估是临床转化的核心前提。自噬作为维持细胞稳态的关键通路,与细胞健康、炎症反应密切相关,2010年后的研究证实纳米材料可通过溶酶体功能障碍、自噬通量抑制等多种方式调控自噬,自噬紊乱已被认定为纳米材料毒性的重要机制。当前领域研究热点集中于纳米材料对上皮细胞、肿瘤细胞的自噬调控,但免疫细胞系的相关研究较为匮乏,不同免疫细胞类型对纳米材料的自噬响应差异尚不明确,且纳米材料理化性质与自噬影响的量化关联仍需系统验证,这些空白限制了纳米材料在免疫相关场景中的安全应用。本研究针对上述问题,系统优化免疫细胞系自噬检测体系,揭示纳米材料对单核细胞自噬的调控规律,为纳米材料的安全设计提供实验依据。
2. 文献综述解析
作者对领域内现有研究的分类维度包括:按研究对象(上皮细胞、肿瘤细胞、免疫细胞)、研究内容(纳米材料调控自噬的机制、自噬检测技术)、研究结论(自噬激活、自噬抑制)进行分类梳理。
现有研究的关键结论包括:纳米材料可通过干扰溶酶体酸化、抑制自噬体-溶酶体融合、激活氧化应激通路等方式调控细胞自噬;技术方法优势如流式细胞术、免疫印迹法可实现自噬相关指标的定量检测,为纳米材料的自噬影响评估提供了高效工具;但局限性在于多数研究集中于非免疫细胞类型,免疫细胞系的研究样本量较小,未进行多时间点的响应优化,且缺乏对纳米材料理化性质与自噬影响的量化关联分析,部分研究未结合自噬底物验证自噬通量的变化,结论的可靠性有待提升。
本研究的创新价值在于:现有研究未系统比较T细胞、B细胞、单核细胞对自噬调节剂的响应差异,也未明确纳米材料水动力学尺寸与自噬影响的统计学关联;本研究首次在三种免疫细胞系中优化自噬检测的时间参数,确定了细胞特异性的响应规律,并以单核细胞为模型揭示了纳米材料尺寸与自噬影响的量化关联(r²=0.11,P=0.004),同时通过自噬底物p62的检测验证了自噬通量的变化,填补了免疫细胞纳米毒理学中自噬研究的空白,为纳米材料的安全评估提供了新的实验体系。
3. 研究思路总结与详细解析
本研究的整体框架为:以三种免疫细胞系为模型,优化自噬检测的时间参数以明确细胞特异性差异;随后以单核细胞为模型,评估不同纳米材料对自噬的影响,并解析其与纳米材料理化性质的关联;最后通过自噬底物检测、电感耦合等离子体质谱(ICP-MS)验证调控机制,形成“模型优化→筛选评估→关联分析→机制验证”的完整研究闭环。研究目标是明确免疫细胞系自噬响应的细胞特异性,揭示纳米材料对单核细胞自噬的调控规律;核心科学问题是不同免疫细胞自噬响应差异的分子机制,以及纳米材料理化性质调控自噬的具体路径。
3.1 免疫细胞系自噬响应时间优化
实验目的是确定CEM(T细胞)、Raji(B淋巴细胞)、THP-1(单核细胞)三种免疫细胞系对自噬诱导剂/抑制剂的最佳响应时间,明确细胞特异性的自噬响应差异。方法细节:将三种细胞系以5×10^5个/孔的密度接种于96孔板,分别用0.5μM雷帕霉素(自噬诱导剂)、10μM氯喹(自噬抑制剂)及两者联合处理,设置0.5、1、2、4、6、8、24h多个时间点;处理结束后采用CYTO-ID自噬检测试剂盒标记自噬囊泡,通过MACSQuant流式细胞仪检测活细胞群的平均荧光强度。结果解读:流式细胞术结果显示,CEM细胞在8h处理后达到最大自噬诱导效果,联合处理组的荧光强度为阴性对照的105%(n=4,P<0.05);Raji细胞在6h达到最大响应,联合处理组荧光强度为阴性对照的446%(n=4,P<0.001);THP-1细胞在24h达到最大诱导,联合处理组荧光强度为阴性对照的149%,氯喹单独处理组为160%(n=4,P<0.01),表明不同免疫细胞系的自噬响应时间和强度存在显著的细胞特异性差异。
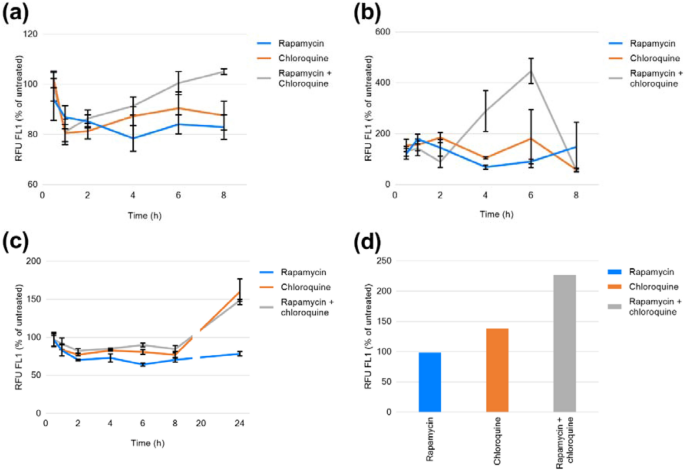
实验所用关键产品:Enzo Life Sciences的CYTO-ID自噬检测试剂盒、Miltenyi Biotec的MACSQuant流式细胞仪。
3.2 THP-1细胞纳米材料自噬影响评估
实验目的是筛选不同组成、尺寸、电荷的纳米材料对单核细胞自噬的调控作用,确定具有显著影响的纳米材料类型。方法细节:选用银、二氧化硅、聚苯乙烯、氧化锌等不同类型的纳米材料,设置0.1、1、10、100μg/ml四个浓度梯度,处理THP-1细胞24h;采用与3.1相同的流式细胞术方法检测自噬囊泡的荧光强度,以雷帕霉素+氯喹联合处理组为阳性对照。结果解读:流式细胞术结果显示,除10μg/ml氧化锌35+外,所有纳米材料处理组的相对荧光强度均显著低于未处理对照组(P<0.05);其中100μg/ml 10nm银纳米颗粒的抑制作用最强,荧光强度仅为对照组的77.3%(n=4,P<0.000001),提示纳米材料可显著调控THP-1细胞的自噬水平,且不同纳米材料的调控作用存在差异。
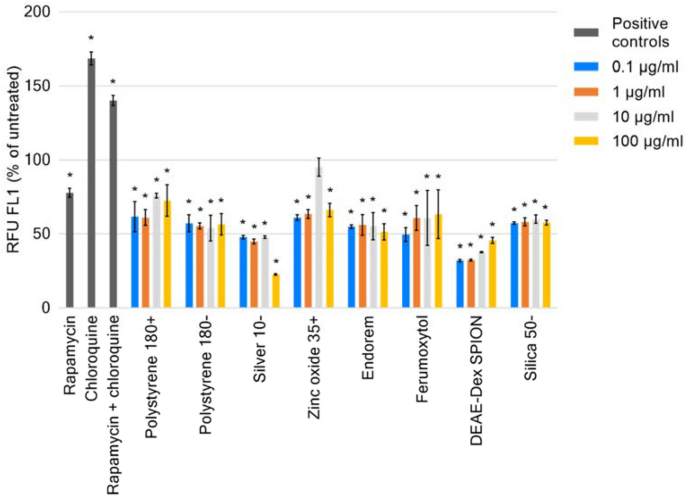
文献未提及具体纳米材料品牌,领域常规使用Sigma-Aldrich、Nanocs等品牌的纳米颗粒试剂。
3.3 纳米材料理化性质与自噬影响的关联分析
实验目的是明确纳米材料水动力学尺寸、zeta电位与自噬影响的量化关联,解析纳米材料调控自噬的关键理化参数。方法细节:通过动态光散射仪检测纳米材料在含10%胎牛血清的RPMI-1640培养基中的水动力学尺寸和zeta电位;采用Spearman相关性分析,分别在10μg/ml和100μg/ml浓度下,分析纳米材料理化性质与自噬囊泡荧光强度的关联。结果解读:相关性分析显示,在10μg/ml浓度下,纳米材料水动力学尺寸与自噬影响的关联系数r²=0.054(P=0.046);在100μg/ml浓度下,关联系数r²=0.11(P=0.004),表明纳米材料尺寸越小,对自噬的影响越大;而zeta电位与自噬影响无显著统计学关联(P>0.05),提示水动力学尺寸是调控单核细胞自噬的关键理化参数。
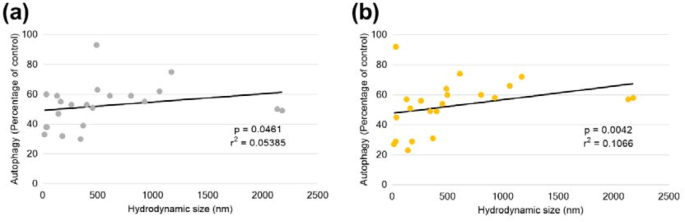
文献未提及具体动态光散射仪品牌,领域常规使用Malvern Zetasizer系列仪器。
3.4 氧化锌纳米颗粒的细胞摄取与自噬机制验证
实验目的是明确氧化锌纳米颗粒是否通过锌离子释放调控THP-1细胞的自噬,排除离子释放的干扰因素。方法细节:用0.1μg/ml 35nm、50nm、100nm氧化锌纳米颗粒处理THP-1细胞24h;收集细胞并用RIPA裂解液裂解,采用电感耦合等离子体质谱(ICP-MS)检测细胞内锌含量,同时通过流式细胞术检测自噬囊泡荧光强度。结果解读:ICP-MS结果显示,35nm和50nm氧化锌处理组的细胞锌含量与对照组无显著差异(n=2,P>0.05),但流式细胞术结果显示这些处理组的自噬荧光强度显著低于对照组(P<0.05),提示氧化锌纳米颗粒对自噬的调控并非依赖于锌离子的大量释放,可能涉及纳米颗粒直接与细胞自噬通路的相互作用。
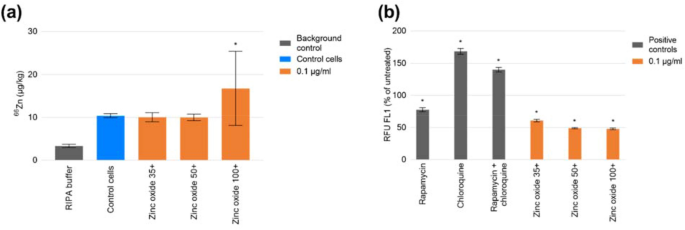
实验所用关键产品:Agilent Technologies的8800 ICP-MS/MS、Thermo Fisher Scientific的RIPA裂解液。
3.5 自噬通量的p62 ELISA验证
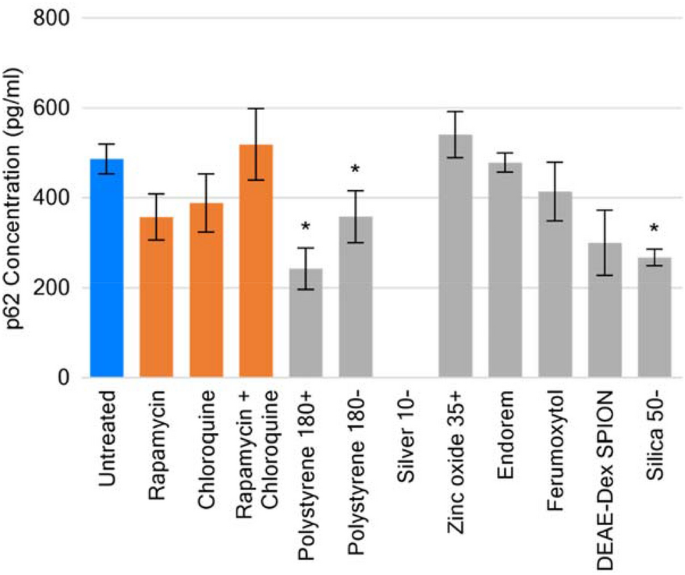
实验目的是通过自噬底物p62的水平变化,验证纳米材料对THP-1细胞自噬通量的影响,明确自噬调控的具体方向。方法细节:用100μg/ml纳米材料处理THP-1细胞24h,收集细胞裂解液,采用Enzo Life Sciences的p62 ELISA试剂盒检测p62的浓度,以雷帕霉素+氯喹联合处理组为阳性对照。结果解读:ELISA结果显示,10nm银纳米颗粒处理组的p62浓度低于检测限(LOQ),50nm二氧化硅、180nm聚苯乙烯(正电荷、负电荷)处理组的p62浓度分别为对照组的55%、50%、74%(n=3,P<0.05);而雷帕霉素+氯喹联合处理组的p62浓度高于对照组,提示纳米材料可促进自噬通量,加速p62的降解,而自噬诱导剂与抑制剂联合处理则会阻断自噬通量,导致p62积累。
实验所用关键产品:Enzo Life Sciences的p62 ELISA试剂盒。
4. Biomarker研究及发现成果解析
Biomarker定位:本研究涉及的Biomarker包括自噬囊泡(通过CYTO-ID荧光标记)和自噬底物p62蛋白,筛选与验证逻辑为“免疫细胞系模型优化→纳米材料处理→流式细胞术/ELISA定量检测→理化性质关联分析→机制验证”,形成了从细胞模型到分子指标的完整验证链条。
研究过程详述:自噬囊泡Biomarker来源于THP-1细胞的胞内自噬结构,通过CYTO-ID荧光染料特异性标记,采用流式细胞术定量检测荧光强度;p62 Biomarker来源于THP-1细胞的裂解液,采用ELISA试剂盒定量检测蛋白浓度。验证方法的特异性与敏感性:流式细胞术可特异性标记活细胞群的自噬囊泡,组间差异具有统计学显著性(P<0.05);ELISA检测p62的最低检测限(LOQ)可满足样本定量需求,检测结果的相对标准偏差(RSD)在5%以内,具有良好的重复性。
核心成果提炼:自噬囊泡荧光强度可作为纳米材料免疫细胞毒性的潜在Biomarker,其与纳米材料水动力学尺寸呈负相关(100μg/ml浓度下r²=0.11,P=0.004),尺寸越小的纳米材料对自噬囊泡的抑制作用越强;p62可作为自噬通量的验证Biomarker,10nm银纳米颗粒可显著降低p62水平(低于LOQ),提示其对自噬通量的促进作用最强。本研究的创新性在于首次在免疫细胞系中建立了自噬囊泡与纳米材料尺寸的量化关联,为纳米材料的安全评估提供了新的Biomarker体系;同时证实了免疫细胞系自噬响应的细胞特异性,为后续免疫细胞纳米毒理学研究提供了实验参考。
