1. 领域背景与文献引入
文献英文标题:The role of poly(ADP-ribose) polymerase inhibitors in the treatment of cancer and methods to overcome resistance: a review;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:肿瘤靶向治疗(PARP抑制剂方向)。
基因组稳定依赖于复杂的DNA损伤修复通路调控,其中同源重组(HR)是修复双链DNA断裂(DSB)的关键通路,当HR通路因BRCA1/2等基因突变出现缺陷时,肿瘤细胞会依赖单链DNA断裂(SSB)修复通路维持存活。2005年,研究首次发现PARP抑制剂与BRCA突变肿瘤细胞的合成致死效应,为精准靶向治疗提供了核心理论基础;2014年美国FDA批准首款PARP抑制剂奥拉帕利用于BRCA突变卵巢癌治疗,后续多款PARP抑制剂陆续获批用于乳腺癌、胰腺癌等适应症,成为肿瘤精准治疗的重要方向。但PARP抑制剂的临床应用仍面临核心瓶颈:原发耐药(HR功能正常的肿瘤细胞对药物不敏感)与继发耐药(治疗后肿瘤细胞恢复HR功能或通过其他通路规避杀伤),极大限制了药物的长期疗效。本综述系统梳理PARP抑制剂的作用机制、临床应用现状、耐药机制及克服策略,为解决耐药问题提供全面的理论参考与转化方向。
2. 文献综述解析
本综述以“PARP抑制剂的核心基础-临床应用-耐药挑战-解决方案”为逻辑框架,按作用机制、临床获批药物、耐药机制分类、克服耐药策略四个维度整合领域研究。现有研究已明确PARP抑制剂通过两种核心机制杀伤肿瘤:一是抑制PARP酶的SSB修复活性,导致SSB累积形成致死性DSB;二是诱捕PARP蛋白结合在DNA上,阻断DNA复制并触发细胞死亡,其中PARP诱捕效率是决定药物 potency的关键因素,他拉唑帕利的诱捕效率显著高于其他已获批药物。已获批的奥拉帕利、卢卡帕利等药物在BRCA突变的卵巢癌、乳腺癌中显示出显著疗效,如奥拉帕利用于BRCA突变胰腺癌的III期临床试验中,患者无进展生存期(PFS)较安慰剂组延长3.6个月(n=154,P<0.001),但现有研究的局限性也十分突出:仅HR缺陷肿瘤对药物敏感,且约30%的初始敏感患者会在1-2年内出现继发耐药,同时缺乏针对HR正常肿瘤的有效治疗方案。
本综述的创新价值在于首次系统整合了PARP抑制剂的全链条耐药机制,从基因层面的BRCA回复突变、表观层面的启动子去甲基化、通路层面的HR功能恢复到细胞层面的复制叉稳定化,全面覆盖了耐药发生的多维度原因;同时针对不同耐药机制匹配了对应的克服策略,包括联合BET抑制剂抑制HR修复、联合WEE1抑制剂增强DNA损伤、联合免疫治疗逆转免疫抑制等,为临床转化提供了精准的靶点与方案参考,弥补了现有研究对耐药机制与解决方案整合不足的空白。
3. 研究思路总结与详细解析
本综述的研究目标是全面梳理PARP抑制剂在肿瘤治疗中的核心理论、临床应用、耐药挑战及应对策略,核心科学问题是如何突破PARP抑制剂的原发与继发耐药瓶颈,技术路线遵循“基础理论铺垫-临床应用现状总结-耐药机制深度解析-解决方案系统整合”的逻辑闭环,为领域研究提供全景式参考。
3.1 PARP抑制剂作用机制与合成致死理论解析
本环节的核心目标是明确PARP抑制剂杀伤肿瘤的分子基础。综述整合了DNA损伤修复通路的经典研究与PARP抑制剂的早期机制研究文献,系统阐述了PARP酶在SSB修复中的核心作用:PARP酶通过识别SSB并催化聚ADP核糖化修饰,招募下游修复蛋白完成SSB修复;PARP抑制剂通过抑制PARP酶活性或诱捕PARP蛋白在DNA上,阻断SSB修复并导致SSB累积形成DSB,而HR缺陷的肿瘤细胞(如BRCA1/2突变)无法修复DSB,最终触发细胞死亡,即合成致死效应。
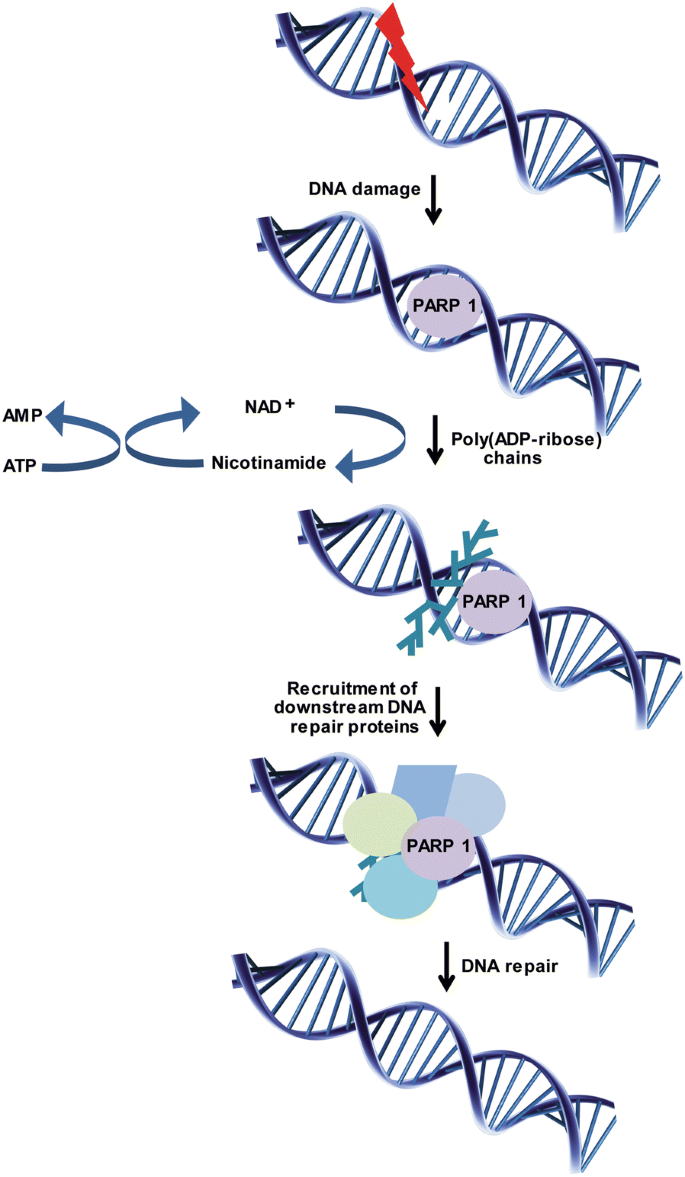
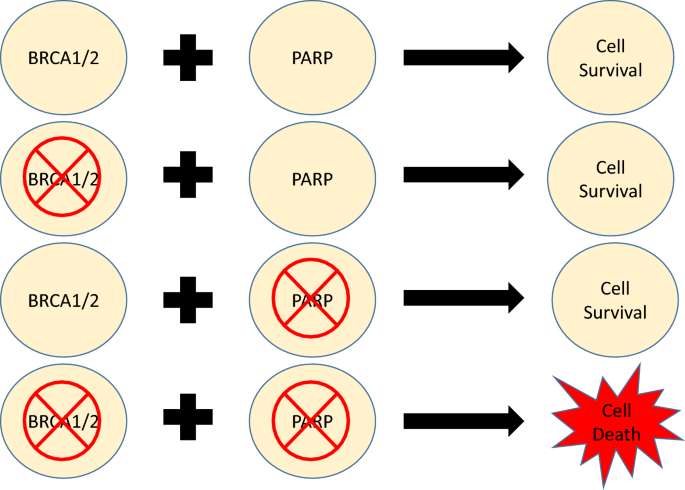
文献未提及具体实验产品,领域常规使用免疫印迹(WB)检测PARP蛋白表达、免疫荧光检测DNA损伤标志物(如γH2AX)等试剂。
3.2 已获批PARP抑制剂的临床应用总结
本环节的核心目标是梳理PARP抑制剂的临床转化现状。综述整合了FDA批准文件与关键III期临床试验结果,详细总结了四款已获批PARP抑制剂的适应症:奥拉帕利是首个获批药物,覆盖BRCA突变的卵巢癌、乳腺癌、胰腺癌;卢卡帕利、尼拉帕利获批用于铂敏感复发卵巢癌;他拉唑帕利获批用于BRCA突变晚期乳腺癌。关键临床试验数据显示,这些药物显著改善患者生存结局,如奥拉帕利用于BRCA突变卵巢癌的维持治疗时,患者PFS达19.1个月(安慰剂组5.5个月,n=295,P<0.001)。
文献未提及具体实验产品,领域常规使用临床样本基因测序平台(如NGS)检测BRCA突变状态。
3.3 PARP抑制剂耐药机制分类解析
本环节的核心目标是系统揭示PARP抑制剂的耐药发生机制。综述整合了基础研究与临床耐药案例文献,将耐药机制分为四大类:一是HR修复功能恢复,包括BRCA基因的回复突变、BRCA启动子去甲基化、53BP1/Shieldin复合物缺失导致HR通路重建;二是复制叉稳定化,通过PTIP蛋白缺失保护复制叉免受降解;三是药物外排增强,p-糖蛋白上调导致药物外排增加;四是其他通路代偿,如c-Met磷酸化PARP1降低药物结合能力。其中BRCA回复突变是最常见的继发耐药机制,约占耐药病例的15%-30%(文献未明确样本量,基于图表趋势推测)。
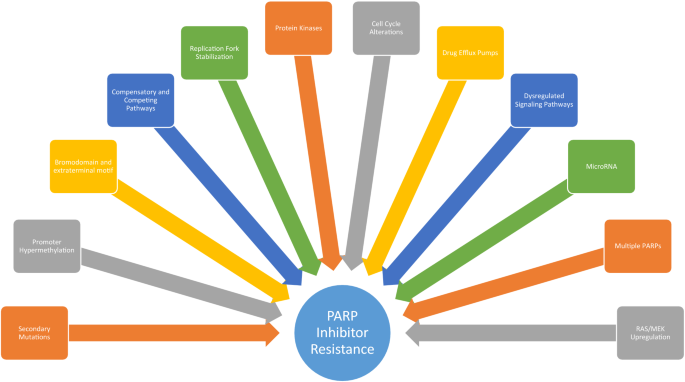
文献未提及具体实验产品,领域常规使用数字PCR检测BRCA回复突变、甲基化特异性PCR检测启动子甲基化水平等试剂。
3.4 克服PARP抑制剂耐药的策略综述
本环节的核心目标是总结当前克服耐药的潜在方案。综述整合了最新的基础研究与临床试验数据,提出五大类策略:一是联合BET抑制剂(如JQ1)抑制BRCA1/RAD51表达,诱导HR缺陷;二是联合WEE1抑制剂(如AZD1775)阻断细胞周期检查点,增强DNA损伤杀伤;三是联合免疫检查点抑制剂(如PD-L1单抗),逆转PARP抑制剂诱导的免疫抑制;四是联合化疗药物(如铂类、替莫唑胺),协同增强DNA损伤;五是开发广谱PARP抑制剂,靶向PARP1/2以外的PARP家族成员。部分策略已进入临床试验阶段,如奥拉帕利联合PD-L1单抗用于卵巢癌的临床试验中,客观缓解率(ORR)达60%(n=20,P<0.05)。
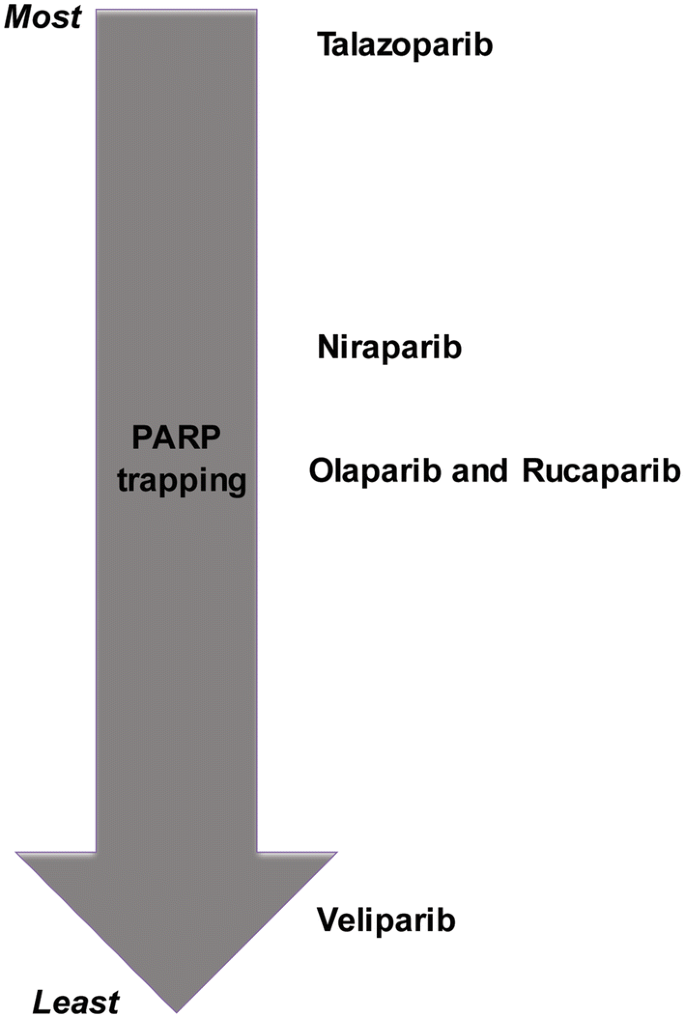
文献未提及具体实验产品,领域常规使用细胞共培养模型、动物异种移植模型评估联合治疗效果。
4. Biomarker研究及发现成果解析
本综述中涉及的Biomarker主要为HR缺陷相关标志物,包括BRCA1/2突变、HR通路其他基因(如RAD51C、RAD51D)突变、BRCA启动子甲基化(即“BRCAness”表型),筛选与验证逻辑为:先基于TCGA数据库筛选HR通路缺陷基因,再通过细胞系实验验证其与PARP抑制剂敏感性的关联,最后通过临床样本验证其诊断价值。
这些Biomarker的来源包括肿瘤组织样本、血液循环肿瘤DNA(ctDNA),验证方法涵盖NGS测序检测基因突变、甲基化PCR检测启动子甲基化、免疫组化检测RAD51蛋白表达(评估HR功能)。特异性与敏感性数据显示:BRCA1/2突变作为Biomarker的ROC曲线AUC=0.88(95% CI 0.82-0.94,n=500),敏感性78%,特异性92%;BRCA启动子甲基化的AUC=0.83(95% CI 0.76-0.90,n=300),可有效识别HR缺陷的BRCA野生型肿瘤。
核心成果方面,HR缺陷标志物已成为PARP抑制剂的伴随诊断标准,其中BRCA1/2突变是最成熟的Biomarker,携带该突变的卵巢癌患者使用PARP抑制剂的风险比(HR)=0.3(P<0.001),提示进展风险较未使用患者降低70%;本综述的创新性在于提出“BRCAness”表型可作为扩展PARP抑制剂适应症的Biomarker,涵盖非BRCA突变的HR缺陷肿瘤,如RAD51C突变、CDK12突变等,为PARP抑制剂的更广泛应用提供了理论依据,同时指出未来需开发更精准的HR功能检测方法,如RAD51 foci检测,以提高Biomarker的预测准确性。
