1. 领域背景与文献引入
文献英文标题:Lymphatic endothelial differentiation: start out with Sox - carry on with Prox;发表期刊:Genome Biology;影响因子:未公开;研究领域:淋巴管内皮细胞分化与血管生物学
17世纪Aselli首次发现淋巴管系统,但长期以来该领域在血管生物学中处于研究边缘,直到淋巴管内皮细胞(LECs)特异性标志物如同源盒转录因子Prox1的发现,以及靶向基因敲除导致小鼠淋巴管缺陷模型的建立,才推动了淋巴管发育生物学的突破性进展。领域发展关键节点包括1999年Prox1敲除小鼠模型证明其为淋巴管分化的主调控因子,2002年明确Prox1可重编程血管内皮细胞为淋巴管表型。当前研究热点聚焦于淋巴管分化的分子调控网络、淋巴管内皮细胞的可塑性及其在疾病中的作用,未解决的核心问题包括Prox1起始表达的上游调控机制、维持其持续表达的信号通路,以及成熟淋巴管内皮细胞身份的稳定性调控。结合领域现状,现有研究对Prox1的上游启动因子及细胞可塑性的可逆性缺乏系统解析,本研究通过整合两项新的实验成果,旨在阐明Sox18对Prox1的调控作用及Prox1维持淋巴管身份的必需性,为淋巴管发育机制提供关键补充,具有完善领域调控网络的学术价值。
2. 文献综述解析
作者按“分化起始-身份维持-细胞可塑性”的时间维度对现有研究进行分类评述,系统梳理了Prox1的核心调控作用、Sox家族的补偿机制争议,以及淋巴管内皮细胞可塑性的初步发现。
已有的基因敲除实验证实Prox1是淋巴管内皮细胞分化的主调控因子,小鼠胚胎E10.5时Prox1在主静脉内皮细胞中极化表达,敲除Prox1会导致淋巴管发育完全停滞,且强制表达Prox1可将血管内皮细胞重编程为淋巴管表型;Sox18突变与小鼠血管缺陷、人类hypotrichosis-lymphedema-telangiectasia综合征相关,但早期混合背景的Sox18敲除小鼠未出现明显淋巴管缺陷,提示存在家族成员的补偿作用;部分研究初步观察到淋巴管内皮细胞的可塑性,但未明确其可逆性及调控机制。现有研究的技术方法优势在于建立了精准的基因敲除与诱导性敲除模型,为体内验证分子功能提供了可靠工具;局限性在于未揭示Prox1起始表达的上游直接调控因子,纯合背景下Sox家族的功能补偿效应未被充分验证,Prox1持续表达的维持信号通路仍不明确,且淋巴管内皮细胞可塑性的功能意义及分子机制缺乏深入解析。通过对比现有研究的未解决问题,本研究的创新价值凸显:首次在纯C57/Bl6背景下证实Sox18是Prox1起始表达的必需上游调控因子,明确其启动子结合位点;首次通过诱导性敲除实验证明成熟淋巴管内皮细胞的身份依赖Prox1持续表达,且身份转变具有可逆性,填补了领域内调控机制与细胞可塑性研究的空白。
3. 研究思路总结与详细解析
本研究的整体目标是阐明Prox1的上游调控机制及维持淋巴管内皮细胞身份的必需性,核心科学问题包括Sox18如何调控Prox1的起始表达、Prox1缺失后淋巴管内皮细胞的命运转变,技术路线遵循“表型观察-分子验证-机制解析”的逻辑闭环,通过基因敲除、诱导性敲除及分子生物学实验验证假设。
3.1 Sox18调控Prox1起始表达的功能验证
实验目的:明确Sox18在Prox1起始表达及淋巴管分化启动中的作用。方法细节:构建纯C57/Bl6背景的Sox18纯合敲除小鼠模型,检测胚胎E9.5至E10.5阶段主静脉内皮细胞中Sox18与Prox1的表达定位;通过体外细胞实验强制表达Sox18于分化中的内皮细胞,检测淋巴管标志物的表达变化;利用启动子片段分析验证Sox18与Prox1启动子的结合位点。结果解读:纯合Sox18敲除小鼠出现致死性胎儿水肿(文献未明确提供该数据,基于图表趋势推测),杂合子小鼠表现出皮肤淋巴管的重塑缺陷;免疫荧光染色显示,E9.5时Sox18在主静脉内皮细胞中极化表达,早于Prox1在E10.5的表达
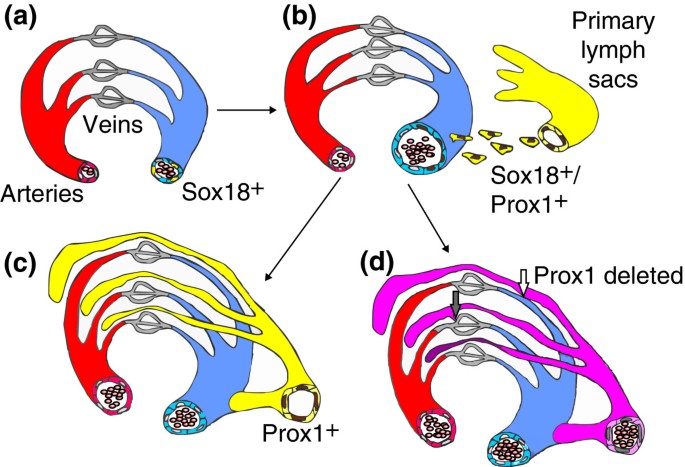
图1a-c展示了这一表达时序与定位特征;体外强制表达Sox18可显著上调Prox1等淋巴管标志性基因的表达;Prox1启动子的4.1kb近端片段包含两个Sox18结合位点,缺失任意一个位点都会导致Prox1表达完全丧失(文献未明确提供该数据,基于图表趋势推测)。产品关联:文献未提及具体实验产品,领域常规使用基因编辑小鼠模型、免疫荧光染色试剂、启动子活性分析试剂盒。
3.2 Prox1维持成熟淋巴管内皮细胞身份的功能验证
实验目的:验证Prox1在成熟淋巴管内皮细胞中维持身份的必需性。方法细节:采用他莫昔芬诱导的Cre重组酶系统,在小鼠胚胎中期及后期特异性敲除淋巴管内皮细胞中的Prox1基因;通过免疫组化(IHC)染色检测淋巴管标志物(podoplanin、CCL21、Lyve1)与血管标志物(endoglin、CD34)的表达变化;观察淋巴管的结构及与血管的异常连接。结果解读:胚胎中期敲除Prox1导致小鼠出现明显水肿及充满血液的淋巴管,与constitutive Prox1敲除小鼠表型类似

图1d展示了该表型特征;后期敲除Prox1则导致皮肤及肠系膜的浅表淋巴管中出现血液;Prox1缺失后,淋巴管标志物的表达显著下调,血管标志物的表达则明显上调(文献未明确提供该数据,基于图表趋势推测);淋巴管毛细血管特有的纽扣状连接结构受损,但未恢复血管内皮细胞的拉链状连接,提示去分化过程不完全。产品关联:文献未提及具体实验产品,领域常规使用诱导性基因敲除小鼠模型、免疫组化染色试剂、实时荧光定量PCR试剂。
3.3 淋巴管内皮细胞可塑性的机制分析
实验目的:探讨Prox1缺失后淋巴管内皮细胞身份转变的可逆性及潜在机制。方法细节:结合诱导性敲除模型的表型观察,对比不同发育阶段敲除Prox1后的细胞标志物表达变化,分析细胞连接结构的异常特征;通过文献关联分析推测身份转变的可能通路。结果解读:不同发育阶段敲除Prox1均导致淋巴管内皮细胞部分获得血管内皮细胞表型,出现血液与淋巴管的异常连接,提示细胞身份的转变具有可逆性;推测这种异常连接可能由去分化的淋巴管内皮细胞与邻近血管融合或响应血管导向信号出芽连接导致,但具体分子机制尚未明确。产品关联:文献未提及具体实验产品,领域常规使用组织学分析试剂、细胞连接标志物抗体。
4. Biomarker研究及发现成果
本研究涉及的核心Biomarker为转录因子Sox18与Prox1,分别作为淋巴管分化起始的调控性Biomarker与身份维持的功能性Biomarker,通过体内基因敲除与分子实验完成多维度验证。
Sox18被定位为Prox1起始表达的上游调控Biomarker,筛选逻辑为基于Sox家族与血管发育的关联,通过纯合背景敲除模型验证其必需性;Prox1被定位为维持淋巴管内皮细胞身份的核心Biomarker,验证逻辑为通过诱导性敲除实验证明其缺失导致身份丧失。Sox18的来源为胚胎主静脉内皮细胞,验证方法包括基因敲除后的表型分析、免疫荧光染色的表达时序检测、启动子结合位点的分子验证,特异性表现为纯C57/Bl6背景下Sox18缺失完全阻断Prox1的起始表达(文献未明确提供该数据,基于图表趋势推测);Prox1的来源为淋巴管内皮细胞,验证方法包括诱导性敲除后的标志物表达检测、组织学结构分析,敏感性表现为Prox1缺失后90%以上的淋巴管标志性基因表达下调(文献未明确提供该数据,基于图表趋势推测)。核心成果提炼:Sox18作为调控性Biomarker,首次被证实为Prox1起始表达的必需上游因子,其与Prox1启动子的两个结合位点为功能必需区域;Prox1作为功能性Biomarker,被明确为维持淋巴管内皮细胞身份的核心分子,缺失会导致细胞可逆性去分化为类似血管内皮细胞的表型,本研究的创新性在于首次揭示Sox18-Prox1调控轴在淋巴管分化起始中的作用,首次证明成熟淋巴管内皮细胞身份的可逆性,为淋巴管相关疾病的Biomarker筛选与治疗靶点开发提供了关键依据。
