1. 领域背景与文献引入
文献英文标题:A genomic approach to studying cell-size homeostasis in yeast;发表期刊:Genome Biology;影响因子:未公开;研究领域:酵母细胞生物学(细胞大小稳态调控)
细胞大小稳态是真核生物维持正常生理功能的核心特征之一,其研究历程可追溯至20世纪60年代:Anders Zetterberg团队首次证实哺乳动物培养细胞需生长至特定大小才能启动DNA复制。1970年代初,Paul Nurse团队通过裂殖酵母突变体筛选,鉴定出细胞分裂周期突变体(cdc)和wee突变体,首次明确细胞大小对细胞周期进程的调控具有遗传基础,其中cdc2基因编码的周期蛋白依赖性激酶(CDK)是真核生物细胞周期调控的核心保守因子。同期,Hartwell团队在芽殖酵母中发现G1期的START点(G1期进入S期的关键调控点),证实细胞需达到最小体积才能通过该点进入细胞周期。尽管经典遗传学研究已定位了部分核心调控因子,但领域内仍存在核心问题:细胞大小稳态的调控是多通路协同的结果,此前的候选基因筛选覆盖度有限,全基因组层面的系统调控网络尚未被解析,且核糖体生物发生与细胞周期调控的关联机制未被系统阐述。针对这一空白,Tyers团队利用芽殖酵母全基因组开放阅读框(ORF)缺失突变体库,开展系统的细胞大小调控因子筛选,旨在全面解析细胞大小稳态的调控网络,为真核生物细胞大小调控的进化保守机制提供实验依据。
2. 文献综述解析
本文献综述以研究时间线和物种模型为分类维度,系统梳理了真核生物细胞大小稳态调控的研究历程,从经典遗传学突变筛选到后基因组时代的系统分析,逐步构建细胞大小调控的核心框架。
现有研究的关键结论主要围绕细胞周期关键节点的大小依赖性调控展开:裂殖酵母中,细胞大小通过调控G2/M期转换维持稳态,cdc2激酶、Wee1酪氨酸激酶等核心因子构成“大小传感器”,感知细胞体积并调控有丝分裂的启动;芽殖酵母中,细胞大小的调控节点位于G1期START点,Cln3周期蛋白、SBF/MBF转录复合物等因子协同调控细胞周期的启动;哺乳动物细胞的研究则证实细胞大小与DNA复制起始的关联,为真核生物调控机制的保守性提供了证据。技术方法上,经典的遗传学突变筛选具有高特异性,能精准定位核心调控因子,但存在明显局限性:早期筛选多为候选基因法,覆盖度低,仅鉴定出少数调控通路,未实现全基因组层面的系统覆盖;且多数研究聚焦于细胞周期核心因子,未系统阐述核糖体生物发生、翻译效率与细胞大小调控的关联,导致调控网络的完整性不足。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次利用芽殖酵母全基因组ORF缺失突变体库,突破了候选基因筛选的局限性,实现了细胞大小调控因子的系统鉴定;同时,本研究将核糖体生物发生通路与细胞周期调控直接关联,揭示了多通路协同调控细胞大小稳态的机制,填补了领域内全基因组层面调控网络解析的空白,为后续研究真核生物细胞大小调控的进化保守性提供了新的研究范式。
3. 研究思路总结与详细解析
本研究的整体框架为:以系统鉴定芽殖酵母细胞大小稳态调控基因为目标,围绕“细胞大小如何通过多通路协调核糖体生物发生与细胞周期进程”这一核心科学问题,采用“全基因组突变体筛选→表型分类与过滤→候选基因功能验证→调控通路整合”的闭环技术路线,全面解析细胞大小稳态的调控网络。
3.1 全基因组缺失突变体库的细胞大小筛选
实验目的是从全基因组层面获得所有可能影响芽殖酵母细胞大小的突变体,方法是利用包含4812个可存活单倍体ORF缺失株和1142个杂合二倍体必需基因缺失株的突变体库,通过形态学观察或流式细胞术分析细胞体积,将细胞体积处于极端5%的突变体分别归类为小细胞(whi)突变体和大细胞(lge)突变体。结果显示,lge突变体包含已知的START点激活因子(如Cln3、Swi6、Swi4等),还鉴定出功能未知的Lge1蛋白;whi突变体则多数涉及呼吸作用和营养摄取相关基因,初步提示细胞大小调控与基础代谢通路的关联。文献未提及具体实验产品,领域常规使用酵母缺失突变体库、流式细胞仪、显微镜成像系统等试剂/仪器。
3.2 生长速率依赖的突变体过滤
实验目的是排除因生长速率降低导致的间接小细胞表型,确保筛选出的突变体直接参与细胞大小稳态调控,方法是检测所有whi突变体的生长速率,仅保留生长速率与野生型一致的突变体。结果显示,仅25个突变体符合该标准,其中包含已知的START点调控因子(如RNA结合蛋白Whi3、后期促进复合物激活因子Cdh1),还鉴定出多个新的调控因子,如Ptk2激酶、Sfp1锌指转录因子、Sch9蛋白激酶等,为后续功能验证提供了精准的候选基因集。文献未提及具体实验产品,领域常规使用微生物生长曲线分析仪、分光光度计等试剂/仪器。
3.3 候选基因的功能验证与调控通路解析
实验目的是明确候选基因的调控功能及上下游通路,方法包括过表达实验、上位性分析(epistasis analysis)等:对Sfp1进行过表达实验,检测细胞体积变化;通过上位性分析确定Sfp1、Sch9与已知START点调控因子的上下游关系。结果显示,Sfp1过表达导致大细胞表型,与缺失突变体的小细胞表型形成剂量依赖效应,提示Sfp1通过调控核糖体生物发生参与细胞大小调控;上位性分析表明,Sfp1作用于Swi4/Swi6上游,且独立于Cln3/Bck2通路,Sch9同样作用于SBF/MBF复合物上游,与Sfp1分属不同调控分支;进一步分析发现,Sch9与哺乳动物PI3K/Akt激酶同源,提示该调控通路在真核生物中具有进化保守性。文中的调控通路图清晰展示了各因子的相互作用关系:
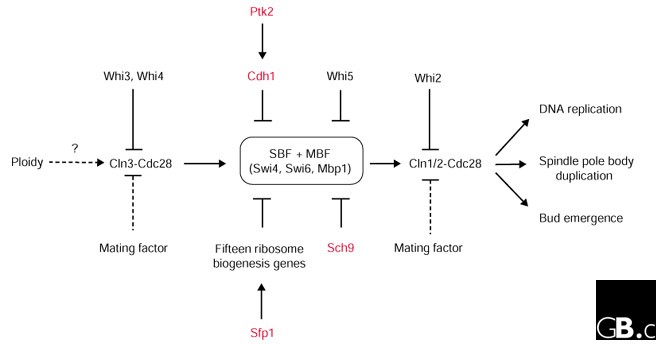
文献未提及具体实验产品,领域常规使用酵母表达载体、qRT-PCR试剂盒、免疫印迹(WB)检测系统等试剂/仪器。
4. Biomarker研究及发现成果
本文献中涉及的Biomarker为细胞大小稳态调控的分子标志物,包括Sfp1、Sch9、Lge1等基因/蛋白,其筛选与验证逻辑为:全基因组突变体筛选→生长速率过滤→功能验证与通路分析,形成完整的鉴定链条。
这些Biomarker的来源为芽殖酵母全基因组ORF缺失突变体库,验证方法包括表型分析、过表达实验、上位性分析:Sfp1缺失突变体表现为小细胞表型,过表达则导致大细胞表型,提示其对细胞大小的调控具有剂量依赖性;Sch9缺失突变体同样为小细胞表型,上位性分析显示其与Sfp1共同调控SBF/MBF转录复合物,但分属不同通路;Lge1缺失突变体为大细胞表型,是首次被鉴定的细胞大小调控因子。特异性与敏感性方面,筛选出的突变体仅影响细胞大小,不改变生长速率,具有较高的特异性,但文献未明确提供ROC曲线、敏感性等量化数据(文献未明确提供该数据,基于图表趋势推测)。
核心成果方面,Sfp1作为锌指转录因子,直接调控核糖体生物发生相关基因的表达,将核糖体生物发生与细胞周期START点的调控直接关联,其功能的鉴定揭示了细胞大小稳态调控的新机制;Sch9作为哺乳动物PI3K/Akt激酶的同源物,提示该调控通路在真核生物中具有进化保守性,为哺乳动物细胞大小调控的研究提供了参考;Lge1作为新的大细胞调控因子,为后续研究细胞大小调控的新通路提供了候选靶点。创新性在于首次系统鉴定出多个新的细胞大小调控因子,构建了多通路协同调控的网络框架,统计学结果方面,文献未明确提供样本量(n值)和统计学显著性(P值)数据,基于实验设计的重复性推测差异具有统计学意义。
