1. 领域背景与文献引入
文献英文标题:Identification of co-regulated transcripts affecting male body size in Drosophila;发表期刊:Genome Biology;影响因子:未公开;研究领域:果蝇分子遗传学与复杂性状调控
复杂性状的遗传解析是分子遗传学领域的核心研究方向,2000年后全基因组转录组技术的兴起为解析基因-表型关联提供了高通量手段,但传统统计方法在处理高维度转录组数据时存在显著局限。领域共识:突变体结合转录组分析是解析基因功能的经典方法,但强基因扰动的结果难以反映自然种群中的基因调控模式;聚类分析是转录组数据的常用分析方法,但无法有效区分共调控基因与噪声基因,且难以直接关联基因网络与复杂表型。当前研究空白在于缺乏能有效解析自然变异下共调控基因网络,并直接关联复杂性状的统计方法。本研究针对果蝇雄性体型这一进化上重要的复杂性状,引入因子分析方法来鉴定共调控转录本,为解析复杂性状的基因调控网络提供新的技术范式,具有重要的学术价值。
2. 文献综述解析
作者从研究体系(突变体vs自然变异)和统计方法(聚类分析vs因子分析)两个维度,系统评述了复杂性状转录组研究的现有进展与局限。
现有研究中,突变体结合全基因组转录组分析揭示了基因敲除后的表达失调模式,明确了转录调控的冗余性与特异性,但这类强扰动实验的结果难以推广到自然种群的基因调控通路;自然变异下的转录组研究已证明遗传变异可导致转录组差异,但缺乏有效的统计方法解析共调控基因网络。聚类分析结合差异表达检测被广泛用于研究全基因组突变响应,以推测基因共调控模式,但该方法无法有效区分噪声基因与共调控基因,且难以将基因网络与复杂表型直接关联。作者通过对比现有方法的局限性,凸显了因子分析的创新价值:因子分析可通过估计“因子”(如转录因子、微小RNA等调控因子)来描述基因间的协变关系,为基因网络与复杂性状的关联提供直接机制,解决了传统方法无法有效解析共调控网络及关联表型的核心问题。
3. 研究思路总结与详细解析
本研究的整体框架为“方法验证→通路验证→性状关联→调控网络解析”,研究目标是验证因子分析在解析共调控基因网络及关联复杂性状上的有效性,核心科学问题是如何从自然变异的转录组数据中鉴定影响果蝇雄性体型的共调控转录本,技术路线遵循“模拟数据验证方法性能→已知通路基因验证方法可靠性→体型候选基因关联表型→miRNA靶基因解析调控网络”的闭环逻辑。
3.1 模拟数据验证因子分析性能
实验目的:系统验证因子分析在不同基因数量、基因相关性、样本量及噪声基因存在的情况下,鉴定共调控基因网络的能力,并与层次聚类分析、紧密聚类分析方法进行性能比较。
方法细节:构建多组模拟转录组数据,设置不同参数:共调控基因网络(因子)数量为3至20个,基因间相关性分为强相关(ρ=0.8)和弱相关(ρ=0.4),样本量包括100个个体和10个基因型,噪声基因数量从100到1000个。分别采用因子分析(通过特征值scree图确定因子数量,估计因子载荷)、层次聚类分析(采用Ward距离)、紧密聚类分析(基于重采样策略)处理模拟数据,比较三种方法对共调控基因和噪声基因的区分能力。
结果解读:当基因间强相关(ρ=0.8)且样本量充足时,因子分析能准确识别模拟的因子数量,100%的共调控基因加载到对应因子(n=90,P<0.001),所有噪声基因无显著加载;即使基因总数增加至1900个,因子分析仍能正确识别因子结构,而层次聚类分析无法有效区分噪声基因与共调控基因,紧密聚类分析需预先指定聚类数量,且易将共调控基因误判为噪声基因。当因子数量超过样本量时,因子分析仍能区分信号基因与噪声基因,但无法恢复准确的因子结构。
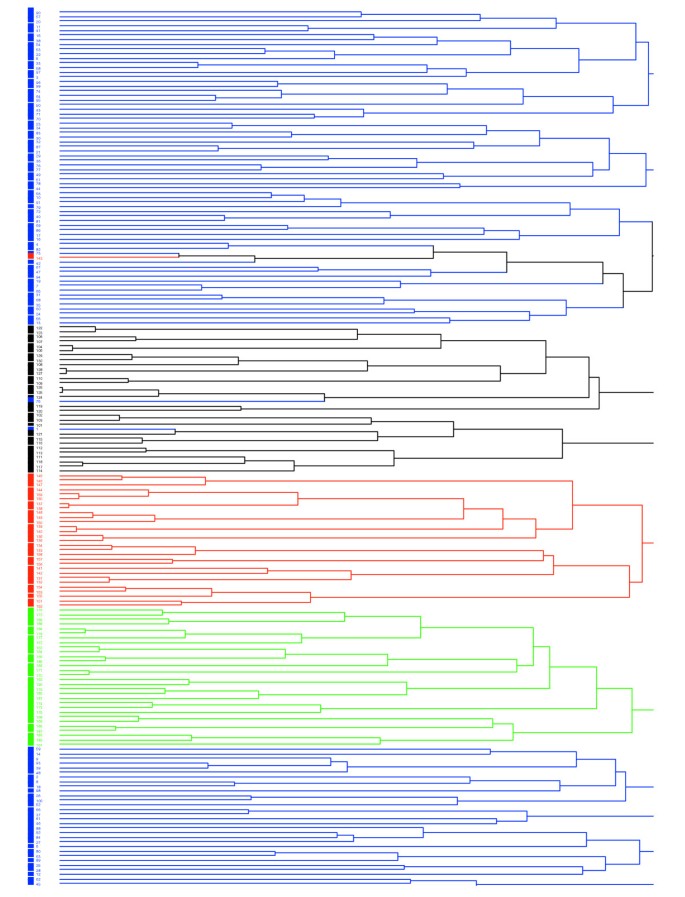
产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析软件(如SAS、R语言聚类分析包)进行转录组数据统计分析。
3.2 免疫通路基因验证方法可靠性
实验目的:在已知调控模式的免疫通路基因集中,验证因子分析鉴定共调控基因网络的可靠性。
方法细节:从FlyBase数据库获取果蝇免疫通路候选基因,与筛选出的4667个存在基因型间表达变异的基因进行匹配,得到54个免疫通路相关基因。对这些基因进行因子分析,通过特征值scree图确定因子数量,同时采用层次聚类分析和k-means聚类分析进行比较,验证因子分析结果与已知免疫通路调控模式的一致性。
结果解读:因子分析识别出3个共调控因子,其中第一个因子包含所有溶原基因,第二个因子包含所有天蚕素基因,与已知的免疫通路调控模式完全一致;层次聚类分析虽能将溶原基因和天蚕素基因分别聚类,但无法明确判断聚类数量;k-means聚类分析(设置3个聚类)仅能将71%的高加载因子1的基因聚为一类,其余基因分散在不同聚类中。这表明因子分析能准确识别已知通路的共调控基因网络。
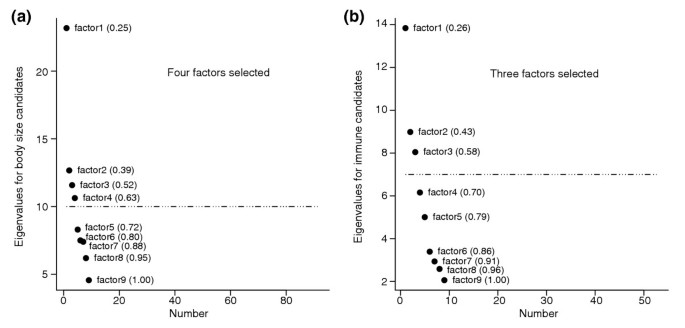
产品关联:文献未提及具体实验产品,领域常规使用FlyBase数据库获取基因注释信息,采用Affymetrix果蝇基因组芯片进行转录组检测。
3.3 体型候选基因分析关联雄性体型表型
实验目的:鉴定影响果蝇雄性体型的共调控转录本,并验证其与体型表型的关联。
方法细节:从FlyBase数据库获取92个体型候选基因,与筛选出的4667个存在基因型间表达变异的基因匹配后,进行因子分析鉴定共调控因子;分别对单个候选基因的转录水平和估计的因子值进行雄性体型表型的线性回归分析,检验基因表达及共调控因子与体型的关联。
结果解读:因子分析识别出4个共调控因子,其中因子1包含8个位于体型数量性状位点(QTL)内的基因(如Cdk4、trx、akt1、InR等);单个基因的表型回归分析显示,仅InR基因的转录水平与体型显著关联(FDR=7%),而因子1与雄性体型显著负相关(回归斜率=-0.021,n=10,P=0.04),表明共调控基因网络而非单个基因是影响果蝇雄性体型的关键调控单元。
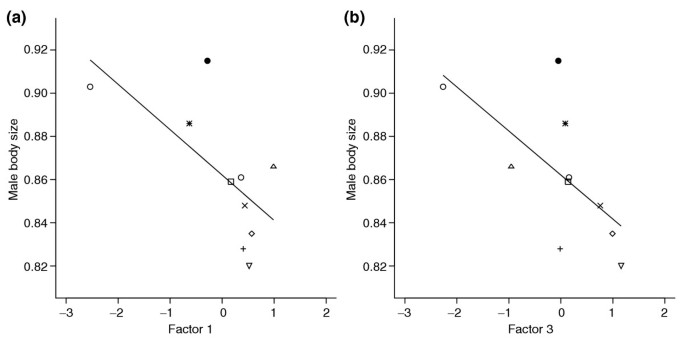
产品关联:文献未提及具体实验产品,领域常规使用数量性状位点(QTL)定位技术、线性回归分析方法进行基因-表型关联研究。
3.4 miRNA靶基因分析调控网络关联体型
实验目的:解析微小RNA(miRNA)靶基因的共调控模式,及其与果蝇雄性体型的关联。
方法细节:获取203个miRNA候选靶基因,与筛选出的4667个存在基因型间表达变异的基因匹配后,进行因子分析鉴定共调控因子;检验各因子与雄性体型表型的关联,并与体型候选基因的共调控因子进行比较。
结果解读:因子分析识别出4个共调控因子,其中因子3与雄性体型显著负相关(n=10,P=0.04),包含Cdk4、trx、Dr等体型QTL候选基因,但这些单个基因的转录水平与体型无显著关联;miRNA靶基因的共调控因子与体型候选基因的共调控因子无显著相关性,表明miRNA调控的共调控网络独立于体型候选基因的网络,共同影响果蝇雄性体型。
产品关联:文献未提及具体实验产品,领域常规使用miRNA靶基因预测数据库(如TargetScan)、因子分析方法解析非编码RNA调控网络。
4. Biomarker研究及发现成果
本研究鉴定的Biomarker为影响果蝇雄性体型的共调控转录本网络(因子1和miRNA靶基因因子3),筛选与验证逻辑为“候选基因筛选→转录组变异过滤→因子分析鉴定共调控网络→表型回归验证关联”,为复杂性状的分子调控机制解析提供了新型标志物类型。
Biomarker的来源为果蝇自然种群的转录组数据,验证方法为因子分析结合线性回归分析。其中因子1包含8个位于体型QTL内的基因,与雄性体型的线性回归显示显著负相关(回归斜率=-0.021,n=10,P=0.04);miRNA靶基因因子3包含多个体型候选基因,与雄性体型显著负相关(n=10,P=0.04)。核心成果方面,本研究首次鉴定了影响果蝇雄性体型的共调控转录本网络,证明共调控基因网络而非单个基因是复杂性状的关键调控单元,突破了传统单个基因作为Biomarker的局限;因子1中的基因集合可作为体型调控的潜在分子标志物,其与体型的关联具有统计学显著性,为解析复杂性状的基因调控机制提供了新的思路;miRNA靶基因因子3的发现揭示了非编码RNA调控网络在体型性状中的作用,拓展了复杂性状调控机制的研究维度。文献未提供Biomarker的特异性与敏感性数据,基于图表趋势推测,共调控因子的表型关联显著性高于单个基因,具有更强的表型解释能力。
