1. 领域背景与文献引入
文献英文标题:Remote ischemic preconditioning protects against spinal cord ischemia–reperfusion injury in mice by activating NMDAR/AMPK/PGC-1α/SIRT3 signaling;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:脊髓缺血再灌注损伤(SCIRI)的神经保护机制研究。
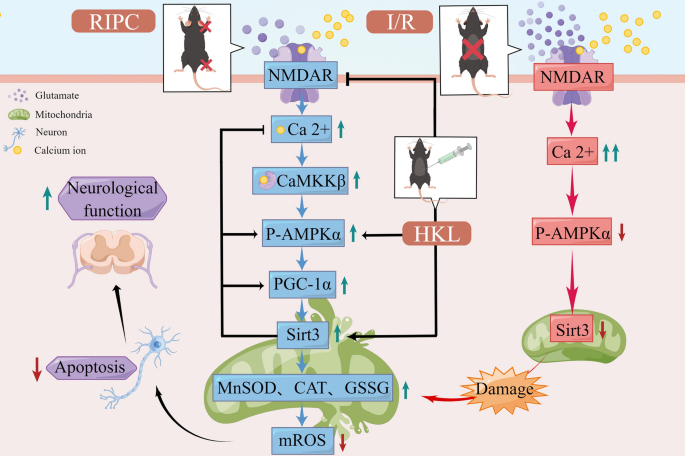
脊髓缺血再灌注损伤是脊柱和胸主动脉术后截瘫的主要诱因,具有高发病率和严重的生活质量影响,尽管现有手术技术已降低术后截瘫风险,但SCIRI的预防与治疗仍是临床亟待解决的核心难题。远程缺血预处理(RIPC)通过对远处组织施加亚致死缺血-再灌注循环,激活器官间天然保护机制,已在心脏、脑、肾等器官的缺血损伤保护中被证实有效,但在SCIRI中的作用机制,尤其是关键调控蛋白及上游信号通路尚未完全阐明。SIRT3作为定位于线粒体的经典去乙酰化酶,通过调控锰超氧化物歧化酶(MnSOD)、过氧化氢酶(CAT)等抗氧化酶活性维持线粒体稳态,在多种器官缺血再灌注损伤中发挥保护作用,但RIPC是否通过SIRT3介导SCIRI的神经保护效应,以及上游调控通路仍属研究空白。本研究旨在明确延迟性RIPC对小鼠SCIRI的保护作用,验证SIRT3的核心介导地位,并解析上游NMDAR/AMPK/PGC-1α信号通路的调控机制,为SCIRI的临床治疗提供新靶点与策略。
2. 文献综述解析
作者对领域内研究的分类维度主要分为三个方向:RIPC的跨器官缺血保护作用、SIRT3在缺血损伤中的线粒体调控功能、NMDAR在缺血耐受中的双向作用。现有研究显示,RIPC可通过释放体液因子激活天然防御机制,显著降低冠状动脉旁路移植术患者的心肌损伤,还能保护脑、肾等器官免受缺血及炎症损伤;SIRT3通过去乙酰化修饰调控多种抗氧化酶活性,维持线粒体氧化还原稳态,在心肌、脑、肠等器官的缺血再灌注损伤中均被证实具有保护作用;NMDAR在缺血损伤中呈现双向效应,过度激活会引发钙超载和神经元凋亡,而亚致死水平的激活则参与缺血耐受的诱导过程。但现有研究存在明显局限性:RIPC在SCIRI中的保护机制尚未明确关键调控蛋白,SIRT3是否参与RIPC介导的SCIRI保护未被报道,NMDAR调控SIRT3的下游信号通路也未得到系统解析。本研究的创新价值在于首次证实RIPC通过SIRT3依赖的方式增强脊髓缺血耐受,明确NMDAR/AMPK/PGC-1α信号通路是RIPC上调SIRT3的核心上游机制,同时提出RIPC联合SIRT3激动剂和厚朴酚(HKL)的联合治疗策略,为SCIRI的临床干预提供了全新的理论依据与实践方向。
3. 研究思路总结与详细解析
本研究的整体框架以“假设-体内外实验验证-机制解析-治疗探索”为闭环逻辑:研究目标是明确RIPC对小鼠SCIRI的神经保护作用及SIRT3的介导地位,解析上游NMDAR/AMPK/PGC-1α信号通路的调控机制,并探索RIPC联合HKL的协同治疗效果;核心科学问题聚焦于RIPC如何通过SIRT3介导SCIRI的神经保护,以及上游信号通路的层级调控关系;技术路线涵盖体内动物模型(WT与SIRT3 KO小鼠的RIPC+SCIRI模型)、体外细胞模型(原代神经元OGD/R模型)、信号通路验证(抑制剂与基因沉默技术)及联合治疗评估四个核心环节。
3.1 体内动物模型构建与神经功能评估
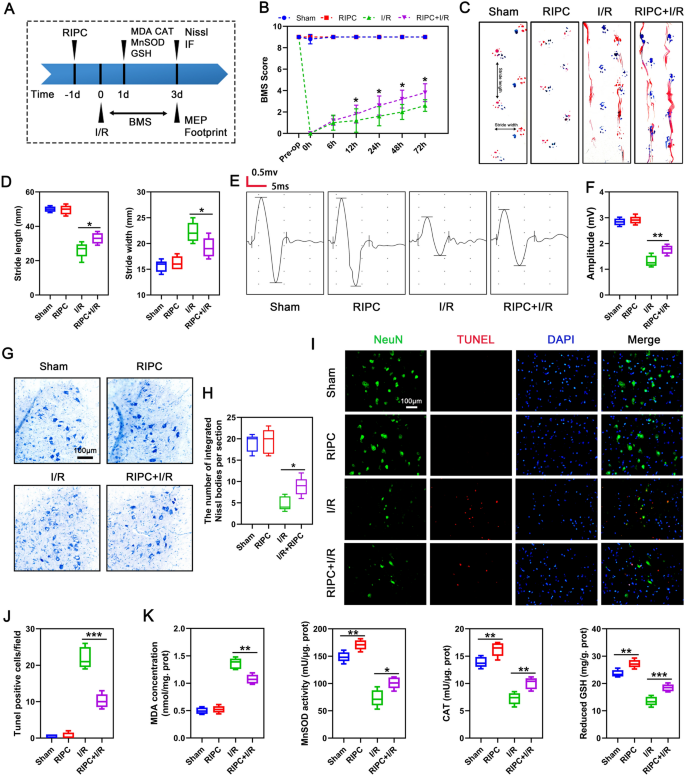
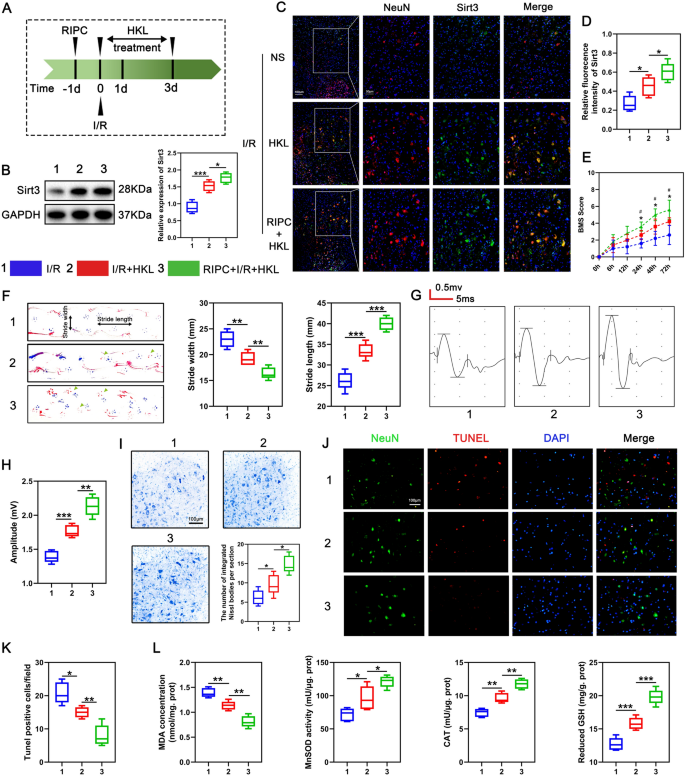
实验目的是验证RIPC对小鼠SCIRI的神经保护作用,并明确SIRT3的必要性。方法细节上,研究采用WT或SIRT3全身敲除(KO)小鼠,对右侧上下肢实施4个循环的5分钟缺血+5分钟再灌注的RIPC处理,24小时后夹闭腹主动脉20分钟诱导SCIRI,再灌注3天后通过多维度指标评估神经功能:采用Basso小鼠运动评分(BMS)动态监测下肢运动功能恢复,足迹分析评估后肢协调性,运动诱发电位(MEP)检测神经传导功能;通过尼氏染色计数脊髓前角运动神经元的尼氏体数量,TUNEL染色检测神经元凋亡率;同时检测脊髓组织的氧化应激指标,包括MnSOD、CAT活性,还原型谷胱甘肽(GSH)、丙二醛(MDA)水平。结果解读显示,RIPC+I/R组小鼠的BMS评分在再灌注3天内显著高于I/R组(n=5,P<0.05),足迹分析显示步长更长、步宽更窄(n=5,P<0.01),MEP振幅显著升高(n=5,P<0.001);尼氏染色结果表明RIPC+I/R组脊髓前角运动神经元的尼氏体数量更多(n=5,P<0.01),TUNEL阳性凋亡神经元比例更低(n=5,P<0.001);氧化应激指标显示RIPC+I/R组MnSOD、CAT活性及GSH水平显著升高,MDA水平降低(n=5,P<0.05)。而在SIRT3 KO小鼠中,RIPC的上述神经保护作用完全消失,氧化应激指标也未出现显著改善。实验所用关键产品:TUNEL检测试剂盒(Beyotime,上海)、Cu/Zn-SOD和Mn-SOD检测试剂盒(Beyotime,上海)、CAT检测试剂盒(Beyotime,上海)、GSH和GSSG检测试剂盒(Beyotime,上海)、MDA检测试剂盒(Beyotime,上海)。
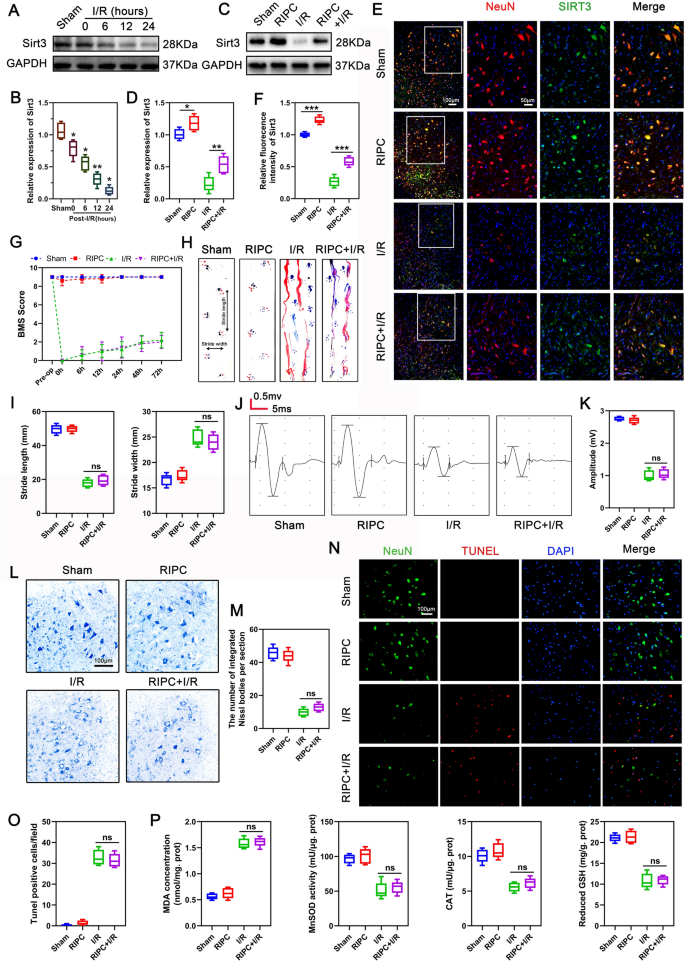
3.2 体外神经元OGD/R模型构建与损伤评估
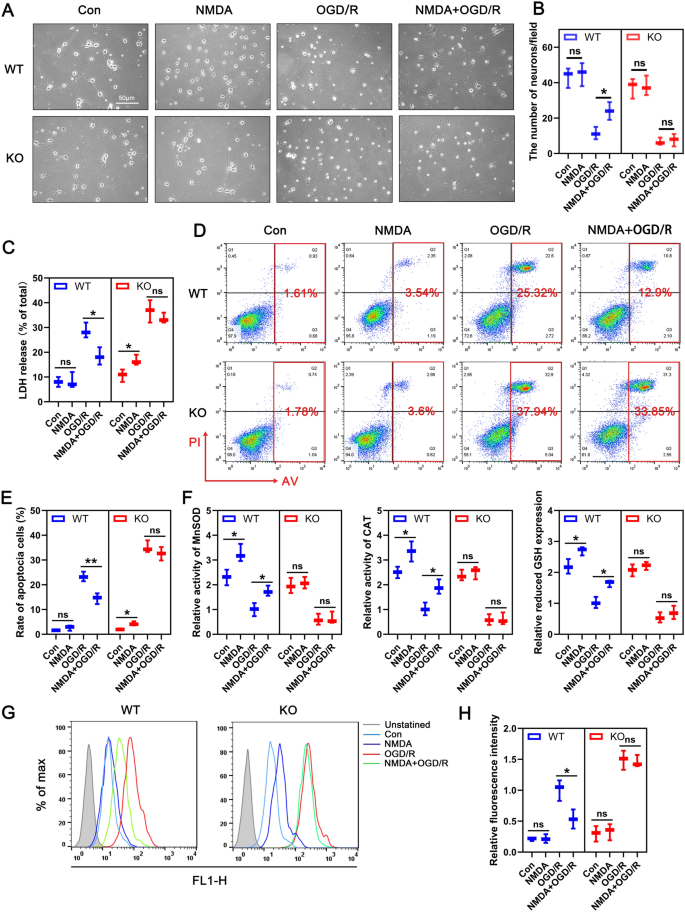
实验目的是在体外模拟RIPC的保护效应,验证NMDA或亚致死谷氨酸预处理对神经元OGD/R损伤的保护作用,并确认SIRT3的介导地位。方法细节上,提取新生小鼠原代皮质神经元,培养至纯度超过90%后,构建氧糖剥夺/复氧(OGD/R)模型模拟体内SCIRI;预处理组采用100μM NMDA或10μM谷氨酸处理4小时,随后通过观察神经元形态、检测乳酸脱氢酶(LDH)释放率、流式细胞术Annexin V/PI染色分析凋亡率,同时检测MnSOD、CAT活性,GSH水平及活性氧(ROS)生成量评估神经元抗氧化能力。结果解读显示,NMDA或谷氨酸预处理可显著改善OGD/R后神经元的形态,降低LDH释放率(n=3,P<0.01)和凋亡率(n=3,P<0.001),提高MnSOD、CAT活性及GSH水平,减少ROS生成(n=3,P<0.05);而在SIRT3 KO来源的神经元中,上述保护效应完全消失,氧化应激指标未出现显著改善。实验所用关键产品:Cell Counting Kit-8(Dojindo,日本)、LDH检测试剂盒(Beyotime,上海)、Annexin V-FITC/PI凋亡试剂盒(Thermo Fisher Scientific,美国)、DCFH-DA ROS探针(Beyotime,上海)。
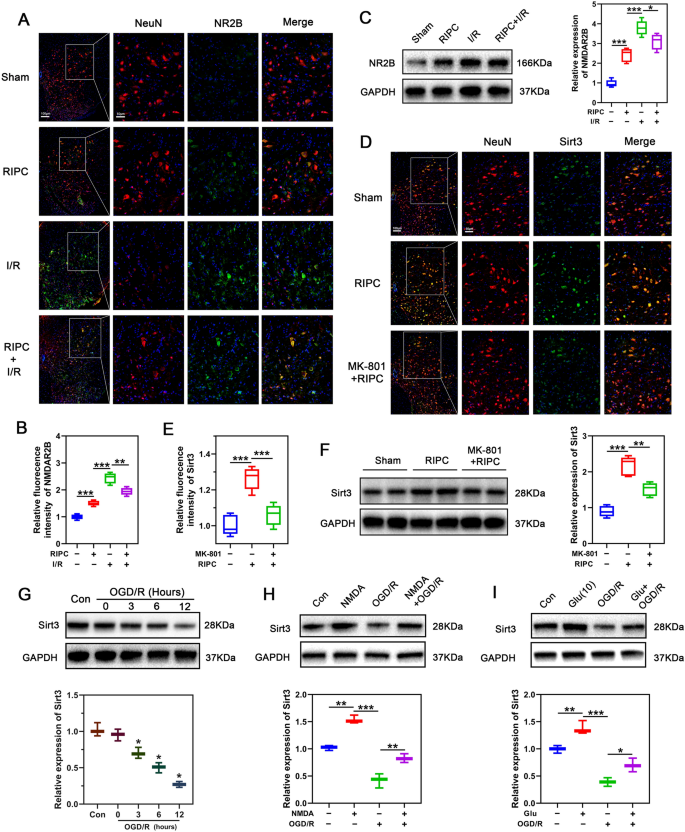
3.3 NMDAR/AMPK/PGC-1α信号通路调控SIRT3的机制验证
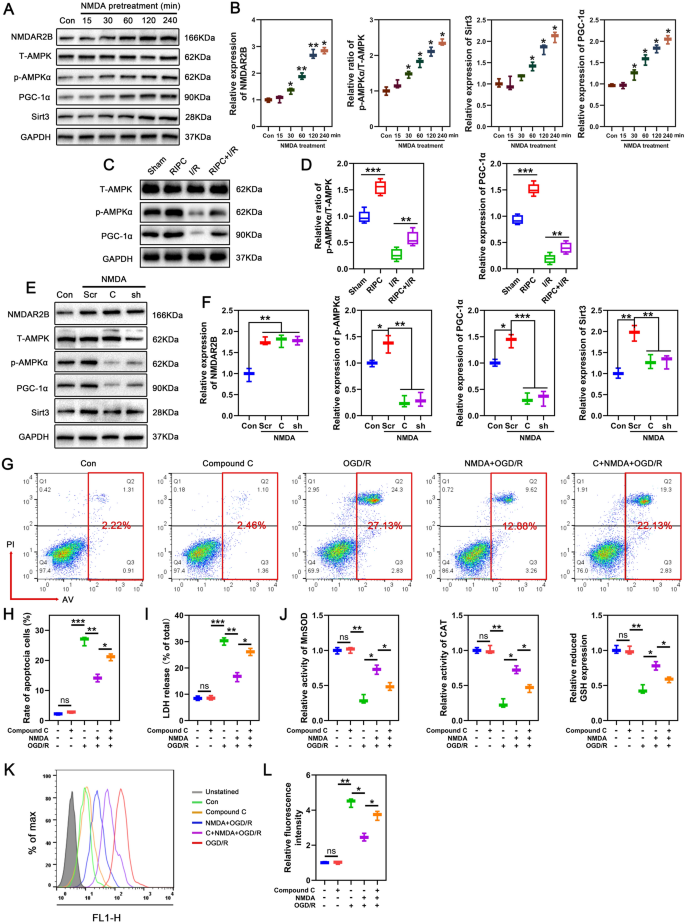
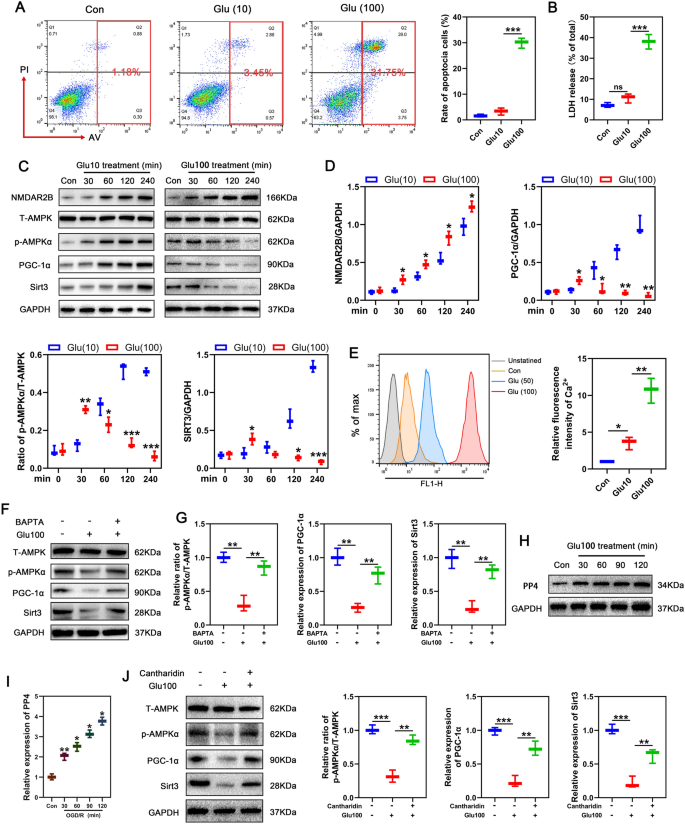
实验目的是解析RIPC上调SIRT3的上游信号通路,明确NMDAR、AMPK、PGC-1α的层级调控关系。方法细节上,体内实验采用NMDAR抑制剂MK-801预处理小鼠,检测RIPC对SIRT3表达的影响;体外实验用NMDA处理神经元,检测AMPK磷酸化、PGC-1α及SIRT3表达的时间依赖性变化;采用AMPK抑制剂Compound C或AMPKα shRNA慢病毒转染神经元,验证AMPK在NMDA调控SIRT3表达中的作用;用不同浓度谷氨酸(10μM亚致死、100μM致死)处理神经元,检测细胞内Ca²+浓度、AMPK磷酸化及蛋白磷酸酶4(PP4)表达,并用钙螯合剂BAPTA-AM或PP4抑制剂斑蝥素处理,验证Ca²+对AMPK的双向调控效应。结果解读显示,MK-801可完全抑制RIPC诱导的SIRT3上调;NMDA处理神经元可时间依赖性地增加AMPK磷酸化、PGC-1α及SIRT3表达;Compound C或AMPK shRNA可显著抑制NMDA诱导的SIRT3和PGC-1α上调;10μM谷氨酸诱导细胞内Ca²+轻度升高,激活AMPK/PGC-1α/SIRT3通路,而100μM谷氨酸诱导Ca²+大量超载,通过上调PP4表达抑制AMPK磷酸化,进而抑制SIRT3表达;BAPTA-AM或斑蝥素可逆转100μM谷氨酸对AMPK/PGC-1α/SIRT3通路的抑制作用。实验所用关键产品:MK-801(MCE,上海)、Compound C(MCE,上海)、AMPKα shRNA慢病毒(Santa Cruz,美国)、Fluo-3 AM Ca²+探针(Beyotime,上海)、斑蝥素(中国药品检验研究院)。
3.4 SIRT3激动剂HKL的治疗效果及联合治疗探索
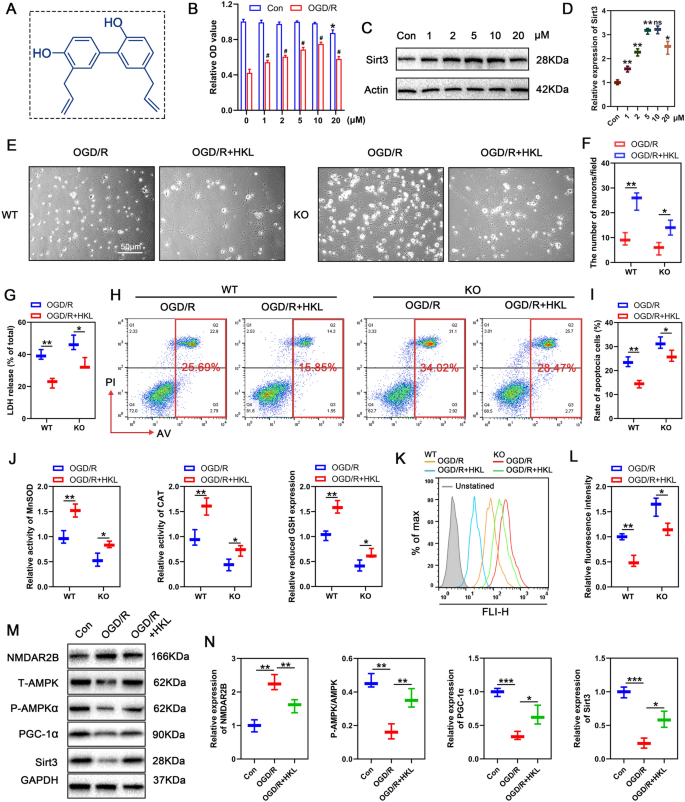
实验目的是验证SIRT3激动剂和厚朴酚(HKL)对SCIRI的治疗作用,并探索RIPC联合HKL的协同治疗效果。方法细节上,体外实验采用不同浓度HKL处理OGD/R后的神经元,检测细胞活力、SIRT3表达、LDH释放率、凋亡率及氧化应激指标;体内实验对SCIRI小鼠术后每日腹腔注射HKL(0.2mg/kg),评估神经功能、组织学损伤及氧化应激指标,并在SIRT3 KO小鼠中验证HKL的依赖效应;联合治疗组术前实施RIPC,术后持续注射HKL,比较其与单独HKL治疗的效果差异。结果解读显示,10μM HKL可显著提高OGD/R后神经元的细胞活力(n=6,P<0.05),上调SIRT3表达,降低LDH释放率和凋亡率(n=3,P<0.01),改善氧化应激指标;体内实验中,HKL可显著改善SCIRI小鼠的神经功能,减少神经元损伤,抑制氧化应激,而在SIRT3 KO小鼠中HKL的保护作用显著减弱;联合治疗组较单独HKL组,SIRT3表达上调更显著(n=5,P<0.01),神经功能恢复更好,神经元损伤更少,氧化应激抑制更明显(n=5,P<0.05)。实验所用关键产品:和厚朴酚(HKL,MCE,上海)。
4. Biomarker研究及发现成果解析
本研究中SIRT3作为RIPC介导SCIRI神经保护的关键调控蛋白,属于线粒体功能相关的Biomarker,其筛选与验证逻辑为:体内实验发现RIPC可上调SCIRI小鼠脊髓组织的SIRT3表达,SIRT3 KO完全消除RIPC的保护作用;体外实验验证NMDA预处理可上调OGD/R后神经元的SIRT3表达,并介导神经保护效应;机制解析明确NMDAR/AMPK/PGC-1α信号通路是RIPC调控SIRT3表达的上游通路。研究过程中,SIRT3的来源为小鼠脊髓组织和原代皮质神经元,验证方法包括蛋白质免疫印迹(WB)检测表达水平、免疫荧光染色定位其在神经元中的分布、通过检测下游抗氧化酶(MnSOD、CAT)的活性验证其功能效应;特异性方面,SIRT3 KO小鼠中RIPC的保护作用完全消失,表明SIRT3是RIPC介导SCIRI神经保护的特异性核心因子;敏感性方面,RIPC可显著上调SCIRI小鼠脊髓组织的SIRT3表达(n=5,P<0.01),NMDA预处理可显著上调OGD/R后神经元的SIRT3表达(n=3,P<0.05)。核心成果方面,SIRT3作为RIPC介导SCIRI神经保护的关键Biomarker,其表达水平与脊髓缺血耐受能力正相关;首次揭示NMDAR/AMPK/PGC-1α信号通路调控SIRT3表达的层级机制,为SCIRI的机制研究提供新靶点;提出RIPC联合HKL的协同治疗策略,通过双重上调SIRT3表达增强脊髓抗氧化能力,为SCIRI的临床治疗提供了全新的可行方案。