1. 领域背景与文献引入
文献英文标题:Botulinum toxin type A promotes microglial M2 polarization and suppresses chronic constriction injury-induced neuropathic pain through the P2X7 receptor;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:神经病理性疼痛与神经胶质细胞调控。
神经病理性疼痛是由体感系统损伤或疾病引发的慢性疼痛,2008年国际疼痛学会重新定义其临床特征后,领域研究逐渐聚焦于神经炎症的调控作用;2010年起,小胶质细胞极化被证实是介导神经病理性疼痛发生发展的核心机制,当前研究热点为通过调控小胶质细胞M1/M2极化平衡开发新型镇痛策略。然而,现有临床治疗手段仍存在疗效有限、机制不明确的问题,尤其是A型肉毒毒素(BTX-A)的镇痛作用已被临床证实,但领域内尚未明确其与小胶质细胞极化的关联机制。针对这一研究空白,本研究旨在探究BTX-A是否通过P2X7受体调控小胶质细胞极化来缓解慢性压迫损伤诱导的神经病理性疼痛,为临床镇痛治疗提供精准的分子依据。
2. 文献综述解析
作者按“神经病理性疼痛病理基础→小胶质细胞极化的调控作用→A型肉毒毒素的镇痛潜力”的逻辑对领域研究进行分类评述,系统梳理了现有研究的结论与局限性,明确了本研究的创新方向。
现有研究已证实神经病理性疼痛的核心病理特征是体感系统损伤引发的神经炎症,小胶质细胞激活后向促炎M1型极化,通过分泌肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)等细胞因子增强脊髓背角神经元突触传递,进而维持慢性疼痛;小胶质细胞向抗炎M2型极化则可通过分泌白细胞介素-10(IL-10)等因子缓解神经炎症,成为潜在治疗靶点。A型肉毒毒素作为临床常用的肌肉松弛剂,已被多项临床研究证实可缓解神经病理性疼痛,但现有研究多聚焦于神经元层面的机制,未涉及对小胶质细胞极化的调控作用。现有研究的技术方法优势在于采用动物模型结合细胞实验的验证体系,可实现体内外结果的互证,但局限性在于缺乏对细胞极化与受体信号通路关联的深入解析,无法明确A型肉毒毒素镇痛作用的核心分子靶点。
通过对比现有研究的未解决问题,本研究的创新点在于首次揭示A型肉毒毒素通过抑制P2X7受体表达,促进小胶质细胞向M2型极化的镇痛机制,填补了领域内对A型肉毒毒素调控神经胶质细胞功能的研究空白,为其临床应用提供了更精准的分子依据。
3. 研究思路总结与详细解析
本研究的整体框架为“动物模型验证镇痛效果→细胞实验明确极化调控→分子实验揭示受体介导机制”的闭环,核心科学问题是A型肉毒毒素是否通过P2X7受体调控小胶质细胞极化来缓解神经病理性疼痛,技术路线遵循“假设提出→体内外验证→靶点确认”的逻辑。
3.1 慢性压迫损伤神经病理性疼痛大鼠模型构建与疼痛阈值检测
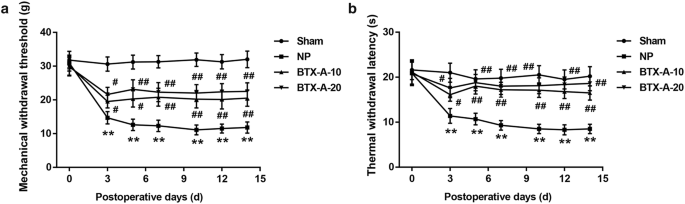
实验目的是验证A型肉毒毒素对慢性压迫损伤(CCI)大鼠疼痛阈值的调控作用;方法细节为将SPF级SD雄性大鼠随机分为假手术组、CCI模型组、10U/kg A型肉毒毒素处理组、20U/kg A型肉毒毒素处理组(n=10/组),CCI术后3天在大鼠跖面皮下注射对应剂量的A型肉毒毒素或生理盐水,分别在术后0、3、5、7、10、12、14天采用电子von Frey仪检测机械缩足阈值(MWT),自动足底热痛仪检测热缩足潜伏期(TWL);结果解读显示,与假手术组相比,CCI模型组大鼠MWT和TWL显著降低(n=10,P<0.01),而A型肉毒毒素处理组的MWT和TWL均显著升高(n=10,P<0.01),且20U/kg剂量的提升效果更显著,说明A型肉毒毒素可剂量依赖性地提升神经病理性疼痛大鼠的疼痛阈值;实验所用关键产品:Allergan Pharmaceuticals Ireland的A型肉毒毒素,IITC-Life Science Instruments的电子von Frey测痛仪(series 2390),Ugo Basile的自动足底热痛仪(No.37370)。
3.2 大鼠脊髓小胶质细胞极化表型检测
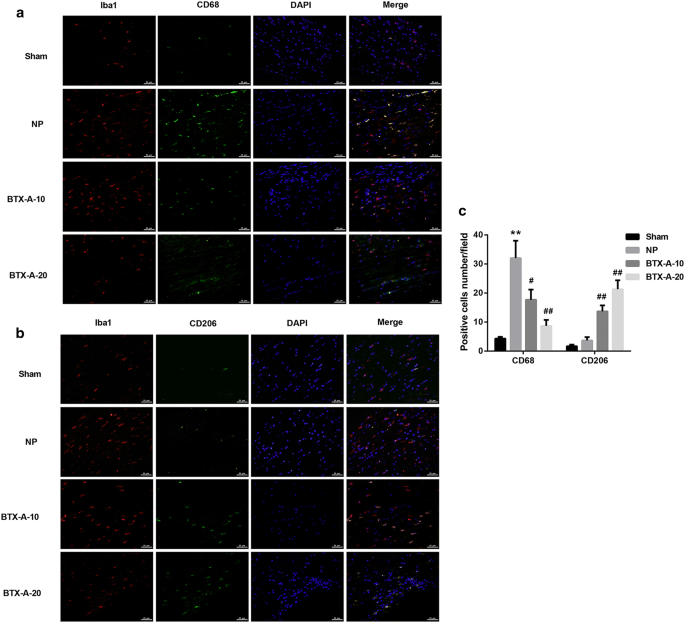
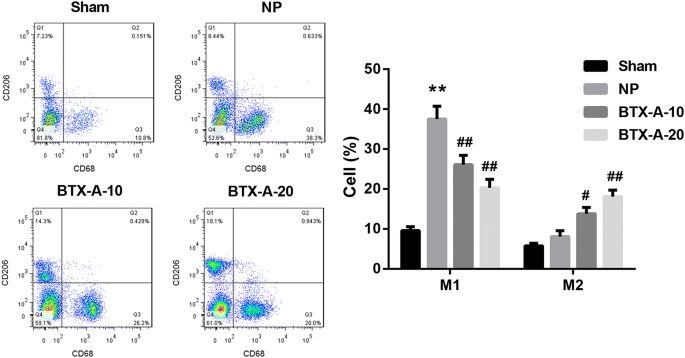
实验目的是探究A型肉毒毒素对CCI大鼠脊髓小胶质细胞极化的影响;方法细节为术后14天取L4-L6脊髓段,采用免疫荧光染色(Iba-1/CD68标记M1型,Iba-1/CD206标记M2型)和流式细胞术检测极化比例;结果解读显示,与假手术组相比,CCI模型组M1型小胶质细胞数量显著增加,A型肉毒毒素处理组M2型细胞数量显著升高(n=10,P<0.01),流式细胞术结果进一步证实A型肉毒毒素可促进小胶质细胞向M2型极化;实验所用关键产品:Abcam的Iba-1、CD206抗体,Santa Cruz Biotechnology的CD68抗体,Becton Dickinson的Accuri C6流式细胞仪。
3.3 LPS激活HAPI小胶质细胞的体外极化验证
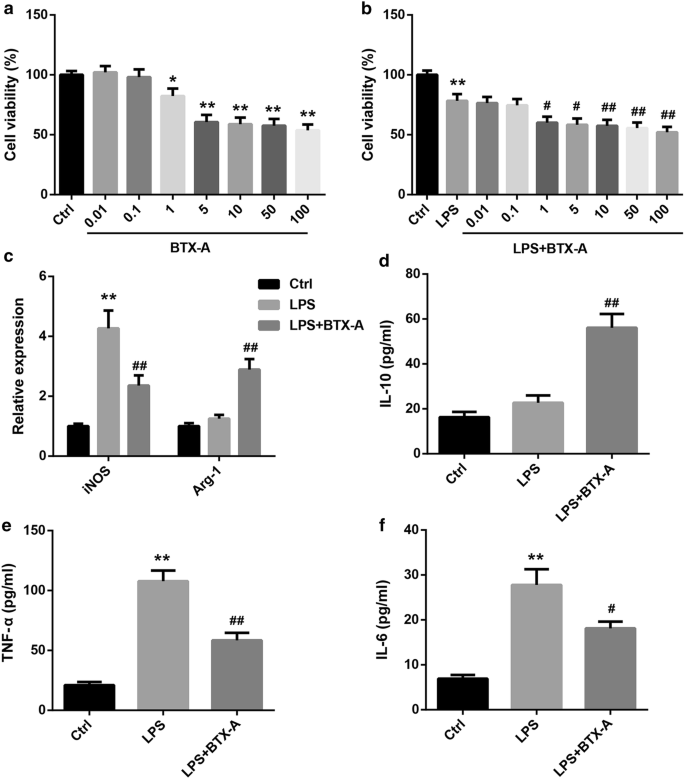
实验目的是在细胞水平验证A型肉毒毒素对小胶质细胞极化的调控作用;方法细节为采用大鼠HAPI小胶质细胞系,先用CCK-8试剂盒筛选A型肉毒毒素的安全作用浓度,确定0.1nM为后续实验剂量,然后用100ng/mL LPS激活小胶质细胞,同时加入0.1nM A型肉毒毒素处理,采用qRT-PCR检测诱导型一氧化氮合酶(iNOS,M1型标记物)、精氨酸酶-1(Arg-1,M2型标记物)的mRNA表达,ELISA检测细胞上清中TNF-α、IL-6(M1相关细胞因子)、IL-10(M2相关细胞因子)的水平;结果解读显示,LPS处理后iNOS mRNA表达及TNF-α、IL-6水平显著升高(n=3,P<0.01),而A型肉毒毒素处理可显著抑制上述M1型标记物的表达,同时显著提升Arg-1 mRNA表达及IL-10水平(n=3,P<0.01),说明A型肉毒毒素可在体外抑制LPS诱导的M1极化,促进M2极化;实验所用关键产品:Sigma-Aldrich的LPS,Beyotime的CCK-8试剂盒,TaKaRa的qRT-PCR试剂盒,R&D Systems的ELISA试剂盒。
3.4 P2X7受体介导的极化调控机制验证
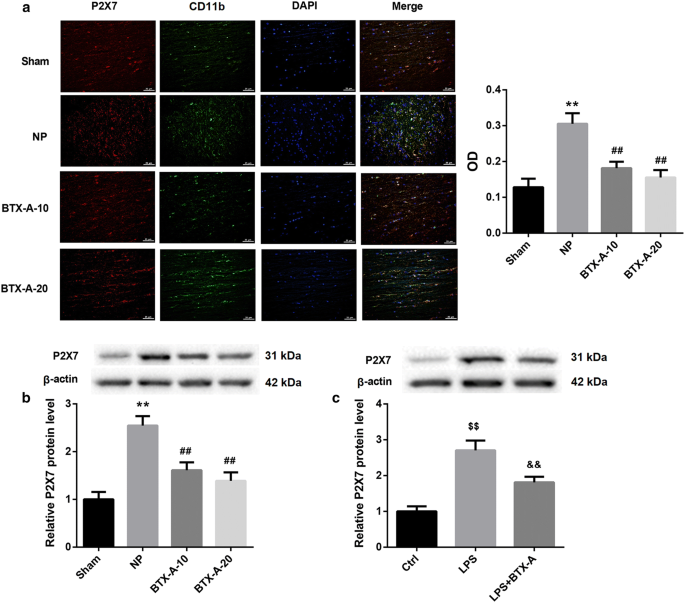
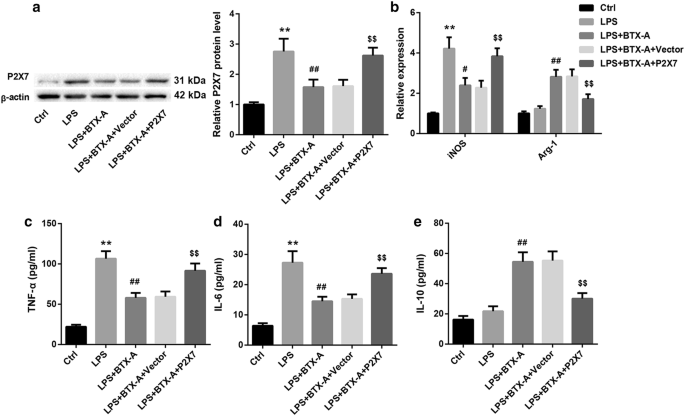
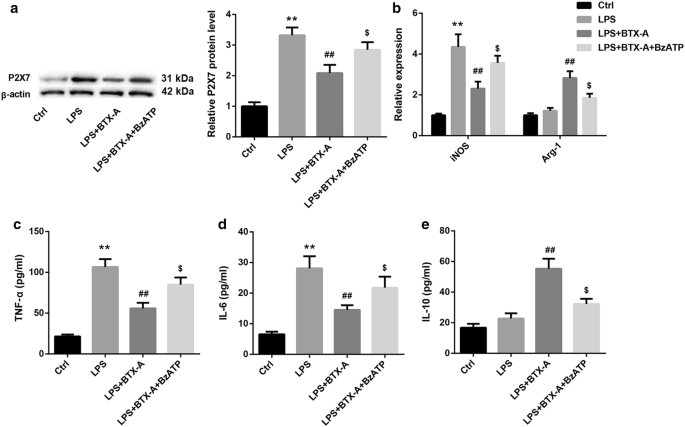
实验目的是明确A型肉毒毒素是否通过P2X7受体调控小胶质细胞极化;方法细节为首先采用免疫荧光双染检测P2X7受体在大鼠脊髓中的细胞定位,然后采用Western blot检测CCI大鼠脊髓及LPS激活HAPI细胞中P2X7的蛋白表达,最后通过转染pcDNA3.1-P2X7载体过表达P2X7,或加入P2X7受体激动剂BzATP处理,检测极化标记物的变化;结果解读显示,P2X7受体仅在CD11b+小胶质细胞中表达,A型肉毒毒素处理可显著降低CCI大鼠脊髓及LPS激活细胞中P2X7的蛋白表达(n=10/3,P<0.01),过表达P2X7或加入BzATP可显著逆转A型肉毒毒素对M1/M2极化的调控作用,即M1型标记物表达回升,M2型标记物表达降低(n=3,P<0.01),说明P2X7受体是A型肉毒毒素调控小胶质细胞极化的关键介导靶点;实验所用关键产品:Invitrogen的P2X7抗体、pcDNA3.1载体、Lipofectamine 2000转染试剂。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker为P2X7嘌呤能受体,其作为A型肉毒毒素调控小胶质细胞极化的关键靶点,通过“动物模型表达检测→细胞功能验证→分子靶点确认”的完整逻辑链条完成筛选与验证。
P2X7受体属于嘌呤能离子通道受体家族,主要表达于小胶质细胞表面,本研究中其筛选与验证逻辑为:首先在CCI大鼠脊髓中检测到P2X7受体表达升高,且A型肉毒毒素可降低其表达;然后在HAPI细胞中验证A型肉毒毒素对P2X7的调控作用;最后通过过表达与激动剂处理,确认其介导小胶质细胞极化的功能。
该Biomarker的来源为大鼠脊髓小胶质细胞及HAPI小胶质细胞系,验证方法包括免疫荧光染色(检测细胞定位)、Western blot(检测蛋白表达)、qRT-PCR(关联极化标记物表达),特异性数据显示P2X7受体仅在CD11b+小胶质细胞中表达,CCI模型组大鼠脊髓中P2X7蛋白表达量较假手术组升高约60%(n=10,P<0.01),A型肉毒毒素处理后降低约40%(n=10,P<0.01);敏感性数据显示,0.1nM A型肉毒毒素即可显著降低LPS激活HAPI细胞中P2X7的蛋白表达(n=3,P<0.01)。
核心成果提炼显示,P2X7受体是A型肉毒毒素促进小胶质细胞M2极化的关键靶点,抑制其表达可逆转神经炎症介导的疼痛;创新性在于首次揭示P2X7受体在A型肉毒毒素镇痛作用中的核心介导作用,统计学结果显示,A型肉毒毒素处理后P2X7表达显著降低(P<0.01),过表达P2X7可显著逆转M2极化效应(P<0.01),为神经病理性疼痛的治疗提供了新的分子靶点。
