1. 领域背景与文献引入
文献英文标题:Vincristine alleviates adriamycin-induced nephropathy through stabilizing actin cytoskeleton;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:儿童激素依赖型肾病综合征治疗机制研究
微小病变肾病综合征(MCNS)是儿童群体中常见的原发性肾小球疾病,领域共识:约90%的患儿对泼尼松初始治疗响应良好,但近30%的病例会出现频繁复发或进展为激素依赖型肾病综合征(SDNS)。长期反复的激素治疗会带来严重的毒副作用,因此临床亟需安全有效的激素替代治疗方案。目前用于SDNS的激素替代药物存在诸多局限性:左旋咪唑或霉酚酸停药后复发率显著升高,无法实现长期缓解;烷化剂虽能有效降低复发率,但反复使用会导致生殖系统毒性,限制了其在儿童患者中的应用;钙调磷酸酶抑制剂可快速缓解症状,但长期使用的肾毒性风险不可忽视。
对于长春新碱(VCR)的研究,早期多为联合化疗方案中的附带观察,无法明确其对肾病综合征的直接治疗作用,仅有的个案报道虽提示单药有效,但缺乏系统的机制研究与体内外实验验证。作者团队此前通过临床研究证实低剂量VCR可有效缓解12例难治性SDNS患儿的症状,但VCR发挥肾脏保护作用的具体机制始终未被阐明,这一研究空白为本研究的开展提供了必要性与学术价值。
2. 文献综述解析
本文献综述部分以“SDNS替代治疗方案的局限性与VCR潜在治疗价值”为核心逻辑,按现有治疗手段的药物类型进行分类评述,同时梳理VCR在肾病领域的应用历程与未解问题。
现有研究显示,针对SDNS的激素替代治疗可分为三类:第一类为免疫调节剂如左旋咪唑、霉酚酸,其优势在于短期使用的安全性较高,但局限性是停药后复发率显著升高;第二类为烷化剂,虽能有效降低复发率,但反复使用会导致生殖系统毒性,限制了其在儿童患者中的应用;第三类为钙调磷酸酶抑制剂,可快速缓解症状,但长期使用的肾毒性风险不可忽视。对于VCR的研究,早期多为联合化疗方案中的附带观察,无法明确其对肾病综合征的直接治疗作用,仅有的个案报道虽提示单药有效,但缺乏系统的机制研究与体内外实验验证。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次在体内外模型中明确低剂量VCR的肾脏保护作用并非依赖其抗肿瘤的微管抑制功能,而是通过稳定肌动蛋白细胞骨架、调控整合素-黏着斑激酶通路实现,填补了VCR治疗SDNS机制研究的空白。
3. 研究思路总结与详细解析
本研究的核心目标是明确VCR缓解阿霉素(ADR)诱导肾病的分子机制,核心科学问题聚焦于“VCR如何通过肌动蛋白细胞骨架相关通路发挥肾脏保护作用”,技术路线遵循“体内模型药效验证→体外细胞模型机制探究→分子通路验证”的闭环逻辑,通过形态学检测、分子生物学实验等多维度验证VCR的作用靶点。
3.1 动物模型构建与药效验证
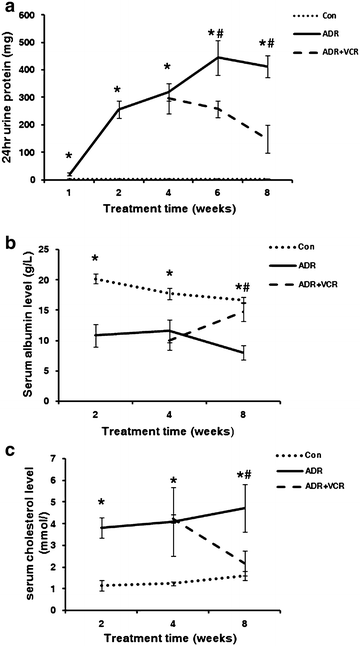
实验目的是构建ADR诱导的大鼠肾病模型,验证VCR的体内治疗效果。方法细节为:选取体重200±20g的雄性SD大鼠,尾静脉注射7.5mg/kg ADR构建肾病模型,对照组注射等量生理盐水;4周后将模型大鼠分为ADR组与ADR+VCR组,VCR组每周两次静脉注射0.2mg/kg VCR(由临床剂量换算而来),持续治疗4周;每周检测24小时尿蛋白水平,在给药后2、4、8周采集血液检测血清白蛋白与胆固醇水平,实验终点取肾脏组织进行组织学与电镜观察。
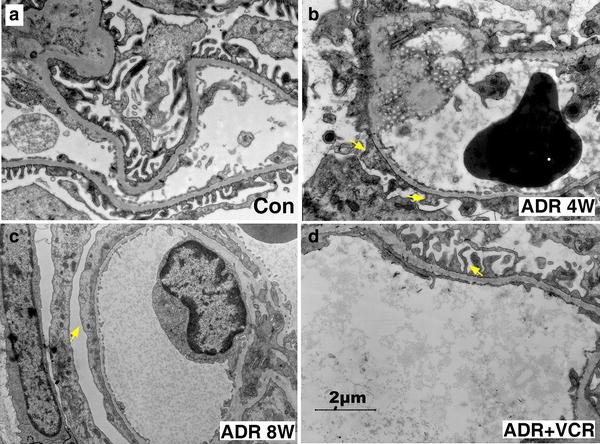
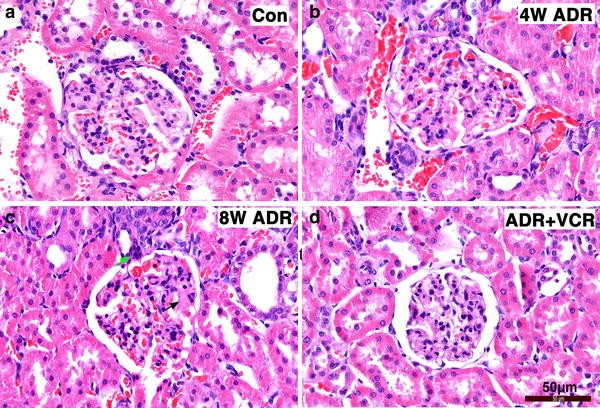
结果解读:ADR组大鼠在注射后1周即出现24小时尿蛋白显著升高(p<0.05),第6周达到峰值,血清白蛋白水平持续降低、胆固醇水平持续升高(p<0.05);电镜观察显示,ADR处理4周后足细胞足突广泛融合,8周后足突融合形成片状结构,HE染色显示8周时出现系膜基质轻度扩张与间质细胞浸润;VCR治疗2周后,大鼠24小时尿蛋白水平较ADR组显著降低(p<0.05),4周后血清白蛋白与胆固醇水平恢复至正常范围,电镜显示足突重新呈现裂隙状结构,HE染色显示肾脏组织病变明显减轻。
实验所用关键产品:Trizol(Invitrogen)、PrimeScript RT Kit(TaKaRa)、SYBR Green PCR Master Mix(TaKaRa)、7900HT Fast Realtime PCR系统(ABI)、RIPA裂解液(Beyotime)、BCA蛋白定量试剂盒(Bio-Rad)
3.2 足细胞模型构建与形态学检测
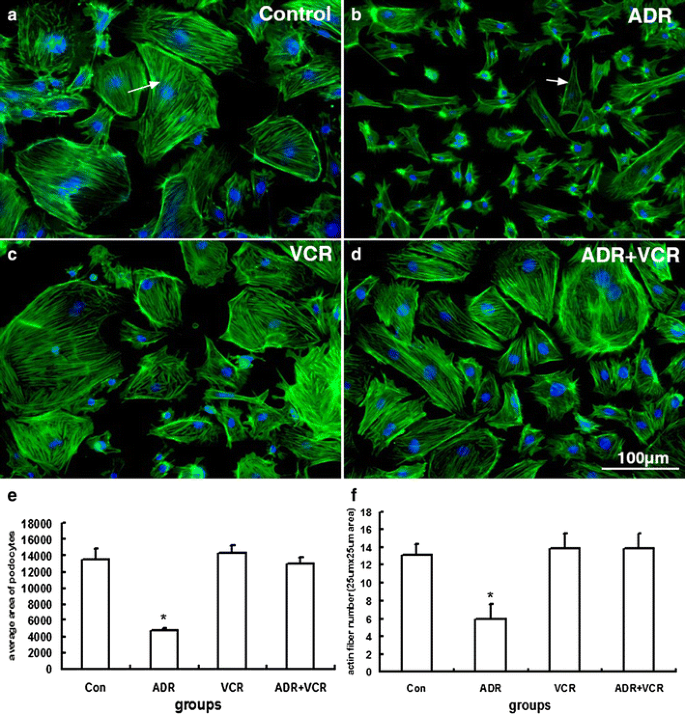
实验目的是建立ADR损伤的体外足细胞模型,观察VCR对足细胞形态的影响。方法细节为:使用永生化小鼠足细胞,先在33℃含γ-干扰素的培养基中培养5天,随后转移至37℃无γ-干扰素的培养基中培养12-14天诱导分化;分化成熟的足细胞用0.5μM ADR处理诱导损伤,VCR组在ADR处理1小时后加入5nM VCR,继续培养24小时后进行形态学观察。
结果解读:正常分化的足细胞呈多边形,胞质内有密集的线性肌动蛋白纤维;ADR处理后,足细胞收缩为纺锤形,胞质内肌动蛋白纤维显著减少;VCR处理后,足细胞形态恢复为多边形,肌动蛋白纤维的分布与数量与对照组无显著差异(p>0.05),细胞面积较ADR组显著增大(p<0.05)。
实验所用关键产品:Actin-stain™488鬼笔环肽(Cytoskeleton)、DM6000 upright显微镜(Leica)
3.3 肌动蛋白细胞骨架稳定性分析
实验目的是验证VCR对ADR损伤足细胞肌动蛋白细胞骨架的稳定作用。方法细节为:采用Actin-stain™488鬼笔环肽对足细胞进行免疫荧光染色,通过Image-Pro Plus软件定量分析细胞面积与肌动蛋白纤维数量,每组设置3个独立重复实验。
结果解读:ADR组足细胞的平均面积较对照组降低约40%(n=3,p<0.05),肌动蛋白纤维数量减少约50%(n=3,p<0.05);VCR处理组的足细胞面积与肌动蛋白纤维数量与对照组无显著差异(p>0.05),说明低剂量VCR可有效抑制ADR诱导的肌动蛋白细胞骨架解聚,维持足细胞的正常形态。
3.4 整合素与黏着斑激酶分子表达检测
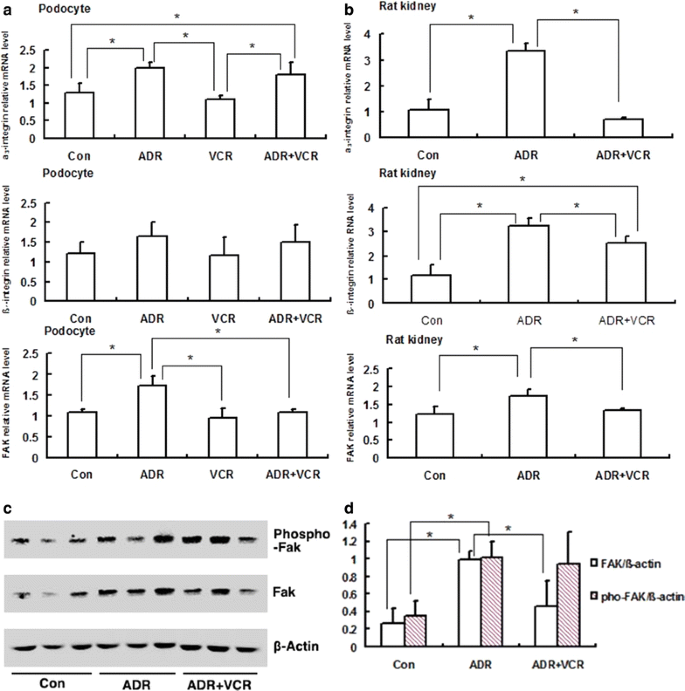
实验目的是探究VCR稳定肌动蛋白细胞骨架的分子通路靶点。方法细节为:提取ADR损伤及VCR处理后的足细胞与大鼠肾皮质组织的总RNA与蛋白,通过实时荧光定量PCR(qPCR)检测α3β1整合素与黏着斑激酶(FAK)的mRNA表达水平,通过蛋白质免疫印迹(Western blot)检测FAK蛋白及Tyr397磷酸化水平,每组设置至少3个生物学重复。
结果解读:qPCR结果显示,ADR组足细胞与肾皮质中α3β1整合素与FAK的mRNA表达水平较对照组显著升高(n≥3,p<0.05),VCR处理后其表达水平显著降低(n≥3,p<0.05);Western blot结果显示,ADR组肾皮质中FAK蛋白表达水平显著升高(n≥3,p<0.05),VCR处理后恢复至接近对照组水平,但FAK的Tyr397磷酸化水平未被显著逆转(p>0.05);此外,VCR对足细胞损伤相关的其他分子如podocin、nephrin等的表达无显著影响。
实验所用关键产品:抗FAK抗体(BD Transduction)、抗磷酸化FAK抗体(Millipore)、IRDye 800标记的羊抗兔二抗(Rockland)、Licor Odyssey红外成像系统(LI-COR Biosciences)
4. Biomarker研究及发现成果
本研究中涉及的Biomarker为α3β1整合素与黏着斑激酶(FAK),筛选逻辑基于足细胞损伤中肌动蛋白细胞骨架调控的核心通路——整合素-黏着斑激酶通路,通过体内外模型的多维度验证,明确其表达变化与VCR治疗效果的关联。
Biomarker的来源为ADR诱导肾病大鼠的肾皮质组织与体外培养的损伤足细胞,验证方法包括实时荧光定量PCR(qPCR)与蛋白质免疫印迹(Western blot)。特异性与敏感性数据显示,ADR诱导的足细胞损伤与肾病模型中,α3β1整合素与FAK的mRNA表达水平显著升高(n≥3,p<0.05),FAK蛋白表达也呈相同趋势,提示二者可作为足细胞损伤的分子标志物;VCR处理后,二者的表达水平显著降低(n≥3,p<0.05),与肾病症状的缓解呈正相关。
核心成果提炼:α3β1整合素与FAK作为足细胞损伤的关键分子标志物,VCR通过抑制其过表达而非调控其磷酸化水平,实现对肌动蛋白细胞骨架的稳定作用,进而减轻足细胞损伤与肾病综合征症状,这是首次明确VCR治疗SDNS的分子靶点,为SDNS的精准治疗提供了新的理论依据与潜在靶点,统计学结果显示各组间差异具有显著性(p<0.05),样本量为每组至少3个生物学重复。
