1. 领域背景与文献引入
文献英文标题:Peptidylarginine deiminase IV promotes the development of chemoresistance through inducing autophagy in hepatocellular carcinoma;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:肝细胞癌化疗耐药机制
肝细胞癌是中国发病率和死亡率均较高的恶性肿瘤,手术切除是早期患者的首选治疗方案,但多数患者确诊时已处于晚期,化疗成为主要治疗手段之一。然而,化疗耐药是导致晚期肝细胞癌治疗失败的核心瓶颈,其中多药耐药(MDR)是最常见的耐药类型,主要由MDR1基因编码的P-糖蛋白(P-gp)过表达介导,通过主动泵出细胞内化疗药物降低疗效。近年来,自噬作为一种保守的细胞自我降解机制,被发现可通过维持细胞存活参与化疗耐药的调控,但具体的上游调控分子仍未完全阐明。肽酰精氨酸脱亚胺酶4(PADI4)可催化蛋白质精氨酸残基的瓜氨酸化,参与基因表达调控、细胞分化等多种病理生理过程,且在多种肿瘤组织中异常表达,但其在肝细胞癌化疗耐药中的作用及调控机制尚未见报道,这一研究空白促使本研究探讨PADI4与肝细胞癌化疗耐药的关联及潜在机制,为逆转化疗耐药提供新的分子靶点。
2. 文献综述解析
本文综述部分从PADI家族功能、自噬与肿瘤化疗耐药的关系、肝细胞癌多药耐药机制三个维度展开,系统梳理了领域内现有研究的进展与不足。关于PADI家族,现有研究表明其广泛分布于哺乳动物体内,可依赖钙离子和巯基催化精氨酸瓜氨酸化,参与基因表达、上皮细胞终末分化等过程,其中PADI4在胚胎干细胞、白细胞及多种肿瘤细胞中表达,与肿瘤发生、类风湿关节炎等疾病相关,但在肝细胞癌中的功能研究较为匮乏。关于自噬与化疗耐药,现有研究证实自噬在肿瘤中的作用具有双面性,既可以通过降解受损细胞器维持细胞存活,介导化疗耐药,也可以在特定条件下诱导细胞死亡,抑制肿瘤进展,但自噬介导肝细胞癌化疗耐药的上游调控分子仍不明确。关于肝细胞癌多药耐药,现有研究明确MDR1/P-gp过表达是核心机制,通过泵出化疗药物降低细胞内药物浓度,但针对MDR1的靶向治疗效果有限,亟需寻找新的耐药调控靶点。本文创新点在于首次将PADI4与肝细胞癌化疗耐药关联起来,揭示了PADI4通过诱导自噬介导耐药的新机制,填补了PADI4在肝细胞癌耐药领域的研究空白,为逆转耐药提供了新的干预方向。
3. 研究思路总结与详细解析
本研究以“PADI4是否参与肝细胞癌化疗耐药及具体机制”为核心科学问题,采用“临床样本关联分析→细胞及动物实验验证耐药表型→自噬检测及抑制剂实验验证机制”的闭环技术路线,明确了PADI4通过诱导自噬促进肝细胞癌化疗耐药的作用及机制。
3.1 临床样本PADI4表达与化疗耐药的关联分析
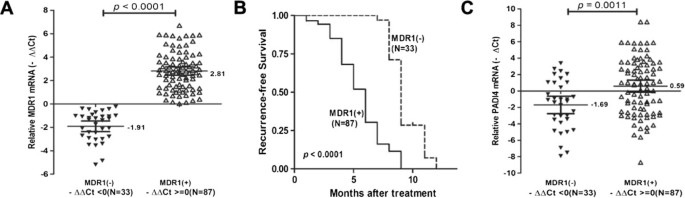
实验目的是明确肝细胞癌患者肿瘤组织中PADI4表达与化疗耐药及预后的相关性;方法细节是收集120例接受手术联合经导管动脉化疗栓塞(TACE)的肝细胞癌患者手术前后静脉血样本,采用实时荧光定量PCR检测外周血中MDR1 mRNA表达,将MDR1表达升高的患者归为耐药组(MDR1+,87例),表达降低的归为敏感组(MDR1-,33例),同时检测患者肿瘤组织中PADI4 mRNA表达,并采用Kaplan-Meier法分析两组患者的无进展生存期;结果解读:耐药组肿瘤组织中PADI4 mRNA表达显著高于敏感组(Mean -∆Ct ± SD = 0.59 ± 0.37 vs -1.69 ± 0.53,n=120,P=0.0011),Kaplan-Meier分析显示耐药组无进展生存期显著短于敏感组(中位生存期6个月vs9个月,n=120,P<0.0001,风险比HR=6.339,95%置信区间CI:3.742-10.74),提示PADI4高表达与肝细胞癌化疗耐药及不良预后密切相关;实验所用关键产品:实时荧光定量PCR系统(Stratagene Mx3000P),TRIzol试剂(领域常规使用Invitrogen产品)。
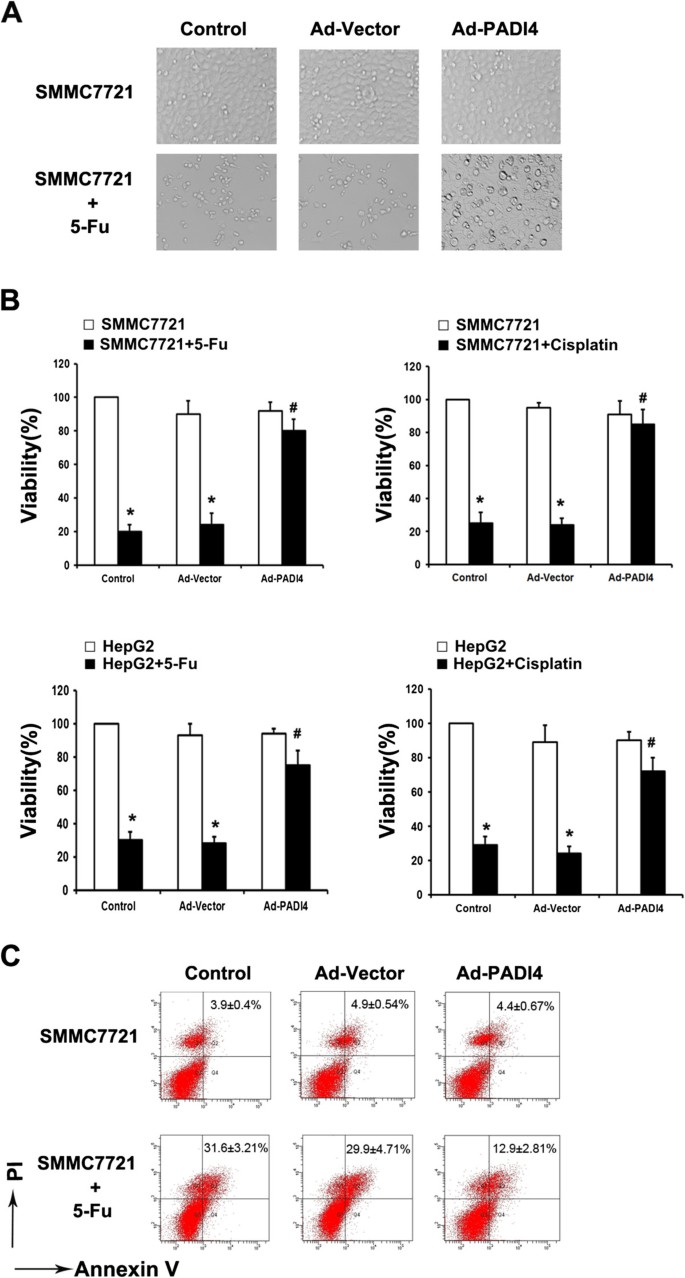
3.2 细胞水平验证PADI4对肝细胞癌化疗耐药的调控作用
实验目的是在体外验证PADI4过表达是否增强肝细胞癌细胞的化疗耐药性;方法细节是构建携带PADI4基因的腺病毒载体(AdPADI4),以空载腺病毒(Ad-Vector)为对照,感染人肝细胞癌细胞系SMMC-7721和Hep-G2,采用MTT法检测5-氟尿嘧啶(5-Fu)和顺铂处理后的细胞活力,采用流式细胞术(PI/Annexin V-PE双染色)检测细胞凋亡率;结果解读:与对照组相比,PADI4过表达组在5-Fu或顺铂处理后细胞活力显著升高(n=3,P<0.05),凋亡率显著降低(n=3,P<0.05),表明PADI4过表达可增强肝细胞癌细胞对化疗药物的耐药性;实验所用关键产品:AdPADI4腺病毒载体(上海吉凯基因),MTT试剂(Sigma,Cat.M2003),PI/Annexin V-PE凋亡检测试剂盒(凯基生物,Cat.KGA108),BD FACSAria流式细胞仪。
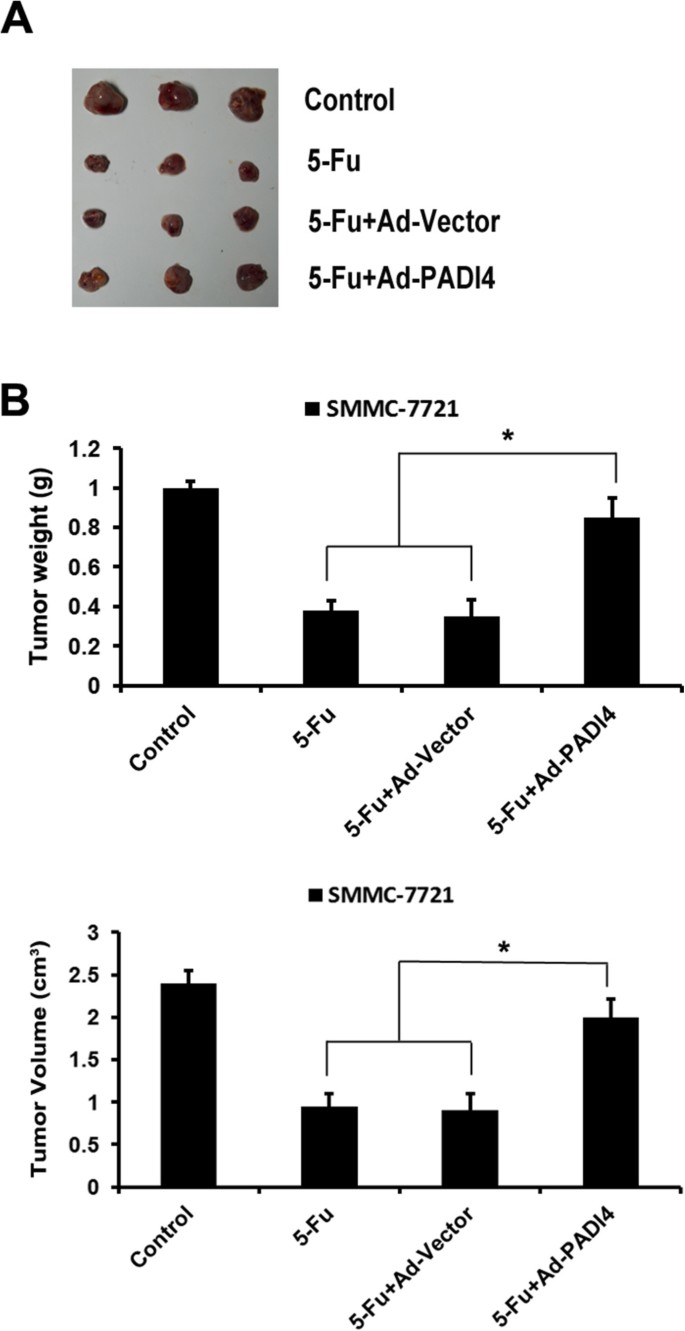
3.3 动物水平验证PADI4对肝细胞癌化疗耐药的调控作用
实验目的是在体内验证PADI4对肝细胞癌化疗耐药的调控作用;方法细节是将过表达PADI4的SMMC-7721细胞(5×10^6个)皮下接种于裸鼠腋窝部位,待肿瘤体积达到一定大小后,每3天瘤内注射5-Fu(30mg/kg),连续处理27天后处死小鼠,剥离肿瘤并检测肿瘤重量和体积;结果解读:与对照组相比,PADI4过表达组肿瘤重量和体积显著增大(n=6,P<0.05),表明PADI4在体内同样可增强肝细胞癌的化疗耐药性;实验所用关键产品:SPF级裸鼠(领域常规使用北京维通利华或上海斯莱克产品),5-Fu(齐鲁制药)。
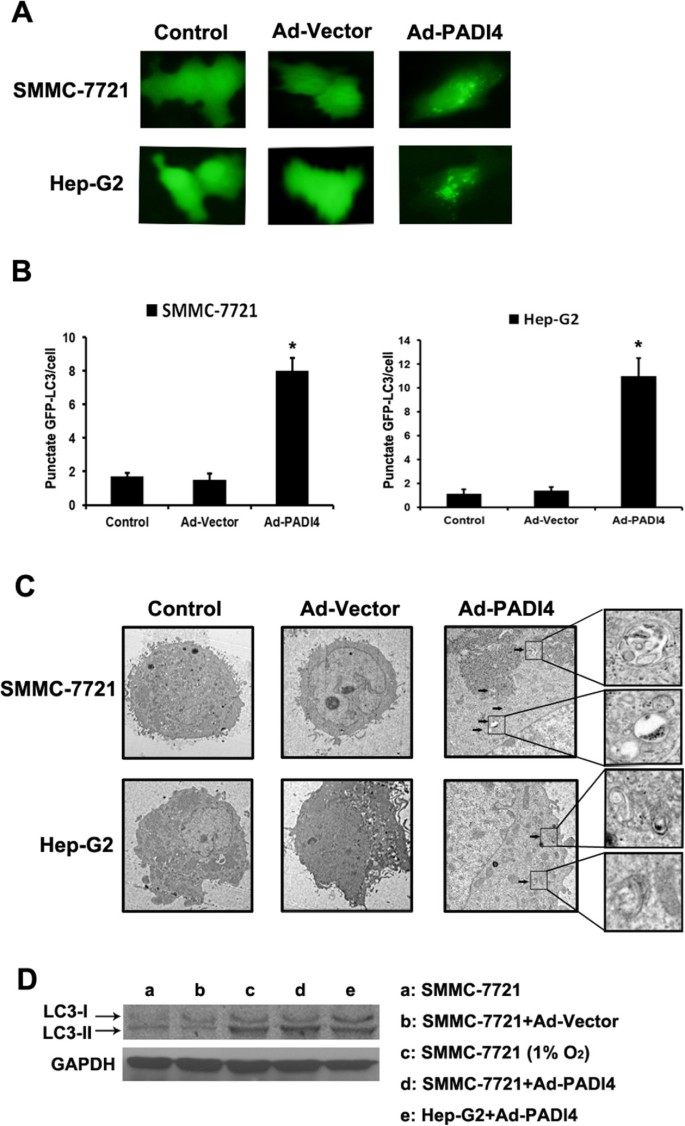
3.4 PADI4诱导肝细胞癌细胞自噬的检测
实验目的是明确PADI4是否可诱导肝细胞癌细胞发生自噬;方法细节是采用Fugene HD转染试剂将GFP-LC3质粒转染至SMMC-7721和Hep-G2细胞,AdPADI4处理24小时后,荧光显微镜下观察GFP-LC3点状聚集情况;采用透射电镜观察细胞内自噬体超微结构;采用蛋白质免疫印迹(Western blot)检测LC3-I/LC3-II蛋白表达水平;结果解读:PADI4过表达后,GFP-LC3点状聚集细胞比例显著升高(n=3,P<0.05),透射电镜下可见大量双层膜结构的自噬体,Western blot结果显示LC3-II/LC3-I比值显著升高,表明PADI4可诱导肝细胞癌细胞发生自噬;实验所用关键产品:GFP-LC3质粒(领域常规使用Addgene产品),Fugene HD转染试剂(Roche,Cat.04709705001),透射电镜(Philips CM-120),PADI4抗体(Abcam,1:1000),LC3抗体(Novus Biologicals,1:1000),ECL发光试剂(Beyotime)。
3.5 自噬抑制剂逆转PADI4介导的肝细胞癌化疗耐药
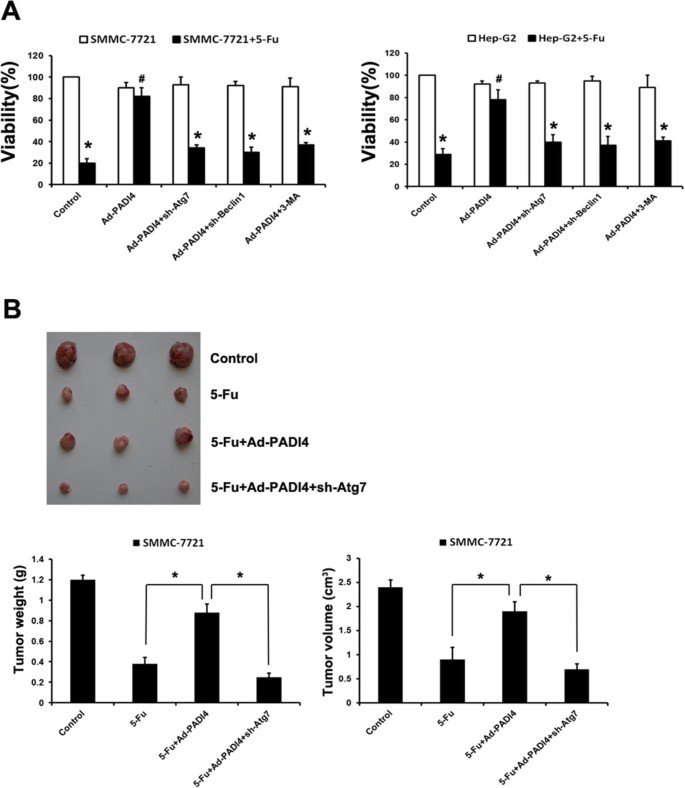
实验目的是验证自噬在PADI4介导的化疗耐药中的关键作用;方法细节是采用自噬抑制剂3-甲基腺嘌呤(3-MA)、氯喹(CQ)处理过表达PADI4的肝细胞癌细胞,或采用shRNA沉默自噬相关基因ATG7、Beclin1,MTT法检测细胞活力,流式细胞术检测凋亡率;同时构建裸鼠皮下移植瘤模型,瘤内注射3-MA联合5-Fu,检测肿瘤生长情况;结果解读:自噬抑制剂或shRNA沉默自噬基因后,PADI4过表达细胞对5-Fu的敏感性显著恢复,细胞活力降低、凋亡率升高(n=3,P<0.05);体内实验中,3-MA联合5-Fu可显著抑制PADI4过表达组肿瘤生长(n=6,P<0.05),表明自噬是PADI4介导化疗耐药的关键机制;实验所用关键产品:3-MA(Sigma,Cat.M9281),shRNA-ATG7/Beclin1(上海吉凯基因)。
4. Biomarker研究及发现成果解析
本研究鉴定了PADI4作为肝细胞癌化疗耐药的潜在预后Biomarker,明确了其通过诱导自噬介导耐药的功能及临床价值。Biomarker定位:PADI4属于分子型Biomarker,筛选与验证逻辑为“临床样本关联分析初步筛选→细胞及动物实验验证耐药调控功能→机制研究明确作用通路”。研究过程详述:PADI4的来源为肝细胞癌患者的肿瘤组织,验证方法采用实时荧光定量PCR检测mRNA表达水平,特异性方面,耐药组PADI4表达显著高于敏感组(P=0.0011),敏感性方面,无进展生存期分析显示PADI4高表达组患者生存期显著缩短(HR=6.339,95%CI:3.742-10.74,P<0.0001),提示PADI4具有区分耐药与敏感患者的潜力。核心成果提炼:PADI4是首次被报道的肝细胞癌化疗耐药调控分子,其通过诱导自噬维持细胞存活,进而介导化疗耐药;作为预后Biomarker,PADI4高表达提示患者化疗耐药风险高、预后差;同时,自噬抑制剂可有效逆转PADI4介导的耐药,为临床治疗提供了新的联合治疗策略。推测:PADI4可能通过调控mTORC1等自噬相关信号通路发挥作用,未来需进一步开展大样本多中心验证及蛋白水平检测,明确其临床转化价值。
