1. 领域背景与文献引入
文献英文标题:PGRMC1 effects on metabolism, genomic mutation and CpG methylation imply crucial roles in animal biology and disease;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:肿瘤生物学与表观遗传学
孕酮受体膜组分1(PGRMC1)作为膜相关孕酮受体家族的核心成员,其功能研究覆盖肿瘤生物学、胚胎发育、代谢调控等多个生命科学细分领域。领域发展关键节点包括:2000年左右发现其与肿瘤细胞耐药性的关联,2010年明确其血红素结合与代谢调控功能,2016年揭示其在胚胎发育中的潜在调控作用。当前研究热点聚焦于PGRMC1的翻译后修饰(尤其是磷酸化)对细胞功能的调控机制,以及其在肿瘤细胞可塑性与胚胎干细胞状态维持中的作用。未解决的核心问题包括:不同磷酸化位点的协同调控网络尚不清晰,磷酸化修饰如何关联代谢、表观遗传与基因组稳定性的分子机制未明确,且缺乏系统性的突变体研究解析特定位点的功能。
现有研究虽已发现PGRMC1磷酸化水平在乳腺癌亚型中存在显著差异,但未深入解析其对细胞多维度功能的调控效应,尤其是表观遗传层面的调控机制。针对这一研究空白,本文通过构建PGRMC1特定磷酸化位点突变体,系统解析其对细胞代谢、基因组甲基化与突变率的调控作用,旨在明确PGRMC1磷酸化状态调控细胞可塑性的分子机制,为理解其在胚胎发育与肿瘤发生中的关键作用提供新的实验依据。
2. 文献综述解析
作者对PGRMC1现有研究的分类维度为功能进化时间与调控方式,将其功能分为两类:一是古老保守功能,包括血红素合成、甾醇代谢、DNA损伤修复等,这类功能从单细胞真核生物延续至后生动物;二是后生动物特化功能,包括胚胎组织分化、肿瘤耐药性、细胞可塑性调控等,这类功能伴随后生动物的进化出现。
现有研究的关键结论包括:PGRMC1通过结合细胞色素P450参与药物代谢与肿瘤耐药,通过调控PI3K/Akt通路影响细胞增殖与迁移,通过血红素结合调控细胞代谢稳态;技术方法优势在于采用细胞模型、蛋白组学与代谢组学等多组学技术,实现了对PGRMC1功能的多维度解析,但局限性在于缺乏对不同磷酸化位点的系统性突变分析,尤其是表观遗传层面的调控机制研究,且未明确特定磷酸化位点与细胞可塑性的直接关联。
本文的创新价值在于首次系统解析PGRMC1 Y180等磷酸化位点突变对细胞代谢、基因组甲基化与突变率的调控效应,发现Y180位点突变可诱导细胞呈现胚胎干细胞样的高甲基化状态,填补了PGRMC1磷酸化修饰调控表观遗传与细胞可塑性的研究空白。通过与现有研究对比,本文明确了PGRMC1磷酸化状态的新功能——调控细胞表观遗传与基因组稳定性,为理解其在胚胎发育与肿瘤发生中的作用提供了新的视角。
3. 研究思路总结与详细解析
本文的研究目标是明确PGRMC1不同磷酸化位点对细胞代谢、基因组稳定性与表观遗传的调控机制,核心科学问题是PGRMC1磷酸化状态如何调控细胞可塑性相关的分子网络,技术路线遵循“突变体构建→表型筛选→多组学分析→机制验证”的闭环逻辑:首先构建PGRMC1野生型(WT)、S57A/S181A双突变体(DM)、S57A/Y180F/S181A三突变体(TM)的稳定表达MIA PaCa-2胰腺癌细胞系,然后通过高光谱成像、流式分析检测代谢与氧化还原状态,通过MTT法验证经典功能响应性,通过全基因组测序检测突变率,通过甲基化芯片分析表观遗传特征,最后通过代谢组学与基因敲低验证关键通路。
3.1 磷酸化突变体细胞系构建与验证
实验目的是获得稳定表达不同PGRMC1磷酸化突变体的胰腺癌细胞系,确保突变体表达水平一致以排除表达量差异的干扰。方法细节:将携带HA标签的WT、DM、TM PGRMC1质粒转染MIA PaCa-2细胞,采用潮霉素进行稳定株筛选,通过免疫印迹(Western blot)验证HA标签蛋白的表达水平,以β-肌动蛋白作为内参。结果解读:免疫印迹图显示,各突变体的PGRMC1-HA表达量与内源性PGRMC1相当,不同细胞系之间无显著差异(n=3,P>0.05),表明成功构建了表达水平一致的突变体细胞系。产品关联:实验所用关键产品:Qiagen的DNeasy Blood & Tissue Kit(货号69504)、Sigma-Aldrich的HA-Tag抗体(货号H3663)、Sigma-Aldrich的RIPA裂解液(货号R0278)。
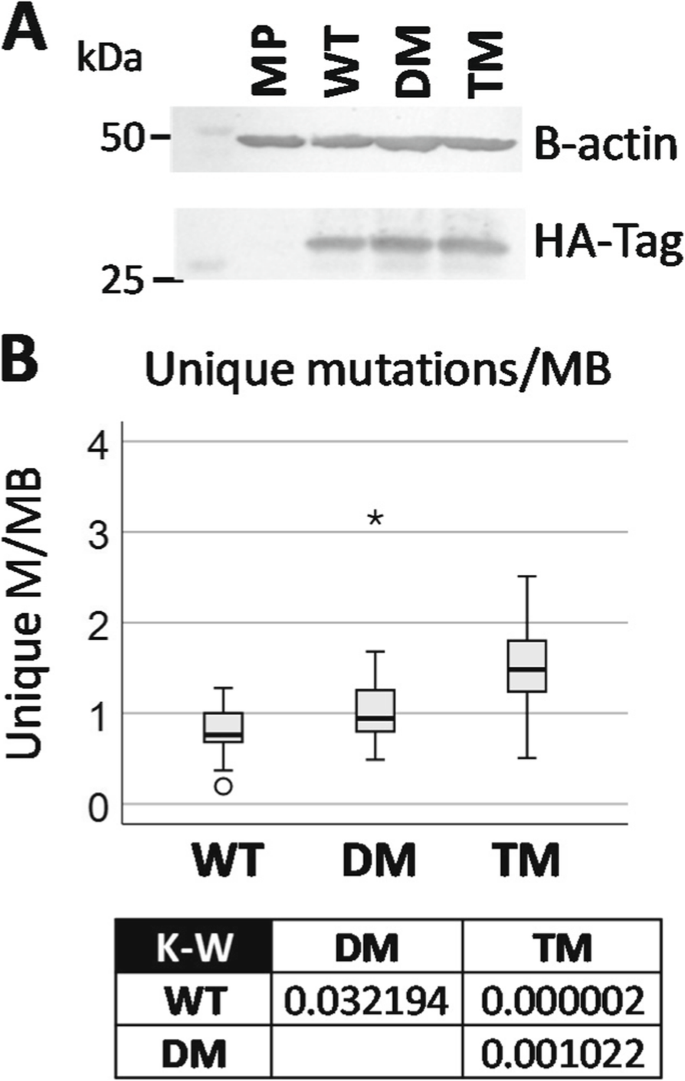
3.2 细胞代谢与氧化还原状态分析
实验目的是检测不同PGRMC1磷酸化突变体的细胞代谢状态差异,明确磷酸化位点对代谢的调控效应。方法细节:采用高光谱自发荧光成像技术,检测细胞内黄素(375nm激发/450nm发射)、血红素相关代谢物(495nm激发/700nm发射)的荧光信号;同时使用胞质氧化还原传感器NpFR1标记细胞,通过流式细胞术分析胞质氧化还原水平。结果解读:高光谱成像图显示,TM细胞的黄素荧光强度显著低于WT和DM细胞(n=300,P<0.001),血红素相关荧光信号也存在显著差异;流式分析图显示,TM细胞中处于高氧化状态的细胞比例最高(90.6%,n=3,P<0.01),且氧化程度显著高于其他组,提示PGRMC1磷酸化状态尤其是Y180位点可显著改变细胞代谢与氧化还原状态。产品关联:文献未提及具体实验产品,领域常规使用高光谱成像系统、流式细胞仪、氧化还原荧光探针等试剂/仪器。
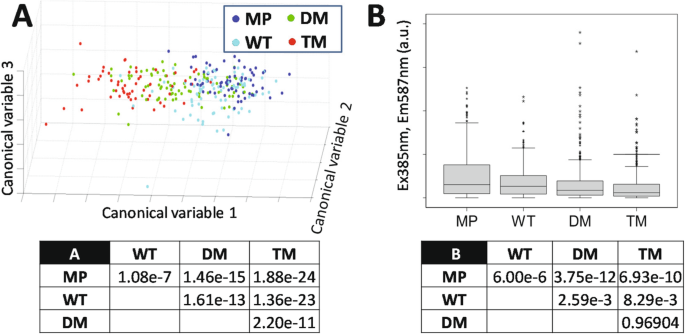
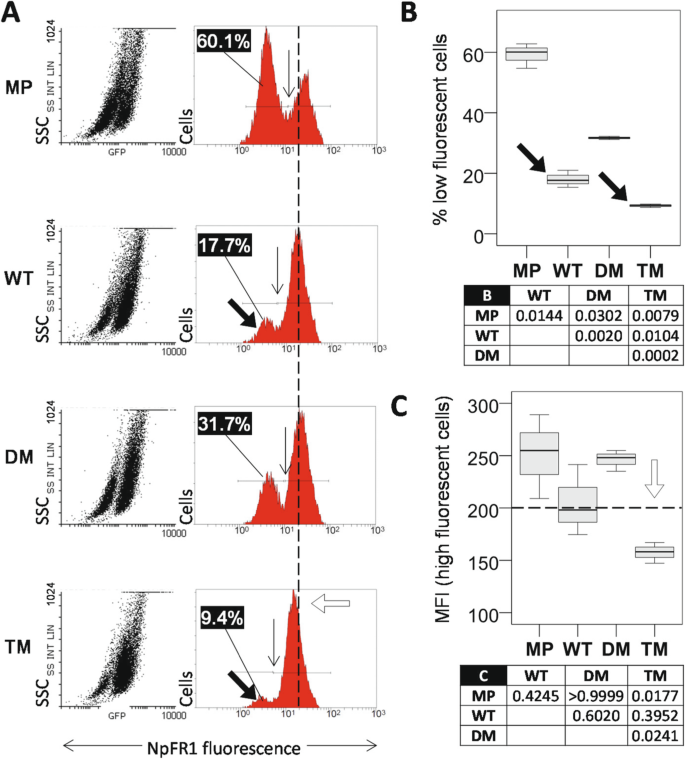
3.3 孕酮与AG-205功能响应性验证
实验目的是验证PGRMC1磷酸化突变是否影响其经典功能,包括孕酮依赖的阿霉素耐药性与AG-205敏感性。方法细节:采用MTT法,将细胞分为孕酮处理组与对照组,加入不同浓度的阿霉素或AG-205,培养24小时后检测细胞活力,计算细胞存活率与半数抑制浓度(EC50)。结果解读:MTT实验图显示,WT、DM、TM细胞均表现出孕酮依赖的阿霉素耐药性,且各突变体之间的耐药性无显著差异(n=6,P>0.05);AG-205处理后的细胞存活率曲线几乎重叠,EC50约为32μM(n=8,P>0.05),提示PGRMC1磷酸化突变不影响其经典的孕酮与AG-205响应功能,本文观察到的代谢与表观遗传变化属于新的调控功能。产品关联:实验所用关键产品:Sigma-Aldrich的MTT(货号M2128)、AG-205抑制剂、孕酮(P4)等。
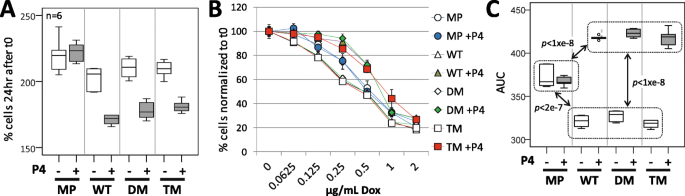
3.4 基因组稳定性与突变率分析
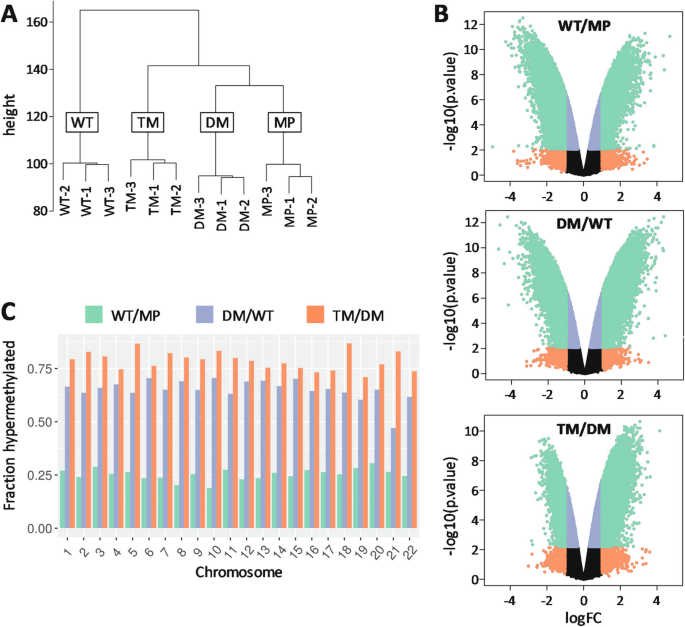
实验目的是解析PGRMC1磷酸化状态对基因组突变率的调控作用,明确其与肿瘤发生的潜在关联。方法细节:将WT、DM、TM细胞传代培养30次后,提取基因组DNA进行全基因组测序,以人类参考基因组为对照,统计各细胞系的每MB独特突变数。结果解读:全基因组测序图显示,TM细胞的每MB突变数显著高于WT和DM细胞,染色体水平的突变率排序为TM>DM>WT(n=23染色体,P<0.05),提示PGRMC1 Y180位点磷酸化状态可调控基因组稳定性,Y180突变可增加基因组突变率,可能参与肿瘤的发生发展。产品关联:实验所用关键产品:Qiagen的DNeasy Blood & Tissue Kit(货号69504)、Illumina的全基因组测序服务等。
3.5 基因组CpG甲基化特征分析
实验目的是检测PGRMC1磷酸化突变对基因组表观遗传的调控效应,明确其与细胞可塑性的关联。方法细节:提取传代10次的细胞基因组DNA,采用Illumina Infinium HD甲基化芯片(EPIC array)检测全基因组CpG甲基化水平,进行层次聚类、差异甲基化位点分析与通路富集。结果解读:甲基化芯片图显示,各突变体细胞系的甲基化模式呈现明显的聚类分离,TM细胞的整体CpG甲基化水平显著升高,类似胚胎干细胞的甲基化特征;差异甲基化位点富集于胚胎发育、细胞周期、ATM/ATR DNA损伤修复等通路(adjP<0.05),提示Y180位点突变可诱导细胞呈现干细胞样的表观遗传状态,调控细胞分化相关通路。产品关联:实验所用关键产品:Illumina的Infinium HD Methylation Assay(EPIC array)、Zymo的EZ DNA Methylation kit等。
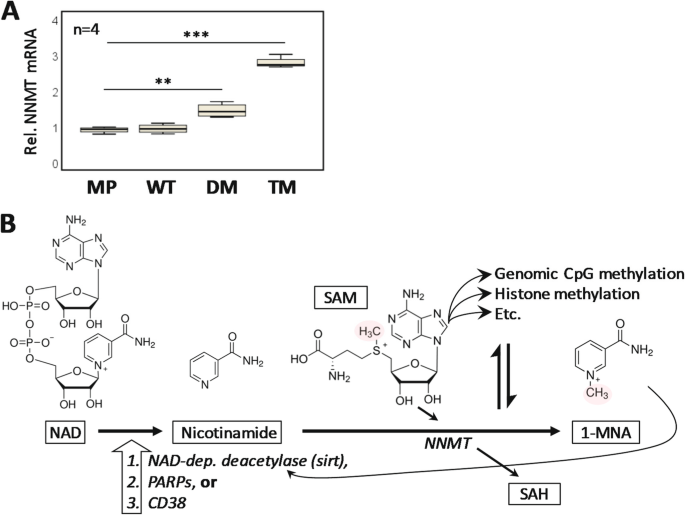
3.6 NNMT代谢通路机制验证
实验目的是解析PGRMC1磷酸化状态调控代谢与表观遗传的关联机制,明确关键代谢通路的作用。方法细节:采用qRT-PCR检测NNMT基因的表达水平,通过液相色谱-质谱(LC/MS)检测细胞内1-甲基烟酰胺(1-MNA)与S-腺苷甲硫氨酸(SAM)的含量,采用shRNA敲低TM细胞中的NNMT,验证其对代谢与甲基化的调控作用。结果解读:qRT-PCR图显示,TM细胞中NNMT的表达量较WT上调2.5倍(n=3,P<0.01);LC/MS结果显示TM细胞的1-MNA水平升高,SAM水平降低(n=12,P<0.05);shRNA敲低NNMT后,1-MNA水平显著降低(n=6,P<0.001),提示PGRMC1 Y180突变可通过上调NNMT通路影响甲基供体代谢,进而调控基因组甲基化状态。产品关联:实验所用关键产品:Bio-Rad的iTaq Universal SYBR Green Supermix(货号1725120)、Agilent的1290 Infinity HPLC系统、Sigma-Aldrich的1-MNA标准品等。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker包括PGRMC1的Y180磷酸化状态,以及关联的NNMT基因表达与基因组CpG甲基化特征,筛选与验证逻辑遵循“突变体筛选→细胞系验证→多组学分析→功能验证”的完整链条:首先通过突变体筛选发现Y180位点对表型的关键调控作用,然后在细胞系中验证其对代谢、甲基化与突变率的影响,最后通过代谢组学与基因敲低验证NNMT通路的介导作用。
Biomarker定位
PGRMC1 Y180磷酸化状态作为调控细胞可塑性的功能Biomarker,NNMT表达与基因组高甲基化状态作为关联的分子Biomarker。筛选逻辑基于PGRMC1磷酸化位点的进化保守性,Y180位点伴随后生动物的胚胎发育组织者一同进化,因此推测其在细胞分化中具有关键作用;验证逻辑通过细胞系突变体构建、多组学分析与功能实验,明确了Y180位点对代谢、表观遗传与基因组稳定性的调控效应。
研究过程详述
Biomarker的来源包括PGRMC1蛋白的Y180磷酸化位点、细胞内的NNMT基因转录本,以及基因组CpG甲基化位点。验证方法包括:通过定向突变构建Y180位点突变体,免疫印迹验证蛋白表达;全基因组测序检测基因组突变率;甲基化芯片检测全基因组CpG甲基化水平;qRT-PCR与LC/MS分别检测NNMT基因表达与代谢物含量。特异性数据显示,TM细胞与DM细胞仅Y180位点存在差异,却导致基因组甲基化水平升高1.2倍(n=850000 CpG位点,P<0.001),NNMT表达上调2.5倍(n=3,P<0.01);敏感性数据显示,Y180位点突变可使黄素荧光强度降低30%(n=300,P<0.001),胞质氧化水平升高25%(n=3,P<0.01),提示该Biomarker可显著调控细胞代谢与表观遗传状态。
核心成果提炼
该Biomarker的功能关联在于,PGRMC1 Y180磷酸化状态可通过调控NNMT通路影响甲基供体代谢,进而诱导细胞呈现胚胎干细胞样的高甲基化状态,调控细胞分化相关通路。创新性在于首次发现PGRMC1磷酸化状态与胚胎干细胞样表观遗传状态的关联,明确Y180位点是调控细胞可塑性的关键位点。统计学结果显示,TM细胞的每MB突变数较WT升高80%(n=23染色体,P<0.05),差异甲基化位点富集于胚胎发育通路的adjP<0.001,提示该Biomarker在胚胎发育与肿瘤发生中具有重要的调控作用,为后续开发针对PGRMC1磷酸化的靶向治疗策略提供了理论依据。
