1. 领域背景与文献引入
文献英文标题:On the effects of cycloheximide on cell motility and polarisation in Dictyostelium discoideum;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(盘基网柄菌细胞行为调控)
盘基网柄菌是研究细胞运动、内吞作用及信号通路时空调控的经典模式生物,领域共识:细胞运动与极化依赖细胞骨架重排、膜转运系统协同及信号分子的精准定位,其中内吞作用不仅参与细胞物质摄取,还通过膜循环过程维持细胞极性、调控信号转导效率。此前已有研究证实蛋白质合成抑制剂环己酰亚胺可快速抑制盘基网柄菌的液相内吞,但该抑制剂对细胞运动、极化及其他膜转运相关功能的影响尚未系统阐明,蛋白质合成与细胞运动、膜转运的潜在关联机制也未被揭示,存在明显研究空白。本研究针对这一领域空白,通过多维度实验解析环己酰亚胺对盘基网柄菌多种细胞功能的调控作用,为揭示蛋白质合成与细胞行为调控的关联机制提供关键实验依据。
2. 文献综述解析
作者围绕环己酰亚胺的作用机制、盘基网柄菌内吞与运动调控的现有研究展开综述,分类维度包括抑制剂作用靶点、细胞功能表型、分子调控通路三个层面。
已有研究证实环己酰亚胺通过特异性结合真核核糖体60S亚基抑制蛋白质合成,且早期研究发现其可快速抑制盘基网柄菌的液相内吞,推测存在不稳定蛋白参与内吞过程的调控;同时,NSF(N-乙基马来酰亚胺敏感因子)作为膜融合事件的关键调控因子,其功能缺失会导致盘基网柄菌细胞变圆、运动停止及内吞抑制,但NSF功能与蛋白质合成的关联尚未被关注。现有研究的优势在于明确了环己酰亚胺的作用靶点及内吞抑制的核心表型,局限性在于未系统探究其对细胞运动、极化、吞噬作用等其他关键细胞功能的影响,且未揭示蛋白质合成与膜转运、细胞运动之间的潜在调控关联。本研究的创新价值在于首次系统解析了环己酰亚胺对盘基网柄菌细胞运动、极化、吞噬作用、受体成帽等多种细胞功能的调控效应,并通过与NSF温度敏感突变体的表型对比,提出蛋白质合成与膜转运、细胞运动关联的两种潜在机制,填补了领域内该方向的研究空白。
3. 研究思路总结与详细解析
本研究的目标是明确环己酰亚胺对盘基网柄菌细胞运动、极化及膜转运相关功能的调控作用,核心科学问题是蛋白质合成如何通过分子机制调控细胞运动与极化过程,技术路线遵循“表型观察→功能验证→分子定位→突变体验证”的闭环逻辑,逐步解析环己酰亚胺的作用机制。
3.1 液相内吞与膜摄取功能检测
实验目的:验证环己酰亚胺对盘基网柄菌液相内吞及膜摄取过程的调控作用,明确其功能特异性。
方法细节:采用Ax2野生型盘基网柄菌菌株,以FITC-葡聚糖为液相内吞标记物,FM1-43为膜摄取标记物,设置0mM、2mM环己酰亚胺处理组,预处理30分钟后检测不同时间点的细胞荧光强度;同时通过共聚焦显微镜观察细胞形态与荧光分布特征。
结果解读:
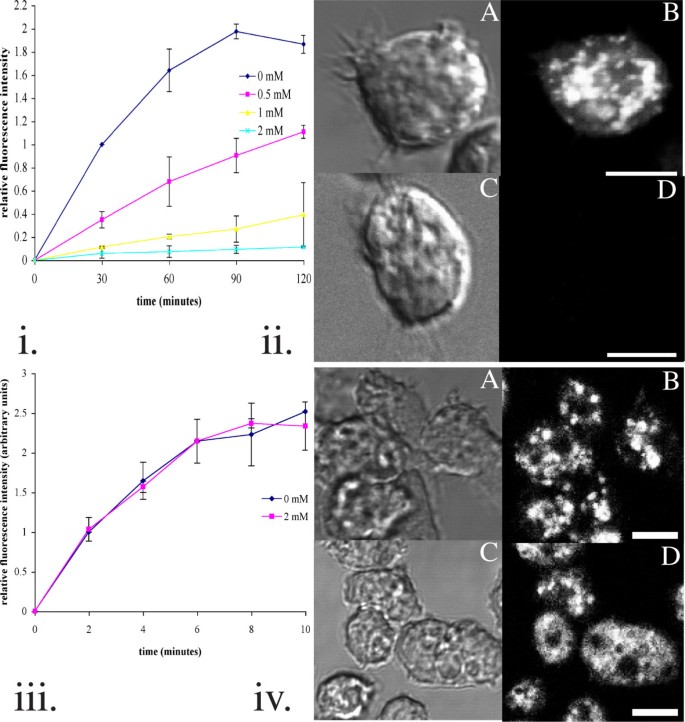
如图1所示,2mM环己酰亚胺处理可抑制超过95%的液相内吞(n=3,P<0.01),对照组细胞的液相内吞速率为0.029-0.15μl/1×10^7细胞/分钟,处理组降至0.38-1.7nl/1×10^7细胞/分钟;而膜摄取过程未受显著影响,细胞在环己酰亚胺处理后快速缩回伪足、呈现圆形形态。这表明环己酰亚胺特异性抑制液相内吞过程,但不影响膜的内吞循环。
产品关联:文献未提及具体实验产品,领域常规使用FITC-葡聚糖、FM1-43荧光染料、激光共聚焦显微镜等试剂与仪器。
3.2 吞噬作用与受体成帽功能检测
实验目的:探究环己酰亚胺对盘基网柄菌吞噬作用及细胞表面受体重排的影响,解析其对细胞运动相关功能的调控。
方法细节:以1μm羧基修饰荧光微球为吞噬底物,检测不同浓度环己酰亚胺处理后细胞的微球摄取量;采用荧光标记的刀豆蛋白A(Con A)交联细胞表面受体,观察受体成帽现象的发生比例。
结果解读:
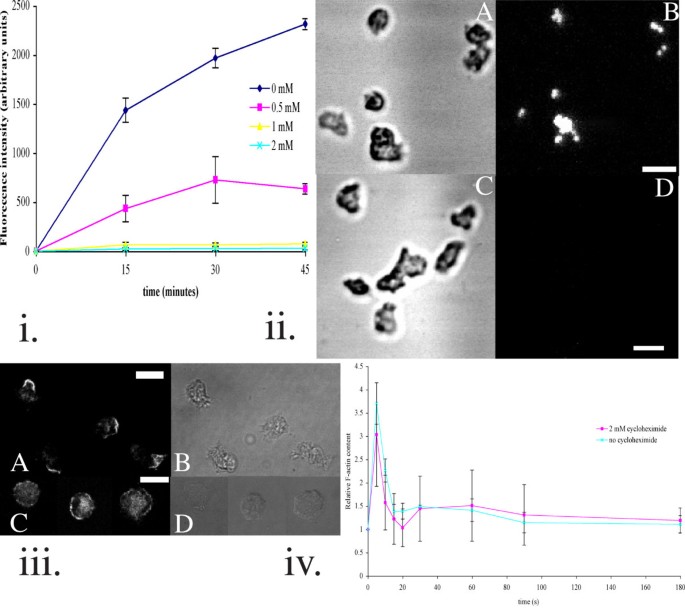
如图2所示,1mM环己酰亚胺处理可完全抑制吞噬作用(n=3,P<0.001),对照组细胞30分钟内平均吞噬3-4个微球,处理组细胞几乎无微球摄取;同时,99%的环己酰亚胺处理细胞无法形成Con A受体成帽(n=140),而对照组约90%的细胞可形成典型的受体成帽(n=200)。这表明环己酰亚胺可抑制吞噬作用与受体成帽过程,影响细胞运动依赖的表面受体重排功能。
产品关联:文献未提及具体实验产品,领域常规使用荧光微球、荧光标记刀豆蛋白A等试剂。
3.3 细胞运动与极化信号分子定位检测
实验目的:解析环己酰亚胺对盘基网柄菌细胞运动能力及趋化信号诱导的极化分子定位的影响,探究其作用的分子层面机制。
方法细节:采用聚集态盘基网柄菌,通过微管施加cAMP趋化因子,利用图像分析软件检测对照组与环己酰亚胺处理组的细胞运动速度与持续性;利用GFP/CFP标记的CRAC、PI3K、ABP120及肌动蛋白,观察信号分子在趋化刺激下的时空定位变化。
结果解读:
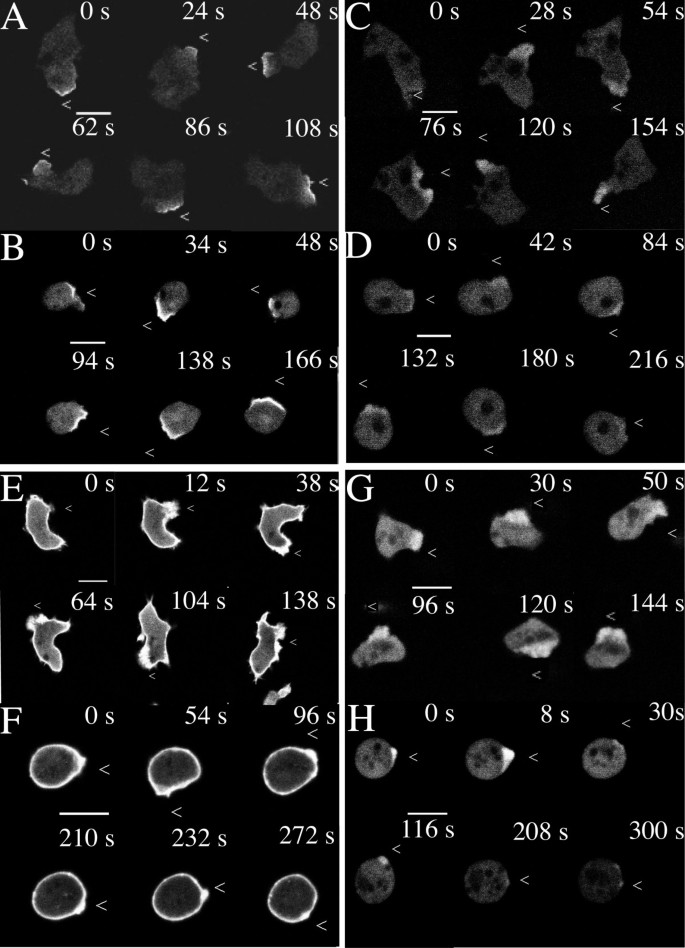
如图3所示,对照组细胞向cAMP源运动的平均速度为12.8±4.6μm/分钟(n=30),运动持续性为0.74±0.28;环己酰亚胺处理组细胞平均运动速度降至1.2±0.54μm/分钟(n=38,P<0.001),持续性降至0.39±0.36。尽管细胞形态变圆,但CRAC、PI3K、ABP120及肌动蛋白仍可向cAMP源方向定位,且肌动蛋白聚合的动力学特征与对照组无显著差异。这表明环己酰亚胺主要抑制细胞的运动执行能力,但不影响趋化信号诱导的极化信号分子定位与肌动蛋白聚合过程。
产品关联:实验所用关键产品:GFP标记的CRAC、CFP标记的PI3K、GFP标记的ABP120、GFP标记的肌动蛋白(由Peter Devreotes、David Knecht等实验室提供)。
3.4 环己酰亚胺抗性突变体验证
实验目的:验证环己酰亚胺的作用靶点为核糖体,排除非特异性作用对实验结果的干扰。
方法细节:采用环己酰亚胺抗性突变株HH31,检测其在2mM环己酰亚胺处理下的液相内吞功能与细胞运动、形态表型,与野生型菌株进行对比。
结果解读:抗性突变株在环己酰亚胺处理后,液相内吞功能未受抑制,细胞仍保持正常的运动能力与梭形形态,无变圆表型出现。这表明环己酰亚胺的作用靶点为核糖体,通过抑制蛋白质合成调控细胞的多种功能表型。
产品关联:文献未提及具体实验产品,领域常规使用模式生物突变株库资源。
4. Biomarker研究及发现成果
本研究未聚焦传统疾病诊断或预后类生物标志物,而是揭示了蛋白质合成过程在盘基网柄菌细胞运动、极化及膜转运中的核心调控作用,提出了两种潜在的调控模式,为真核细胞功能调控机制研究提供了新的视角。
Biomarker定位:本研究中的核心调控靶点为真核核糖体60S亚基,筛选与验证逻辑为通过环己酰亚胺抗性突变株的表型对比,验证其特异性作用靶点,结合多维度功能实验揭示其调控的细胞功能网络。研究过程详述:通过对比野生型与抗性突变株在环己酰亚胺处理下的液相内吞、细胞运动、形态等表型,证实核糖体60S亚基为环己酰亚胺的特异性作用靶点;通过液相内吞、膜摄取、吞噬作用、受体成帽、细胞运动及信号分子定位等多维度实验,明确蛋白质合成抑制可导致液相内吞、吞噬作用、受体成帽及细胞运动的抑制,但不影响膜摄取、趋化信号分子定位及肌动蛋白聚合过程。核心成果提炼:本研究首次系统阐明了环己酰亚胺对盘基网柄菌多种细胞功能的调控效应,揭示了蛋白质合成与细胞运动、膜转运过程的潜在关联,提出两种可能的调控机制:一是参与极化膜循环的不稳定蛋白因合成抑制而降解,导致细胞功能丧失;二是细胞存在蛋白质合成与膜转运关联的调控机制,蛋白质合成抑制激活该调控通路导致细胞功能变化。本研究未涉及临床相关的特异性、敏感性数据,所有实验数据均基于模式生物的功能验证结果。
