1. 领域背景与文献引入
文献英文标题:Multiple immunofluorescence labelling of formalin-fixed paraffin-embedded (FFPE) tissue;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:组织病理学与细胞生物学交叉领域,聚焦FFPE组织的免疫荧光标记技术优化。
组织病理学是现代临床诊断和转化医学研究的核心支柱,福尔马林固定石蜡包埋(FFPE)是临床组织样本的主要保存形式,具有形态结构保存完好、样本存档量大、可长期保存的优势,是连接基础研究与临床实践的重要资源。传统免疫组化(IHC)是FFPE组织标记的主流技术,其优势在于方法稳定可靠、可实现自动化操作,但作为研究工具存在三大核心局限:一是一次仅能标记一种蛋白质,多色标记效果不佳,无法精准分析两种抗原在同一亚细胞结构中的共定位;二是抗原定位分辨率受限,显色底物的沉淀效应及3-4μm的切片厚度导致亚细胞结构观察模糊;三是显色系统易饱和,限制了半定量分析的准确性。
免疫荧光标记技术虽具备多色标记、高分辨率的优势,但长期以来多用于新鲜冰冻切片,FFPE组织因存在自发荧光强、抗原修复难度大等问题,高质量免疫荧光标记难以常规开展,导致临床大量存档FFPE样本无法用于更精细的细胞生物学研究,比如多标志物共表达分析、亚细胞定位研究等,形成了基础细胞生物学研究与临床病理样本资源之间的技术壁垒。针对这一研究空白,本研究旨在开发一种稳定、高效的FFPE组织多色免疫荧光标记方法,结合共聚焦激光扫描显微镜,突破现有技术的局限,为充分利用FFPE样本资源开展深入研究提供技术支撑。
2. 文献综述解析
作者从现有FFPE组织蛋白质标记技术的两大类别(免疫组化与免疫荧光)入手,对比两类技术的优缺点,进而回顾此前报道的FFPE组织免疫荧光标记方法,分析其未被广泛应用的原因,最终凸显本研究方法的创新性与必要性。
传统免疫组化技术的核心优势在于方法成熟、稳定性高,可实现标记、图像采集与评分的自动化,是临床诊断的标准方法,但存在单标记限制、分辨率低、半定量分析受限的固有缺陷。此前已有多个研究团队尝试开发FFPE组织的免疫荧光标记方法,但这些方法未被科研界广泛采用,主要原因包括使用旧一代荧光染料(如异硫氰酸荧光素FITC、罗丹明等),荧光稳定性差、亮度低;采用普通荧光显微镜,无法有效控制FFPE组织的自发荧光;部分方法依赖复杂的图像分析系统,操作门槛高。此外,现有高通量FFPE免疫荧光检测系统虽能实现批量样本分析,但缺乏高分辨率的多色标记能力,无法满足亚细胞定位与多标志物共表达的研究需求。
与现有研究相比,本研究的核心创新在于整合了抗原修复优化、间接免疫荧光标记与共聚焦激光扫描显微镜技术,有效解决了FFPE组织自发荧光的问题,实现了高质量的多色免疫荧光标记;同时,本研究验证了标记后样本的长期保存稳定性,为样本的重复使用提供了依据;此外,该方法操作流程标准化,可常规应用于不同类型的FFPE组织样本(正常组织、肿瘤组织、组织芯片),填补了传统免疫组化、冰冻切片免疫荧光与高通量FFPE免疫荧光检测之间的技术空白,打通了细胞生物学研究与临床病理样本资源之间的壁垒。
3. 研究思路总结与详细解析
本研究的核心目标是开发并验证一种适用于FFPE组织的高质量多色免疫荧光标记方法,核心科学问题是如何克服FFPE组织自发荧光、抗原修复不完全等技术难点,实现稳定、高分辨率的多标志物共表达分析;技术路线遵循“方法优化→多类型样本验证→保存稳定性评估→结论总结”的闭环逻辑,通过系统优化实验流程,结合共聚焦显微镜的高分辨率成像能力,全面验证方法的可靠性与适用性。
3.1 实验方法体系优化
实验目的:建立FFPE组织免疫荧光标记的标准化操作流程,解决脱蜡不彻底、抗原修复不足、非特异性染色、自发荧光干扰等关键技术问题。
方法细节:以FFPE组织为起始材料,样本经10%中性缓冲福尔马林固定过夜,常规石蜡包埋后切取3-4μm切片;脱蜡步骤根据切片情况调整二甲苯处理时间(未包蜡切片为2×5分钟,重包蜡切片为2×20分钟),随后经梯度乙醇水化;抗原修复采用Dako靶标修复液,95℃水浴处理30分钟,室温放置20分钟后流水冲洗5分钟;免疫荧光标记时,先用ImmEdge笔圈定样本区域,加入免疫荧光缓冲液(含1%牛血清白蛋白与2%胎牛血清)封闭,一抗按优化浓度室温孵育60分钟或4℃过夜,PBS洗涤3次(每次5分钟)后,加入2μg/ml的AlexaFluor系列二抗室温孵育60分钟,再经含DAPI的PBS洗涤复染细胞核,最后用Vectashield封片剂封片,指甲油密封边缘。
结果解读:通过各步骤的系统优化,成功实现了FFPE组织的特异性免疫荧光标记,非特异性背景染色可忽略,标记灵敏度与传统免疫组化(采用Vector Laboratories的Vectastain avidin-biotin complex系统)相当(文献未明确提供具体定量数据,基于图表趋势推测)。
产品关联:实验所用关键产品:Vector Laboratories的Vectastain avidin-biotin complex(ABC)系统、ImmEdge笔(H-4000)、Vectashield封片剂(H-1000);Dako的靶标修复液(S1699);Invitrogen的AlexaFluor系列二抗、DAPI(D21490)、胎牛血清;Sigma的牛血清白蛋白(A3059);Leica SP2共聚焦激光扫描显微镜。
3.2 人肾脏组织标记验证
实验目的:验证优化后的方法在正常组织样本中的多色标记能力,评估其对蛋白质亚细胞定位与共表达模式的分析精度。
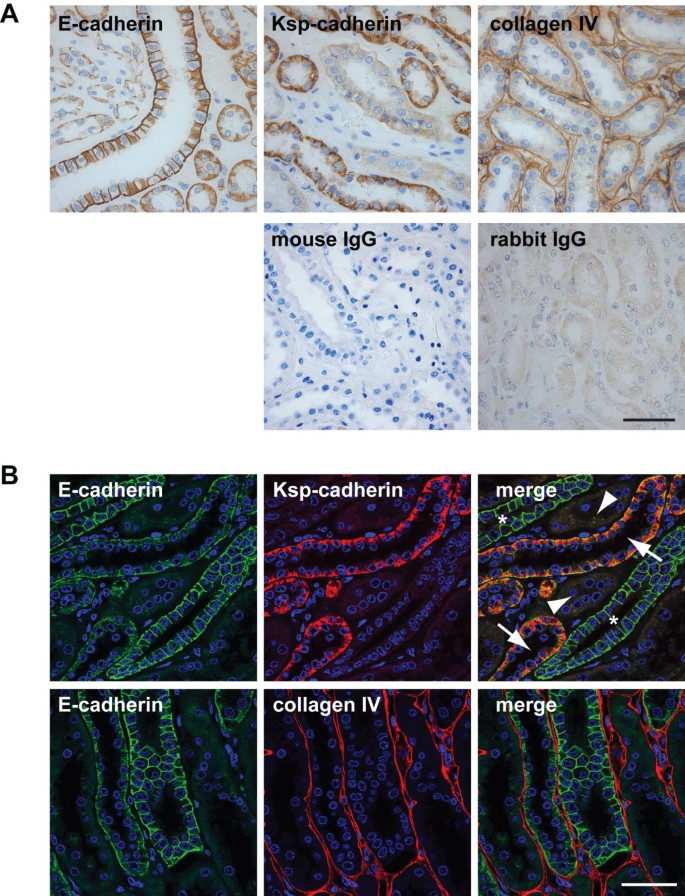
方法细节:取成人肾脏FFPE切片,经脱蜡、抗原修复后,分别进行传统免疫组化标记(E-钙粘蛋白、Ksp-钙粘蛋白、IV型胶原)和免疫荧光双标记(E-钙粘蛋白与Ksp-钙粘蛋白、E-钙粘蛋白与IV型胶原),采用共聚焦激光扫描显微镜采集0.5μm厚度的光学切片图像。
结果解读:传统免疫组化仅能显示不同肾小管中钙粘蛋白的差异表达,而免疫荧光双标记结合共聚焦的薄光学切片,清晰揭示出三种肾小管亚型:同时表达E-钙粘蛋白与Ksp-钙粘蛋白、仅表达E-钙粘蛋白、两种钙粘蛋白均不表达;同时,该方法可清晰呈现抗原的亚细胞分布特征,分辨率显著高于传统免疫组化,充分体现了高分辨率成像的优势。
3.3 乳腺组织及乳腺癌样本标记验证
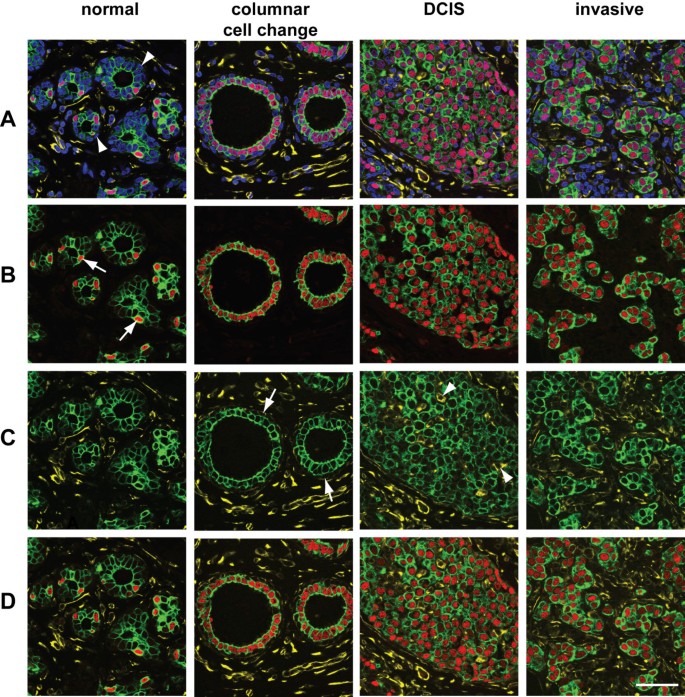
实验目的:验证方法在正常乳腺、癌前病变及肿瘤组织中的四色标记能力,评估其对复杂组织中细胞异质性的分析能力。
方法细节:取包含正常乳腺组织、柱状细胞改变、导管原位癌(DCIS)及浸润性导管癌的FFPE切片,采用抗细胞角蛋白8/18单克隆抗体、抗波形蛋白单克隆抗体、抗雌激素受体(ER)抗体进行免疫荧光标记,分别搭配Alexa488、Alexa633、Alexa555标记的二抗,DAPI复染细胞核,共聚焦显微镜采集四色荧光图像。
结果解读:四色荧光图像清晰显示,正常乳腺组织中ER仅在高表达细胞角蛋白8/18的腔上皮细胞中表达,波形蛋白则局限于基质成纤维细胞与肌上皮细胞;柱状细胞改变区域的肌上皮细胞中波形蛋白表达上调;DCIS区域存在波形蛋白阳性、细胞角蛋白8/18阴性的细胞群,精准呈现了不同细胞群的标志物表达模式,为分析组织细胞异质性提供了高分辨率的可视化数据。
3.4 乳腺肿瘤组织芯片标记验证
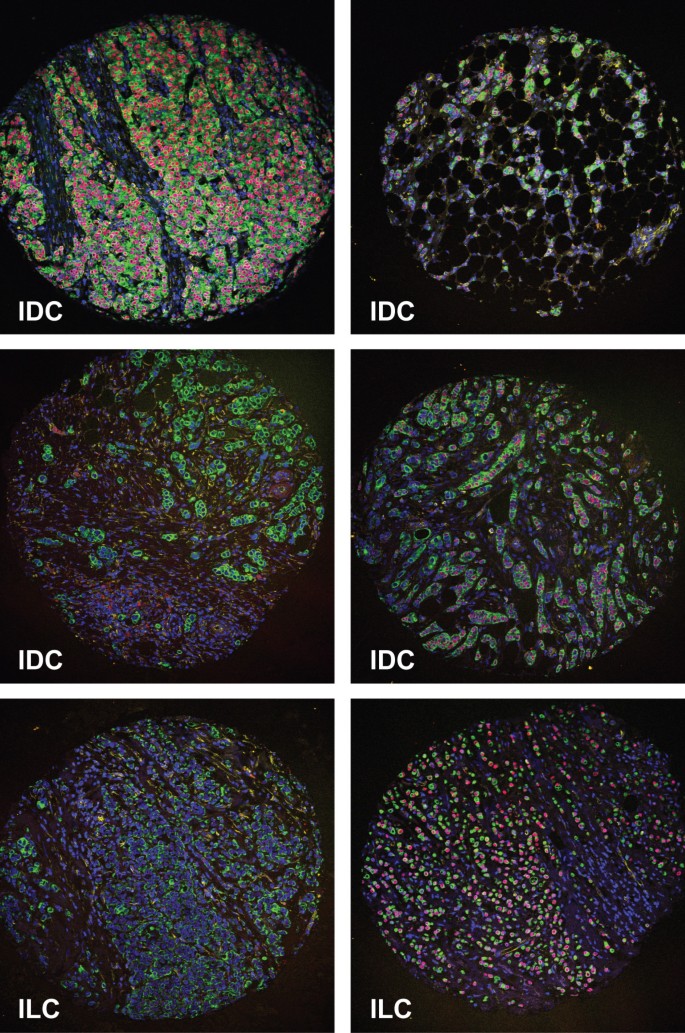
实验目的:验证方法在高通量临床样本中的适用性,评估其在大样本转化研究中的应用价值。
方法细节:采用包含245例浸润性乳腺癌样本的组织芯片(每芯直径0.6mm),使用与乳腺组织验证相同的抗体组合及标记流程进行免疫荧光标记,共聚焦显微镜采集图像。
结果解读:从组织芯片的不同样本芯中均获得了高质量的四色荧光图像,标记信号特异性强、背景低,说明该方法可稳定应用于大样本FFPE组织芯片的多色免疫荧光标记,满足转化医学研究中高通量样本分析的需求。
3.5 标记后样本保存稳定性验证
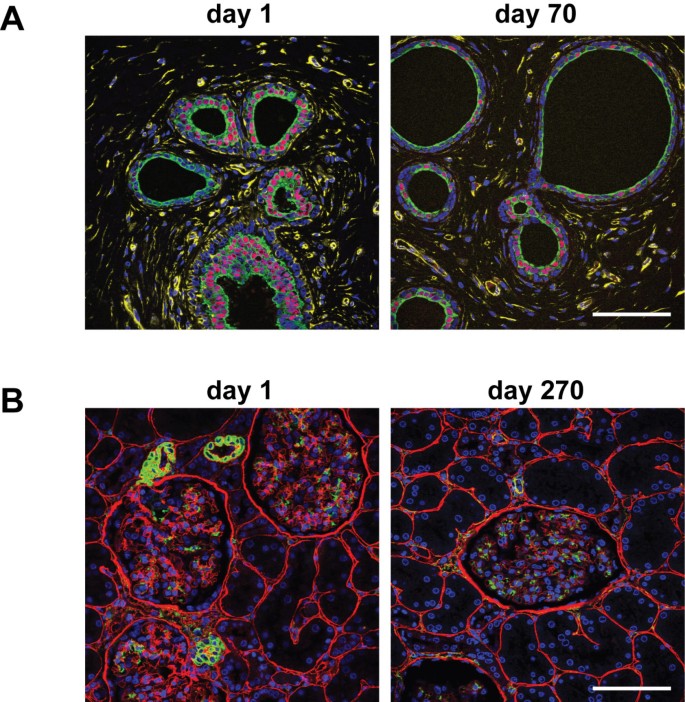
实验目的:评估免疫荧光标记后FFPE切片的保存期限,为样本的长期存储与重复使用提供实验依据。
方法细节:将标记后的乳腺柱状细胞改变FFPE切片在4℃保存10周,标记后的肾脏FFPE切片在-20℃保存9个月,分别在保存后用共聚焦显微镜采集图像,与标记后立即采集的图像进行对比。
结果解读:4℃保存10周、-20℃保存9个月的切片,荧光信号仅出现可忽略的衰减,图像质量与新鲜标记的样本无显著差异(文献未明确提供荧光强度定量数据,基于图表趋势推测),说明标记后的样本可长期保存,便于后续重复观察与分析。
4. Biomarker研究及发现成果解析
本研究的核心成果并非发现新的生物标志物(Biomarker),而是开发了一种可用于FFPE组织中多Biomarker精细分析的技术方法,该方法突破了传统技术的局限,为临床FFPE样本中已知Biomarker的验证、共表达分析及功能研究提供了更强大的工具支撑。
Biomarker定位:本研究以组织特异性已知Biomarker为研究对象,包括肾小管标记物(E-钙粘蛋白、Ksp-钙粘蛋白)、基底膜标记物(IV型胶原)、乳腺上皮标记物(细胞角蛋白8/18)、激素受体标记物(雌激素受体ER)、间质细胞标记物(波形蛋白),验证逻辑为“已知Biomarker→FFPE组织标记优化→共聚焦显微镜验证表达模式与共定位”,完整覆盖了从方法建立到临床样本应用的全流程。
研究过程详述:Biomarker来源为临床FFPE组织样本,包括正常成人肾脏组织、正常乳腺及乳腺癌组织、245例浸润性乳腺癌组织芯片;验证方法为优化后的间接免疫荧光标记结合共聚焦激光扫描显微镜检测,通过同型对照抗体验证了标记的特异性,敏感性与传统免疫组化相当(文献未明确提供ROC曲线、敏感性、特异性等定量数据);样本量方面,组织芯片样本量为245例(n=245),保存稳定性实验设置了10周(4℃)和9个月(-20℃)两个时间点。
核心成果提炼:该技术方法的创新性在于首次建立了稳定、可常规开展的FFPE组织多色免疫荧光标记流程,结合共聚焦显微镜实现了高分辨率的Biomarker亚细胞定位与共表达分析;功能关联方面,该方法可用于临床FFPE样本中Biomarker的精细分析,比如乳腺癌中ER、细胞角蛋白、波形蛋白的共表达模式,有助于更准确地定义肿瘤细胞异质性,为Biomarker的临床应用提供更精准的依据;统计学结果方面,未提供具体P值、置信区间等数据,但组织芯片大样本验证证明了方法的稳定性与适用性。
