1. 领域背景与文献引入
文献英文标题:The chromatin reader Dido3 is a regulator of the gene network that controls B cell differentiation;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:免疫血液学(B细胞分化与表观遗传调控)
B细胞作为适应性免疫的核心效应细胞,其发育过程从造血干细胞(HSC)启动,历经多能祖细胞(MPP)、淋系定向祖细胞(LMPP)、共同淋系祖细胞(CLP)等多个阶段,最终分化为成熟B细胞,该过程依赖关键转录因子的时序性激活与沉默,以及免疫球蛋白基因的V(D)J重排。领域共识:表观遗传调控尤其是组蛋白修饰的识别与解读,在细胞命运决定中发挥核心作用,组蛋白修饰阅读器可通过结合特定组蛋白标记调控染色质结构与基因表达。当前研究热点聚焦于表观调控因子在造血细胞分化中的具体机制,以及其在血液系统疾病中的潜在治疗价值,但Dido家族成员Dido3作为组蛋白H3K4me2/3的阅读器,其在B细胞分化中的功能与调控机制尚未明确,现有研究仅报道了Dido3缺失对胚胎干细胞分化的影响,缺乏在造血系统尤其是B细胞谱系中的深入探究,这一空白限制了对B细胞发育表观调控网络的全面理解。本文旨在通过条件性基因敲除小鼠模型结合多组学技术,解析Dido3在B细胞分化中的关键作用及分子机制,为B细胞发育异常相关疾病的治疗提供新的靶点与理论依据。
2. 文献综述解析
作者围绕B细胞发育的调控网络与表观遗传机制展开综述,以“B细胞发育阶段-关键调控事件-表观调控因子功能”为分类维度,系统梳理了现有研究进展与未解决问题。
现有研究明确了B细胞发育各阶段的核心标志与关键事件,如CLP阶段启动免疫球蛋白重链的DH-JH重排,pre-B阶段依赖pre-BCR信号完成发育检查点,同时证实了E蛋白(如E2A、HEB)、Ebf1等转录因子在B细胞命运决定中的核心作用,以及PRC2复合物通过H3K27me3修饰调控发育基因的沉默。技术方法上,流式细胞术与细胞分选技术为B细胞亚群的精准分析提供了支持,多组学技术的应用也推动了表观调控网络的解析,但现有研究存在局限性:一是缺乏对Dido3这类组蛋白阅读器在B细胞分化中功能的研究,二是未明确Dido3与PRC2复合物及E蛋白调控网络的关联,三是对B细胞发育中染色质可及性变化与转录调控的耦合机制解析不足。本文的创新价值在于首次聚焦Dido3在B细胞分化中的作用,通过条件性敲除模型结合多组学技术,揭示了Dido3通过调控PRC2活性与E蛋白表达维持B细胞正常发育的机制,填补了表观调控因子在B细胞分化研究中的空白,为血液系统疾病的表观治疗提供了新的视角。
3. 研究思路总结与详细解析
本研究的核心目标是明确Dido3在B细胞分化中的功能与分子机制,核心科学问题为“Dido3如何通过表观调控网络影响B细胞发育的关键阶段”,技术路线遵循“模型构建→表型分析→多组学解析→机制验证”的闭环逻辑,通过条件性Dido3缺失小鼠模型观察B细胞发育缺陷,结合转座酶可及性染色质测序(ATAC-seq)、转录组测序(RNA-seq)、染色质免疫沉淀测序(ChIP-seq)解析染色质可及性、基因表达与组蛋白修饰的变化,最终验证关键调控基因的功能。
3.1 条件性Dido3缺失小鼠模型构建与造血系统表型分析
实验目的:构建Dido3条件性缺失小鼠模型,明确Dido3在体内造血系统尤其是B细胞发育中的作用。
方法细节:将携带Dido1基因E16外显子loxP位点的小鼠与Vav1-Cre转基因小鼠杂交,获得造血系统特异性缺失Dido3 C端的Dido1∆E16小鼠,以同窝野生型(WT)小鼠为对照,选取6-10周龄性别匹配的小鼠,通过血常规分析外周血细胞计数,流式细胞术分析骨髓造血干祖细胞及B细胞亚群的数量与比例。
结果解读:血常规显示Dido1∆E16小鼠白细胞数量降至WT的33%,淋巴细胞亚群中B220+细胞减少95%(n=14,P<0.0001);流式分析显示骨髓LSK细胞绝对数量显著降低(WT n=9,Dido1∆E16 n=9,P<0.01),B细胞亚群中pre-B与未成熟B细胞数量显著减少(WT n=13,Dido1∆E16 n=11,P<0.0001),提示Dido3缺失导致B细胞发育阻滞在pre-B阶段。
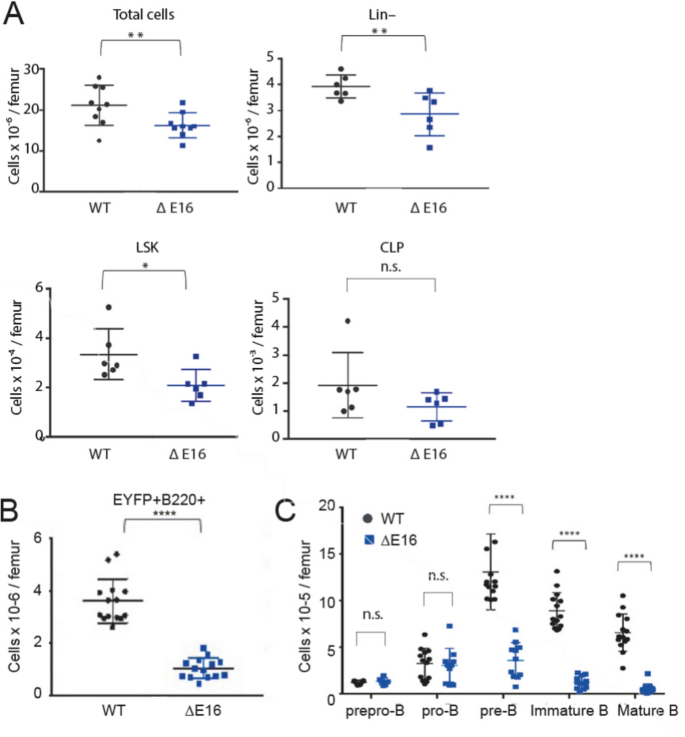
产品关联:实验所用关键产品:eBioscience的B220-eF450等抗体、Beckman Coulter的Gallios流式细胞仪、BD FACSAria Fusion分选仪、STEMCELL Technologies的EasySep小鼠造血祖细胞分离试剂盒等。
3.2 B细胞发育阶段的凋亡与增殖分析
实验目的:探究Dido3缺失导致B细胞发育阻滞的细胞生物学机制,分析凋亡与增殖的变化。
方法细节:采用流式细胞术结合Annexin V与DAPI染色,检测骨髓B细胞亚群的凋亡水平;通过腹腔注射BrdU,18小时后检测BrdU掺入率分析细胞增殖能力,同时进行体外半固体培养基培养分析B细胞前体的分化能力。
结果解读:Annexin V染色显示Dido1∆E16小鼠未成熟B细胞的凋亡率显著升高(n=3,P<0.05),Annexin V平均荧光强度从WT的13.41升至22.9;BrdU掺入实验显示未成熟B细胞的S期比例升高,但增殖能力无显著差异,提示未成熟B细胞存在S期阻滞并最终凋亡;体外培养中Dido1∆E16小鼠的lin-细胞无法形成CFU-pre-B集落,进一步证实B细胞前体的分化能力缺陷。
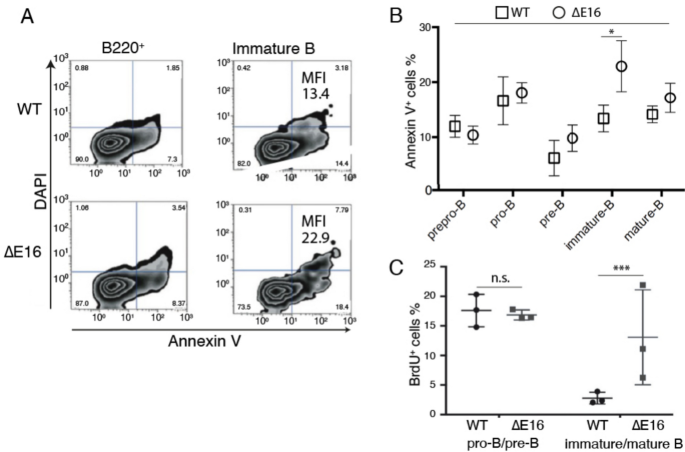
产品关联:实验所用关键产品:Invitrogen的BrdU染色试剂盒、Immunostep的Annexin V-APC、STEMCELL Technologies的Methocult培养基3630等。
3.3 多组学测序与生物信息学分析
实验目的:解析Dido3缺失导致B细胞发育缺陷的表观遗传与转录调控机制。
方法细节:分选WT与Dido1∆E16小鼠的骨髓LSK细胞与pre-B细胞,分别进行转座酶可及性染色质测序(ATAC-seq)、转录组测序(RNA-seq)、染色质免疫沉淀测序(ChIP-seq)检测H3K27me3修饰,通过生物信息学分析差异可及区域、差异表达基因与组蛋白修饰变化,结合GSEA、STRING、Metascape等工具进行功能富集与网络分析。
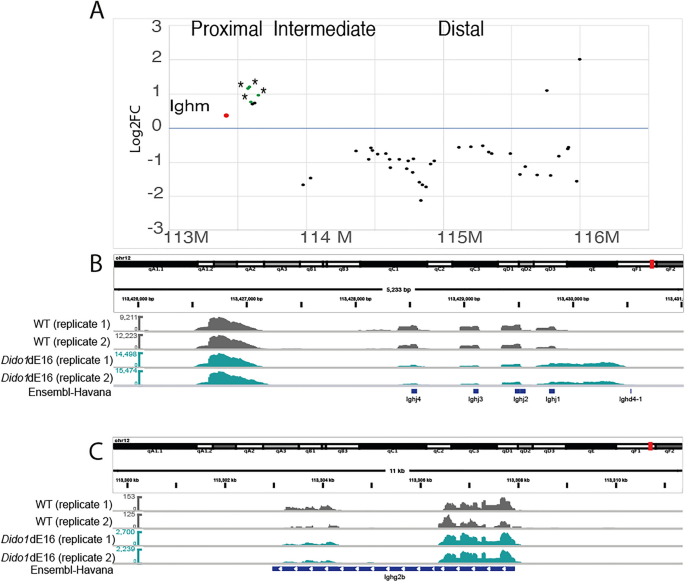
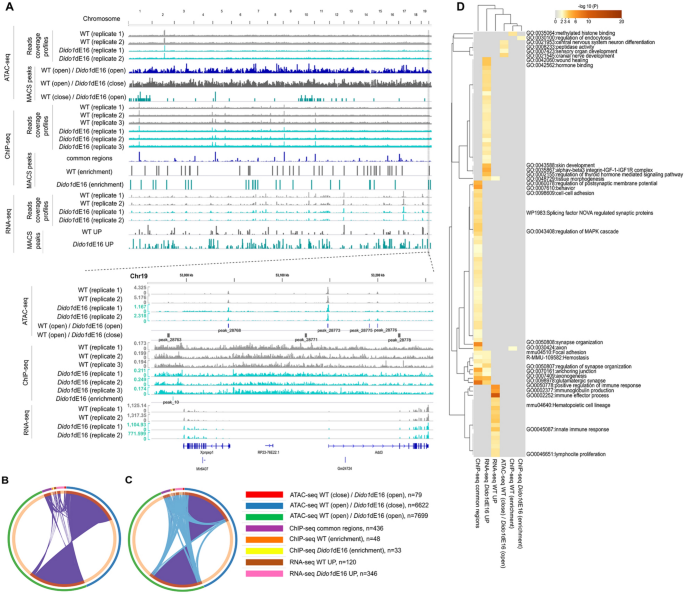
结果解读:ATAC-seq分析显示Dido1∆E16小鼠LSK细胞中PRC2靶基因的启动子区域染色质可及性降低,GSEA富集到PRC2复合物靶基因集(p=2.66×10^-57);RNA-seq分析显示pre-B细胞中120个基因下调、346个基因上调,其中PRC2靶基因显著下调,免疫球蛋白重链的近端V片段过度表达而远端V片段表达不足;ChIP-seq分析显示Dido1∆E16小鼠LSK细胞中58个区域的H3K27me3修饰显著低于WT,涉及B细胞分化相关基因。
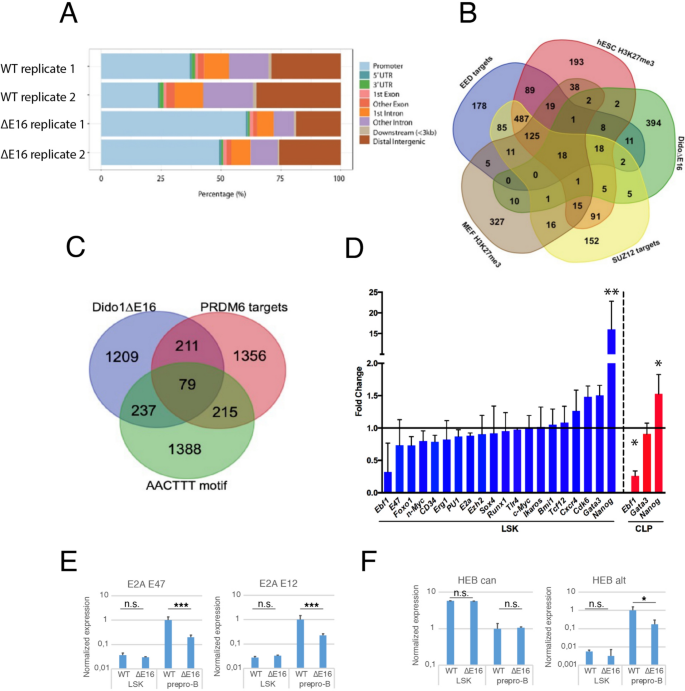
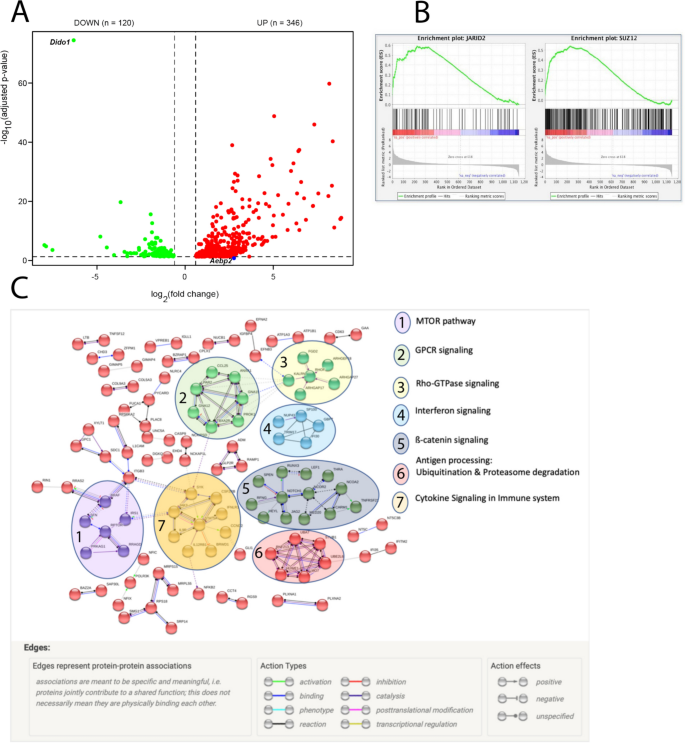

产品关联:实验所用关键产品:Qiagen的RNeasy Plus Mini Kit、Invitrogen的SuperScriptIII反转录试剂盒、Applied Biosystems的ABI PRISM 7900HT qPCR系统、DIAGENODE的True MicroChIP-seq Kit、Illumina的测序平台等。
3.4 关键基因表达验证与调控机制关联
实验目的:验证多组学分析结果,明确Dido3调控B细胞分化的关键基因与通路。
方法细节:采用实时荧光定量PCR(qRT-PCR)检测LSK细胞与CLP细胞中关键转录因子的表达,设计特异性引物检测Tcf3与Tcf12的不同亚型表达。
结果解读:qRT-PCR验证显示Dido1∆E16小鼠LSK细胞中Nanog表达上调16倍(n=4,P<0.01),Ebf1表达显著降低,Tcf12的HEBalt亚型在prepro-B细胞中仅为WT的10%(n=4,P<0.001),提示Dido3通过调控Nanog-Ebf1轴及HEBalt亚型的表达,影响B细胞的命运决定与发育进程。
产品关联:实验所用关键产品:Qiagen的RNeasy Plus Mini Kit、Applied Biosystems的SYBR Green qPCR Master Mix等。
4. Biomarker研究及发现成果解析
本文中涉及的Biomarker主要为B细胞分化调控的关键表观与转录标志物,包括组蛋白H3K27me3修饰位点、Ebf1、Tcf12的HEBalt亚型及Nanog,筛选与验证逻辑遵循“多组学筛选→细胞水平验证→功能关联分析”的完整链条。
Biomarker的来源为WT与Dido1∆E16小鼠的骨髓LSK细胞与pre-B细胞,验证方法包括染色质免疫沉淀测序检测H3K27me3修饰、实时荧光定量PCR检测基因表达、流式细胞术检测细胞亚群标志。特异性与敏感性数据方面,H3K27me3修饰在PRC2靶基因启动子区域的差异富集具有统计学意义(如WT vs Dido1∆E16的58个区域P<0.05),Ebf1在CLP细胞中的表达降低具有显著性(n=4,P<0.05),HEBalt亚型的表达差异具有高度显著性(n=4,P<0.001)。核心成果提炼:这些Biomarker的功能关联明确,Nanog通过负调控Ebf1抑制B细胞命运决定,HEBalt亚型参与B细胞前体的增殖与分化,H3K27me3修饰的变化调控发育基因的沉默;创新性在于首次发现Dido3通过调控PRC2活性与HEBalt亚型的表达维持B细胞正常发育,首次揭示了Dido3缺失导致的免疫球蛋白重链重排缺陷与染色质可及性变化的关联;统计学结果显示,Nanog表达上调16倍(n=4,P<0.01),HEBalt亚型表达降至WT的10%(n=4,P<0.001),Ebf1在CLP细胞中的表达显著降低(n=4,P<0.05)。这些成果不仅深化了对B细胞发育表观调控网络的理解,还为B细胞发育异常相关疾病(如B细胞白血病)的诊断与治疗提供了潜在的靶点与生物标志物。
