1. 领域背景与文献引入
文献英文标题:Structural determinants of PINK1 topology and dual subcellular distribution;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:神经退行性疾病(帕金森病)与线粒体生物学
帕金森病是全球常见的神经退行性疾病,PTEN诱导的假定激酶1(PINK1)是与常染色体隐性帕金森病密切相关的线粒体靶向激酶,其功能异常被认为是疾病发生的关键机制之一。领域共识:核编码线粒体蛋白通常通过N端疏水前序列(线粒体定位信号,MLS)或内部隐秘序列靶向线粒体,多数蛋白仅定位于线粒体特定区域,但少数如酵母延胡索酸酶和人类PINK1可组成性分布于线粒体和胞质,这种双重定位的调控机制尚未明确,是领域内未解决的核心问题。明确PINK1的亚细胞定位机制,不仅能揭示其亚区室特异性功能,还能为解析PINK1突变导致帕金森病的病理过程提供关键依据。针对PINK1如何在线粒体加工后实现胞质定位的未知机制,本研究聚焦线粒体定位信号、跨膜结构域和激酶结构域在其定位中的作用,旨在系统解析PINK1双重亚细胞定位的结构决定因素。
2. 文献综述解析
作者对领域内现有研究的分类维度包括:线粒体蛋白定位信号的类型、PINK1定位与功能的研究争议、PINK1剪切形式的相关报道。现有研究已证实PINK1的N端MLS足以介导线粒体靶向,过表达和内源性PINK1均存在多种剪切形式,部分研究显示PINK1参与线粒体裂变/融合及线粒体自噬过程,也有证据支持其胞质激酶功能,如胞质降解途径、结合胞质伴侣蛋白及神经保护作用;但现有研究存在明显局限性,多数依赖PINK1过表达系统,缺乏高特异性多用途PINK1抗体,内源性PINK1表达水平极低,且无法明确线粒体和胞质PINK1各自的功能贡献,也未阐明其双重定位的具体结构决定因素。本研究的创新价值在于首次系统解析了PINK1双重亚细胞定位的结构基础,明确了跨膜结构域、跨膜后的剪切位点及激酶结构域与热休克蛋白90(Hsp90)的相互作用是实现双重定位的关键,同时构建了可特异性消除胞质PINK1的突变体(Immt-Δ151 PINK1),弥补了现有研究对PINK1定位机制的空白,为后续功能研究提供了精准的实验模型。
3. 研究思路总结与详细解析
本研究的核心目标是明确PINK1拓扑结构与双重亚细胞定位的结构决定因素,核心科学问题是线粒体定位信号、跨膜结构域、激酶结构域及Hsp90相互作用如何调控PINK1的定位与拓扑,技术路线遵循“验证内源性剪切形式→定位剪切位点→解析结构域功能→探究Hsp90调控作用→总结机制”的闭环逻辑。
3.1 内源性PINK1剪切形式验证
实验目的是确认内源性PINK1的剪切形式,为后续定位剪切位点提供实验基础。方法细节:使用Hela细胞作为实验模型,分别用缬氨霉素(线粒体膜电位去偶联剂,增加全长PINK1积累)和环氧霉素(蛋白酶体抑制剂,增加剪切形式积累)处理细胞,通过蛋白质免疫印迹(Western blot)检测蛋白表达,同时采用siRNA敲低内源性PINK1验证条带特异性。结果解读:
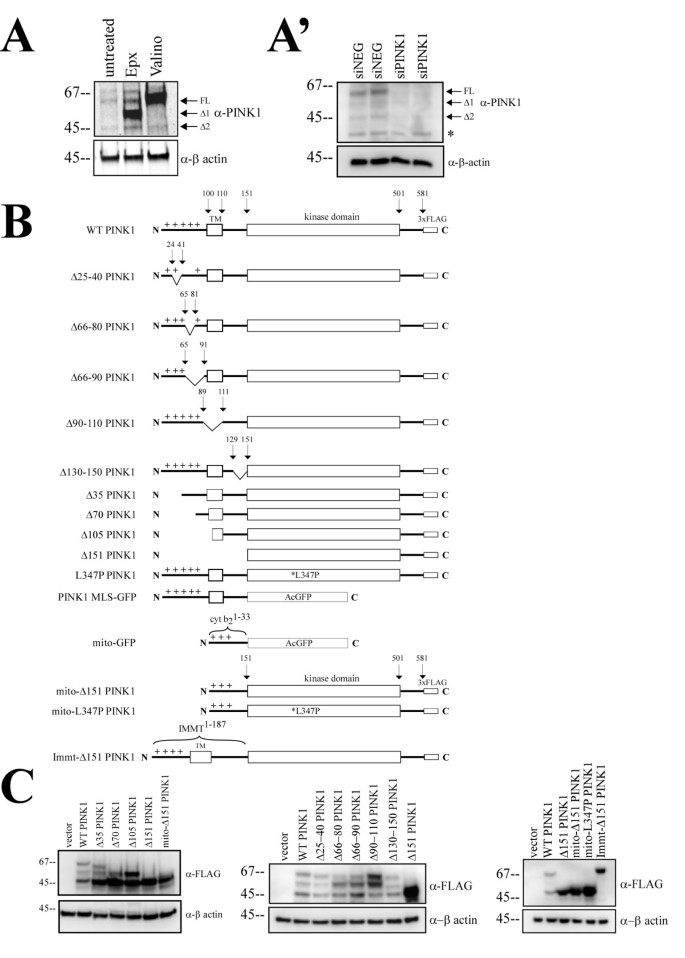
图1A显示,缬氨霉素处理后全长PINK1(FL)水平显著增加,环氧霉素处理后出现约55kDa的Δ1和45kDa的Δ2两种剪切形式;siRNA敲低内源性PINK1后,三条蛋白带均明显减少(图1A"),证实内源性PINK1存在全长、Δ1、Δ2三种稳定形式,且Δ2为功能性剪切产物而非降解产物。产品关联:实验所用关键产品:Novus Biological的抗PINK1抗体(货号BC100-494)、Sigma的FLAG抗体、LI-COR Biosciences的Odyssey红外成像系统。
3.2 PINK1剪切位点定位
实验目的是确定PINK1 N端的剪切位点,解析其线粒体加工机制。方法细节:构建N端系列缺失突变体(Δ35、Δ70、Δ105、Δ151)和内部缺失突变体(Δ25-40、Δ66-80、Δ66-90等),在Hela细胞中过表达后通过蛋白质免疫印迹检测蛋白形式。结果解读:图1C显示,Δ70和Δ105突变体的分子量与野生型PINK1的Δ1和Δ2剪切产物对应,Δ151突变体仅表达为单一最小分子量形式,提示剪切位点位于氨基酸70-105和105-151区间;内部缺失突变体均未消除PINK1的剪切,说明PINK1的MLS剪切机制复杂,不遵循经典的R-2/R-10线粒体加工基序。产品关联:文献未提及具体实验产品,领域常规使用PCR定点突变试剂盒、蛋白质免疫印迹相关试剂。
3.3 跨膜结构域对PINK1定位与拓扑的作用
实验目的是明确跨膜结构域(TM)在PINK1膜锚定和胞质朝向拓扑中的调控作用。方法细节:构建PINK1 MLS-GFP(保留跨膜结构域,替换激酶结构域为绿色荧光蛋白,GFP)、Δ90-110 PINK1(缺失跨膜结构域)等突变体,在Hela细胞中表达后进行线粒体分离、蛋白酶K消化实验及免疫荧光染色。结果解读:
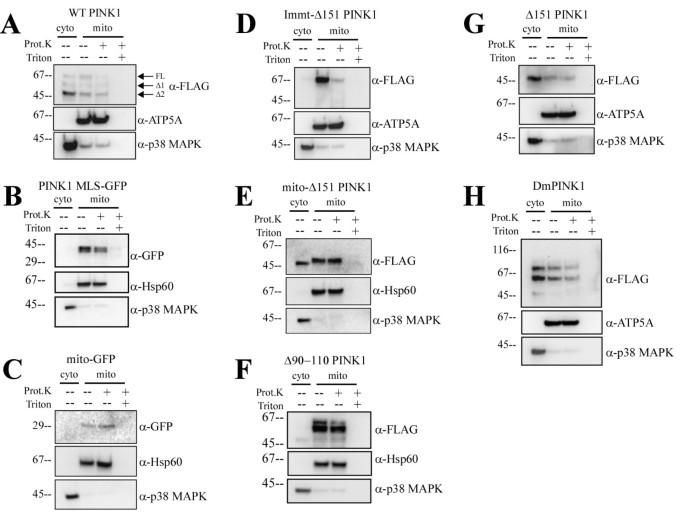
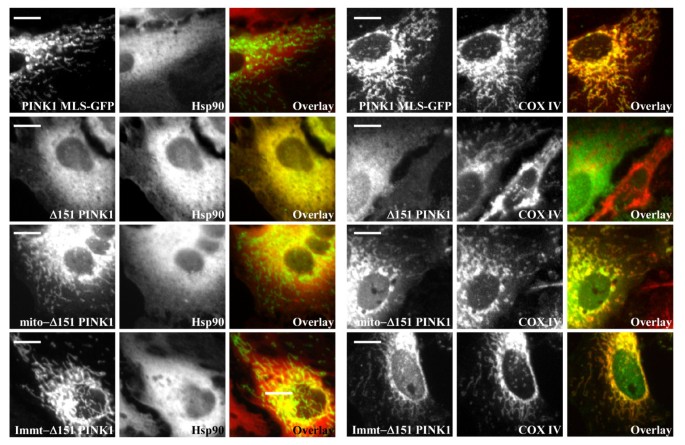
图2B和图3显示,PINK1 MLS-GFP仅定位于线粒体,且抵抗蛋白酶K消化,说明跨膜结构域单独不足以实现胞质定位;Δ90-110 PINK1主要定位于线粒体且抵抗蛋白酶K,仅少量剪切形式存在于胞质,说明跨膜结构域是膜锚定和胞质朝向拓扑的重要但非必需因素。产品关联:实验所用关键产品:Invitrogen的Lipofectamine 2000转染试剂、Pierce的线粒体分离试剂盒、Olympus的DSU转盘共聚焦显微镜。
3.4 激酶结构域与Hsp90相互作用对PINK1定位的调控
实验目的是探究激酶结构域及与Hsp90的相互作用在PINK1胞质再分布中的核心作用。方法细节:构建Immt-Δ151 PINK1(含mitofilin的MLS和PINK1激酶结构域,无跨膜后剪切位点)、mito-Δ151 PINK1(含细胞色素b2的MLS和激酶结构域,无跨膜结构域)、L347P突变体(天然帕金森病突变,降低与Hsp90的结合),使用Hsp90抑制剂17-AAG处理细胞,进行亚细胞分离、免疫共沉淀(Co-IP)实验及定量分析。结果解读:
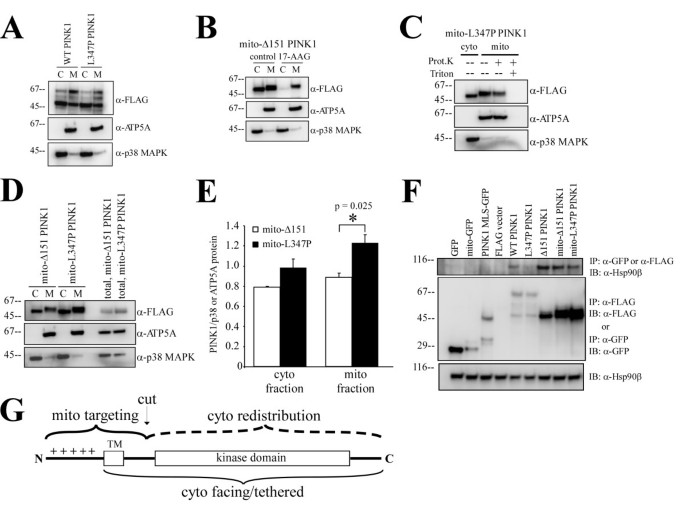
图2D和图3显示,Immt-Δ151 PINK1仅定位于线粒体,说明跨膜后的剪切位点是胞质定位的必需条件;mito-Δ151 PINK1均等分布于胞质和线粒体,线粒体部分抵抗蛋白酶K;图4D-E显示,mito-L347P PINK1在线粒体中的比例显著高于mito-Δ151 PINK1(1.226±0.086 vs 0.888±0.044,均值±标准误,n=3,P=0.025),免疫共沉淀实验显示L347P突变显著降低了PINK1与Hsp90的结合(图4F);17-AAG处理后,mito-Δ151 PINK1的胞质分布完全消失,说明Hsp90与激酶结构域的相互作用可阻止PINK1进一步进入线粒体基质,促进其逆向运动至胞质。产品关联:实验所用关键产品:Sigma的p3XFLAG-CMV14载体、Cell Signal Technologies的Hsp90β抗体、Promega的HRP标记二抗。
4. Biomarker研究及发现成果解析
本研究聚焦的Biomarker为PINK1自身,属于功能型Biomarker,其筛选与验证逻辑为:基于内源性PINK1的剪切形式,通过系列突变体定位调控定位的关键结构域,再通过Hsp90相互作用实验验证调控机制。
研究过程中,Biomarker来源为Hela细胞表达的野生型和突变型PINK1,验证方法包括蛋白质免疫印迹、亚细胞分离、蛋白酶K消化、免疫共沉淀、免疫荧光染色等。特异性与敏感性数据显示,Immt-Δ151 PINK1可特异性消除胞质PINK1,仅保留线粒体定位;L347P突变体与Hsp90的结合显著降低,在线粒体中的比例较野生型增加38%(P=0.025,n=3)。
核心成果总结:本研究明确了PINK1双重亚细胞定位的三个关键结构决定因素:跨膜结构域、跨膜后的剪切位点、激酶结构域与Hsp90的相互作用;首次构建了仅定位于线粒体的PINK1突变体(Immt-Δ151 PINK1),为单独研究线粒体PINK1的功能提供了精准工具;创新性在于揭示了Hsp90相互作用在PINK1拓扑结构和胞质再分布中的关键调控作用,推测:PINK1进入线粒体后,跨膜结构域和激酶结构域共同阻止其进入线粒体基质,形成锚定拓扑,跨膜后的剪切使其从膜上释放,结合Hsp90后实现逆向运动至胞质,提示PINK1具有线粒体和胞质的亚区室特异性功能,为帕金森病的发病机制研究提供了新的视角。
