1. 领域背景与文献引入
文献英文标题:The MEK2-binding tumor suppressor hDlg is recruited by E-cadherin to the midbody ring;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(胞质分裂调控与肿瘤抑制蛋白信号通路)
领域共识:肿瘤抑制蛋白hDlg(果蝇Dlg的人类同源物)属于膜相关鸟苷酸激酶(MAGUK)家族,通过PDZ、SH3等多个蛋白相互作用结构域,在细胞间连接、突触前致密区组装信号复合物,参与细胞生长调控与肿瘤抑制。已知hDlg定位于上皮细胞连接、细胞核及胞质分裂的中体结构,但其中体处的具体功能及结合伴侣尚未明确;经典RAF/MEK/ERK信号通路调控细胞增殖与周期进程,活化MEK2在胞质分裂阶段定位于中体,但与hDlg的相互作用及调控机制未被揭示。当前研究空白在于缺乏对hDlg中体定位的特异性调控机制、其与MEK2相互作用的活化状态依赖性,以及E-钙粘蛋白在该过程中作用的系统性研究,因此本研究旨在鉴定hDlg在中体处的结合伴侣,明确二者相互作用的特异性及招募调控机制,为理解胞质分裂的信号调控网络提供新依据。
2. 文献综述解析
作者从hDlg的亚细胞定位与功能、MEK2的活化与胞质分裂作用、E-钙粘蛋白的细胞连接调控三个维度,对领域内现有研究进行分类评述。
现有研究表明,hDlg作为肿瘤抑制蛋白,通过PDZ结构域招募腺瘤性息肉病coli(APC)、人乳头瘤病毒E6蛋白等多种分子,参与上皮细胞连接组装与细胞周期调控;活化MEK2作为RAF/MEK/ERK通路的关键激酶,在胞质分裂阶段定位于中体,调控分裂进程;E-钙粘蛋白与hDlg在上皮细胞连接处结合,维持细胞粘附与极性。现有技术方法如酵母双杂交、免疫共沉淀已鉴定hDlg的部分结合伴侣,但存在局限性:未明确hDlg在中体处的特异性结合伴侣及活化状态对相互作用的影响,也未揭示E-钙粘蛋白对hDlg中体招募的调控作用,且部分研究对hDlg可变剪接体的定位存在非特异性结果。
本研究的创新价值在于,首次发现活化MEK2通过C端I类PDZ结合基序与hDlg的PDZ结构域特异性相互作用,且E-钙粘蛋白介导膜结合型hDlg(而非活化MEK2)向中体环的招募,填补了hDlg中体功能及调控机制的研究空白,为胞质分裂的信号调控网络提供了新的分子节点。
3. 研究思路总结与详细解析
本研究的整体目标是鉴定hDlg在中体处的特异性结合伴侣,明确二者相互作用的活化状态依赖性及招募调控机制;核心科学问题为hDlg如何与活化MEK2特异性相互作用,以及E-钙粘蛋白在hDlg中体招募中的调控作用;技术路线遵循“筛选结合伴侣→验证相互作用特异性→确认活化状态依赖性→定位亚细胞分布→验证招募调控因子”的闭环逻辑,通过多层面实验验证研究假设。
3.1 酵母双杂交筛选hDlg的新结合伴侣
实验目的为筛选与hDlg相互作用的未知信号蛋白,以明确其中体处的功能复合物组成。方法细节采用MatchMaker酵母双杂交系统,以全长hDlg为诱饵,对HeLa细胞cDNA文库进行筛选,获得阳性克隆后,通过与对照质粒共转化验证报告基因激活的特异性,排除非特异性相互作用。结果解读显示,筛选到编码MEK2 C端126个氨基酸的克隆,该克隆与hDlg共转化时可显著激活lacZ报告基因,而与空载体或无关蛋白质粒共转化时无激活,表明MEK2 C端片段与hDlg存在特异性相互作用。产品关联:文献未提及具体实验产品,领域常规使用酵母双杂交系统试剂盒、cDNA文库、酵母菌株等试剂/仪器。
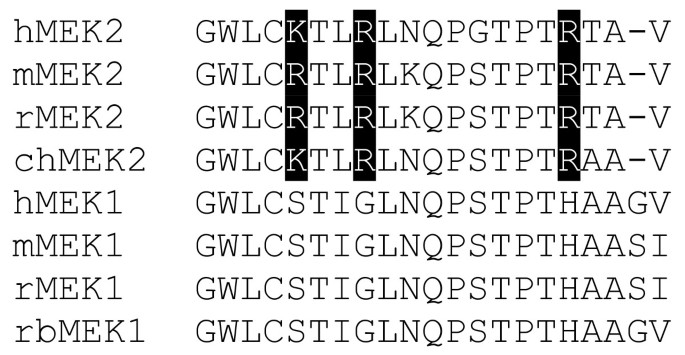
3.2 肽结合实验验证MEK2与hDlg PDZ结构域的特异性相互作用
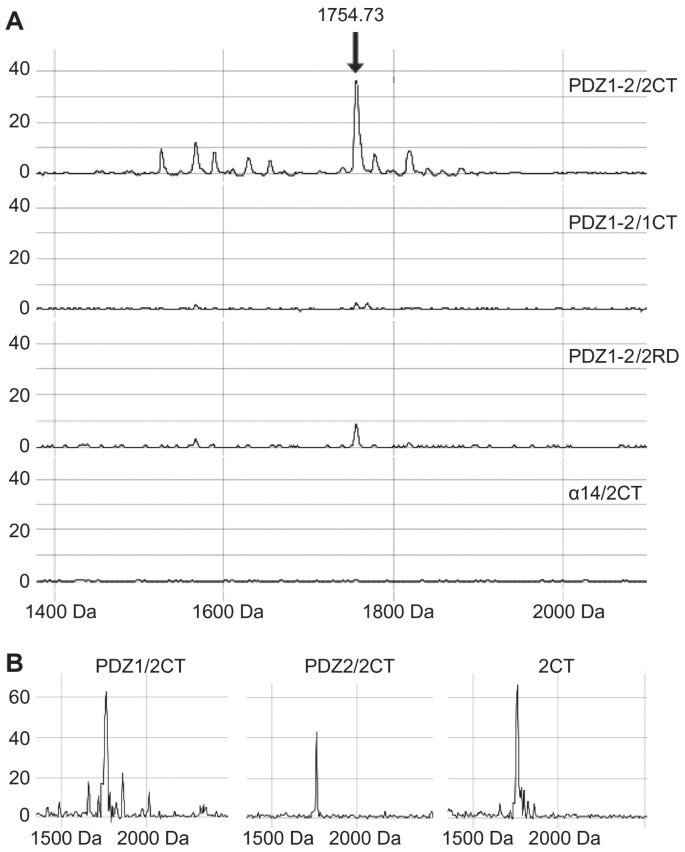
实验目的为验证MEK2(而非MEK1)通过C端基序与hDlg PDZ结构域的特异性结合,明确相互作用的结构基础。方法细节合成对应MEK2、MEK1 C端16个氨基酸的肽段,以及MEK2肽段的随机序列,将这些肽段与hDlg的PDZ1-PDZ2 GST融合蛋白孵育,通过MALDI-TOF质谱分析结合的肽段,同时单独检测每个PDZ结构域与MEK2肽段的结合情况。结果解读显示,仅MEK2肽段能与GST-PDZ1-2特异性结合,且与单独表达的PDZ1、PDZ2结构域均有结合(PDZ3结合最弱),序列比对表明MEK2 C端具有I类PDZ结合基序(-X-(S/T)-X-Φ),而MEK1无该基序,证实MEK2通过C端特异性基序与hDlg PDZ结构域相互作用。产品关联:文献未提及具体实验产品,领域常规使用GST融合蛋白表达系统、多肽合成服务、MALDI-TOF质谱仪等试剂/仪器。
3.3 昆虫细胞共表达验证hDlg与活化MEK2的相互作用
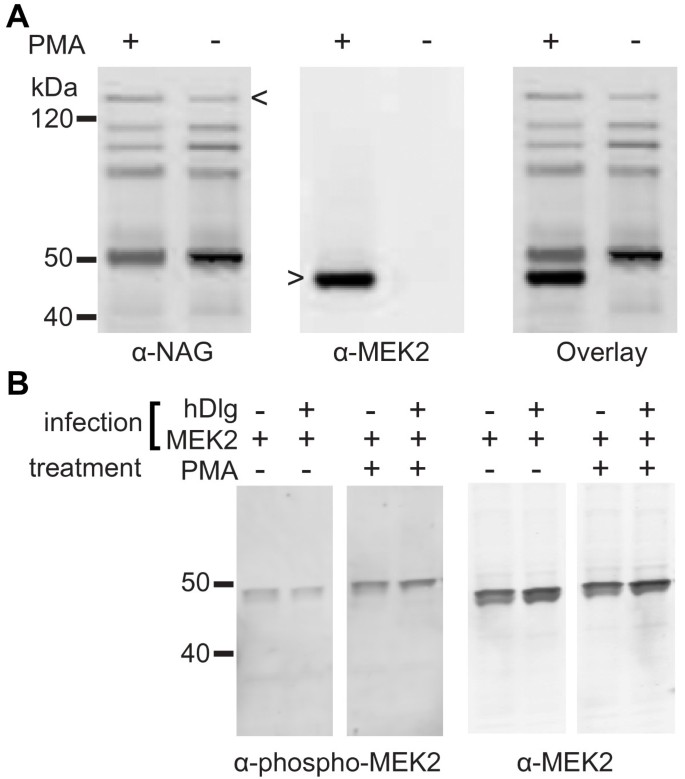
实验目的为在体内验证hDlg与MEK2的相互作用是否依赖MEK2的活化状态。方法细节在High 5昆虫细胞中,通过重组杆状病毒共表达GST-hDlg与MEK2,用佛波酯(PMA)处理细胞以激活RAF/MEK/ERK通路,通过GSH-琼脂糖亲和纯化GST-hDlg复合物,免疫印迹检测共沉淀的MEK2及磷酸化MEK2水平。结果解读显示,仅PMA处理组中MEK2与GST-hDlg共沉淀,且PMA处理显著提高MEK2的磷酸化水平,而未处理组中无共沉淀现象,表明hDlg选择性结合活化(磷酸化)状态的MEK2,该相互作用依赖MEK2的活化。产品关联:文献未提及具体实验产品,领域常规使用杆状病毒表达系统、免疫印迹检测试剂盒、磷酸化抗体等试剂/仪器。
3.4 免疫荧光分析hDlg与活化MEK2的亚细胞定位
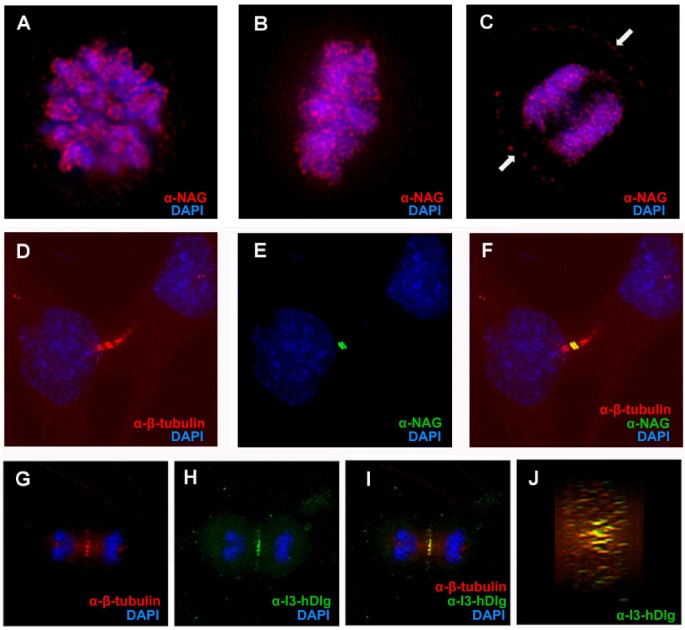
实验目的为明确hDlg与活化MEK2在细胞周期不同阶段的亚细胞分布,尤其是胞质分裂阶段的共定位情况。方法细节对MCF10A细胞进行免疫荧光染色,使用抗hDlg(识别所有亚型)、抗I3可变剪接片段(识别膜结合型hDlg)、抗β-微管蛋白、抗磷酸化MEK2抗体,通过去卷积显微镜观察有丝分裂各阶段及胞质分裂阶段的蛋白定位,对中体结构进行三维重建分析。结果解读显示,有丝分裂前期到后期,hDlg定位于浓缩染色体表面;胞质分裂阶段,含I3可变剪接片段的膜结合型hDlg特异性定位于中体环结构,与活化MEK2共定位,而含I2可变剪接片段的核定位hDlg不进入中体,表明仅膜结合型hDlg被招募至中体环。产品关联:文献未提及具体实验产品,领域常规使用免疫荧光染色试剂盒、去卷积显微镜、荧光二抗等试剂/仪器。
3.5 RNA干扰验证E-钙粘蛋白对hDlg中体招募的调控作用
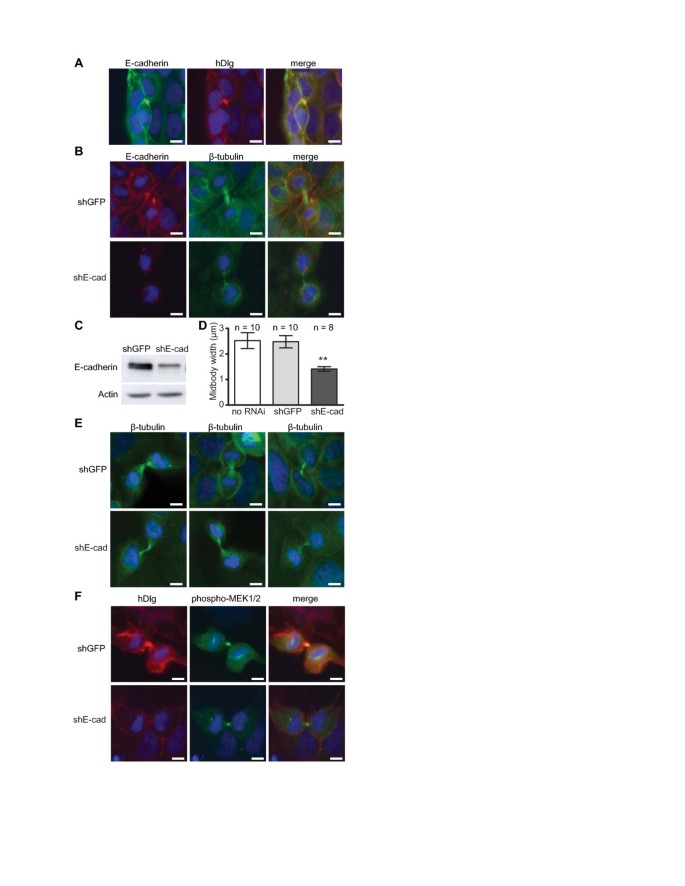
实验目的为明确E-钙粘蛋白是否参与hDlg向中体环的招募过程,以及对活化MEK2定位的影响。方法细节在Caco-2/15结肠上皮细胞中,通过慢病毒介导的shRNA敲低E-钙粘蛋白表达,设置对照shRNA(靶向TurboGFP)及无处理组,免疫荧光染色观察hDlg、活化MEK2及β-微管蛋白的定位,测量中体宽度并进行双尾Student"s t检验分析统计学差异。结果解读显示,E-钙粘蛋白敲低后,hDlg在中体环的定位显著减弱,中体平均宽度较对照组显著变窄(shE-cadherin vs shGFP,P=0.002;shE-cadherin vs 无RNAi,P=0.007),但活化MEK2的中体定位不受影响,表明E-钙粘蛋白是hDlg向中体环招募的必要条件,但不调控活化MEK2的中体定位。产品关联:文献未提及具体实验产品,领域常规使用慢病毒RNA干扰系统、免疫荧光定量分析软件、统计学分析工具等试剂/仪器。
4. Biomarker研究及发现成果解析
本研究中涉及的功能调控分子为hDlg的I3可变剪接亚型,作为中体环特异性招募的分子标志物,其筛选与验证遵循“亚细胞定位鉴定→调控因子验证”的逻辑链条。
该Biomarker属于蛋白亚型标志物(膜结合型hDlg),筛选逻辑为通过免疫荧光染色区分不同可变剪接体的亚细胞定位,验证逻辑为通过RNA干扰敲低E-钙粘蛋白,观察其定位变化。研究过程详述:该Biomarker来源于内源性表达的上皮细胞,验证方法为免疫荧光染色(抗I3特异性抗体),特异性表现为仅I3亚型定位于中体环,而I2核定位亚型不进入中体;敏感性相关数据文献未明确提供(文献未明确提供该数据,基于图表趋势推测)。
核心成果提炼:I3亚型hDlg作为中体环的特异性招募分子,通过与活化MEK2相互作用参与胞质分裂信号复合物的组装,E-钙粘蛋白是其招募的必要条件;该发现首次揭示了hDlg在中体处的信号复合物组成及招募机制,为理解肿瘤抑制蛋白在胞质分裂中的功能提供了新的分子视角;统计学结果显示,E-钙粘蛋白敲低后中体宽度的差异具有高度统计学显著性(P=0.002、P=0.007),样本量未明确提供(文献未明确提供该数据,基于图表趋势推测)。推测:该调控机制可能参与上皮细胞的胞质分裂调控,若hDlg招募异常可能导致胞质分裂缺陷,进而促进肿瘤发生,需进一步在肿瘤细胞模型中验证其功能。
