1. 领域背景与文献引入
文献英文标题:Optimisation of cryopreservation conditions, including storage duration and revival methods, for the viability of human primary cells;发表期刊:BMC Molecular and Cell Biology;影响因子:未明确提供;研究领域:组织工程与再生医学(原代细胞冻存)
领域共识:原代细胞因具有与体内细胞更接近的表型与功能,是组织工程与再生医学研究的核心细胞资源,但原代细胞的获取难度大、体外培养周期长,冻存是实现其长期保存的唯一可行方法。组织工程与再生医学领域中,细胞冻存技术的发展经历了多个关键节点:1949年Polge等发现甘油的冻存保护作用,开启了细胞冻存的先河;1950年代二甲基亚砜(DMSO)的应用大幅提升了冻存效率,成为至今最常用的渗透型冻存保护剂;近年来,无血清/无动物源冻存培养基、程序化降温与玻璃化冻存技术成为研究热点,旨在提升临床应用的安全性与细胞活力稳定性。当前领域未解决的核心问题在于,原代细胞具有高度异质性,不同细胞类型的最优冻存方案缺乏统一标准,现有方案常存在复苏后细胞活力下降、功能表型丢失等问题,限制了原代细胞在组织工程产品制备与再生医学治疗中的应用。
针对这一研究空白,本研究系统评估了细胞类型、冻存培养基、储存时长、储存位置与复苏方法对人原代细胞活力的影响,通过回顾性细胞库数据分析与针对性实验验证,筛选出最优冻存参数组合,为原代细胞的标准化冻存提供了可落地的技术指南,对推动组织工程与再生医学的临床转化具有重要学术价值与实践意义。
2. 文献综述解析
作者在综述部分围绕冻存损伤机制、冻存保护剂分类与现有方案局限性三个维度,系统评述了原代细胞冻存领域的研究现状,明确了现有研究的核心结论、技术优势与未解决问题,为本次研究的创新定位提供了逻辑支撑。
现有研究已证实,细胞冻存过程中的损伤主要源于冰晶形成导致的机械损伤、渗透压失衡引发的细胞脱水与氧化应激;渗透型保护剂如二甲基亚砜可通过进入细胞降低电解质浓度减少损伤,非渗透型保护剂如胎牛血清(FBS)可通过提供营养与渗透压支持维持细胞稳态;程序化降温容器如CoolCell可实现稳定的-1℃/min降温速率,提升冻存一致性,无血清冻存培养基则避免了动物源成分的安全风险,更适配临床应用场景。但现有研究多集中于永生化细胞系,针对原代细胞的研究样本量有限,且未充分考虑细胞类型、储存时长与复苏方法的协同效应,长期冻存后细胞功能表型的维持情况也缺乏系统评估,导致现有方案在原代细胞中的适用性不足。
与现有研究相比,本研究的核心创新点在于首次基于大型原代细胞库的真实世界数据,系统分析了多种冻存参数的组合效应,同时通过针对性实验验证了人真皮成纤维细胞在不同冻存条件下的活力与功能表型维持,填补了原代细胞冻存方案缺乏多维度系统优化的研究空白,为原代细胞的标准化冻存提供了兼具科学性与实用性的参考依据。
3. 研究思路总结与详细解析
本研究的整体研究框架以“筛选最优冻存参数、验证细胞活力与表型”为核心目标,聚焦“冻存条件如何协同影响原代细胞活力与功能”这一科学问题,采用“回顾性数据分析→实验验证→多指标评估”的闭环技术路线,系统完成了从数据挖掘到功能验证的研究过程。
3.1 原代细胞库冻存数据回顾性分析
本环节的核心实验目的是从已建立的原代细胞库数据中,初步筛选出对细胞复苏活力影响显著的冻存参数组合。研究人员收集了马来西亚国民大学组织工程与再生医学系(DTERM)细胞库中皮肤角质形成细胞、成纤维细胞、呼吸道上皮细胞、骨髓间充质干细胞的冻存与复苏数据,涵盖4种细胞类型、2种冻存培养基(FBS+10%二甲基亚砜与商用培养基)、4种储存时长区间(0-6个月、6-12个月、12-24个月、>24个月)、液氮气相与液相两种储存位置,以及直接复苏(解冻后直接接种)与间接复苏(解冻后离心去除上清再接种)两种复苏方法,以复苏后24小时的细胞贴壁率作为活力评估指标。结果显示,成纤维细胞在所有细胞类型中表现出最高的复苏贴壁率,FBS+10%二甲基亚砜冻存培养基组的贴壁率>60%的冻存管数量显著多于商用培养基组,储存时长0-6个月的样本复苏效果最优,直接复苏方法的贴壁率优于间接复苏,液氮气相储存的样本贴壁率高于液相储存。实验所用关键产品:CoolCell冻存容器(Corning, USA)、FBS(LSP, UK)、二甲基亚砜(Sigma, Germany)。
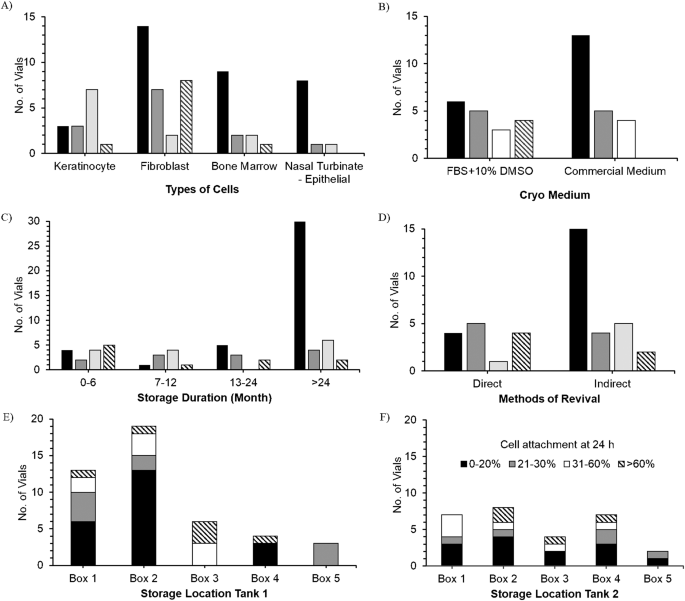
3.2 人真皮成纤维细胞冻存与复苏验证实验
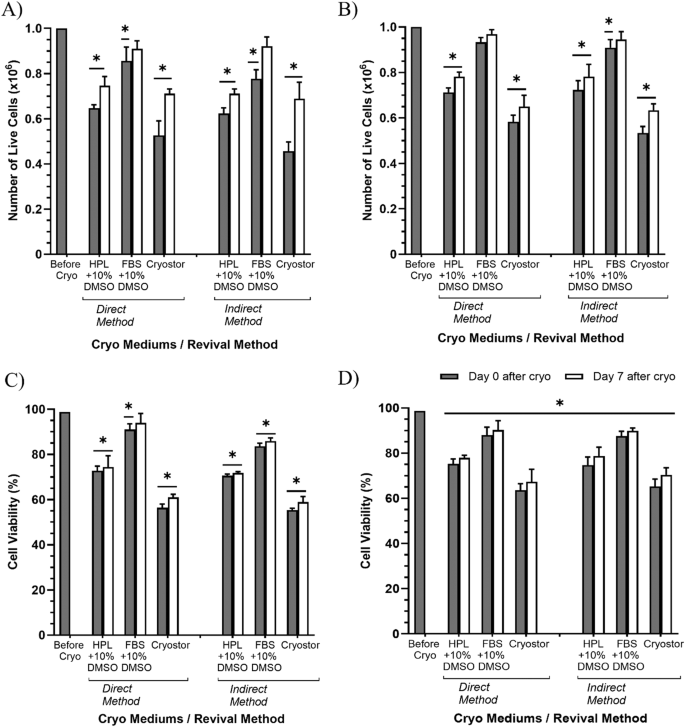
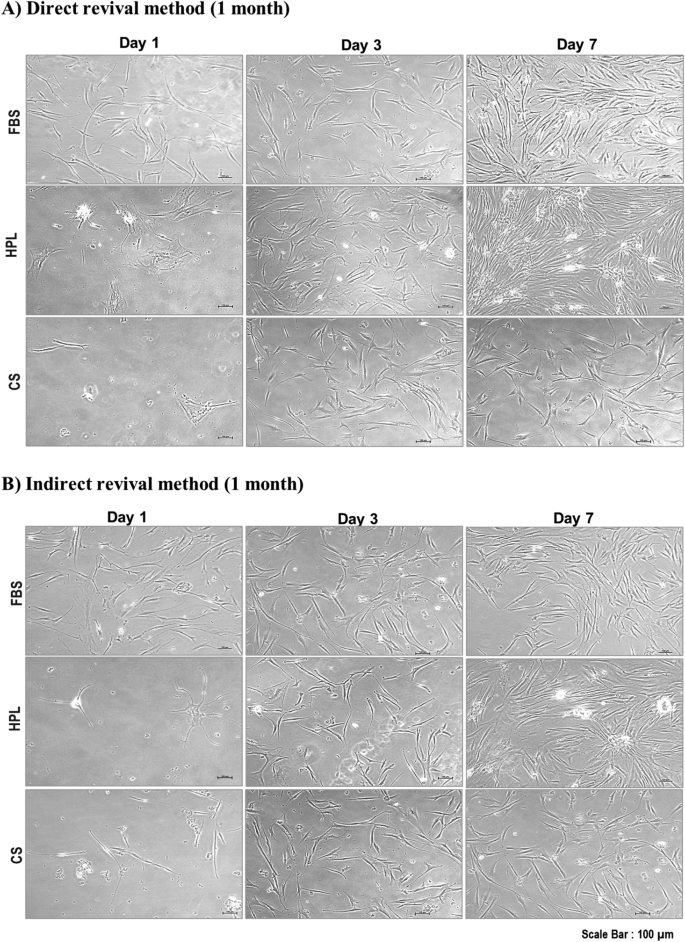
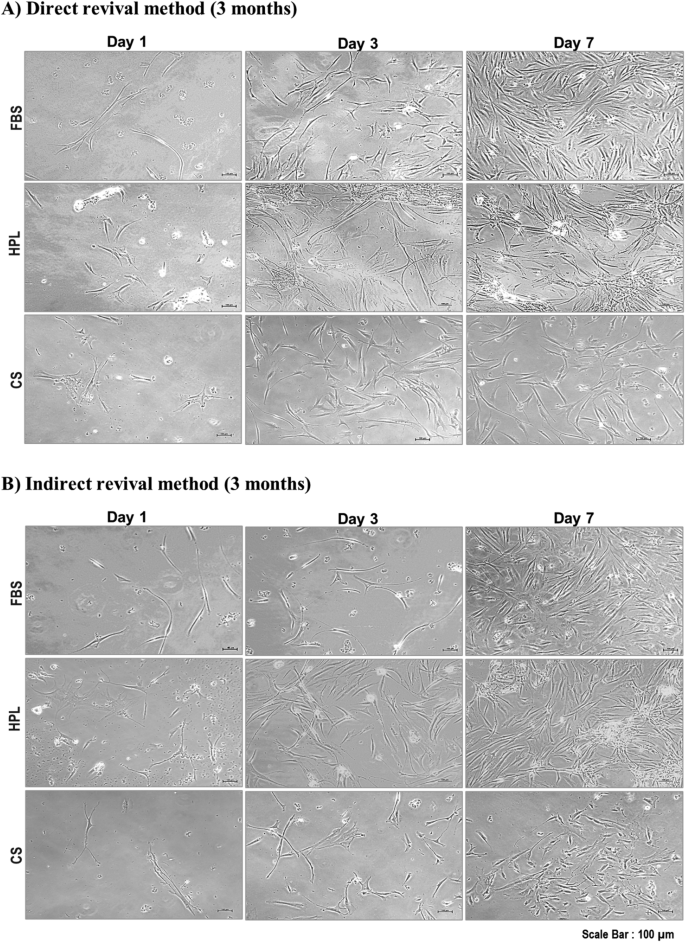
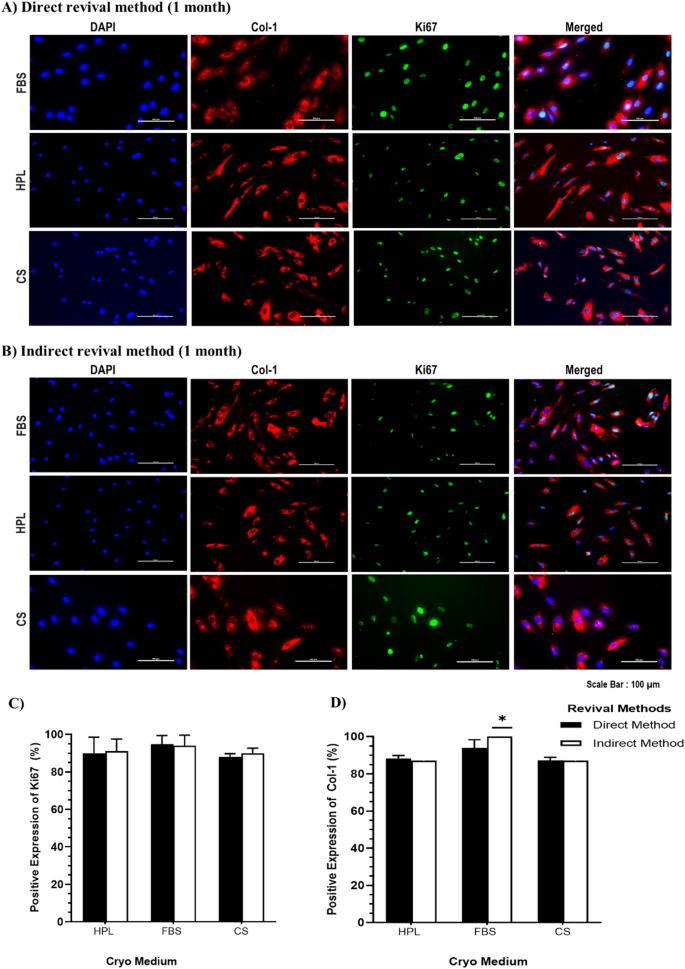
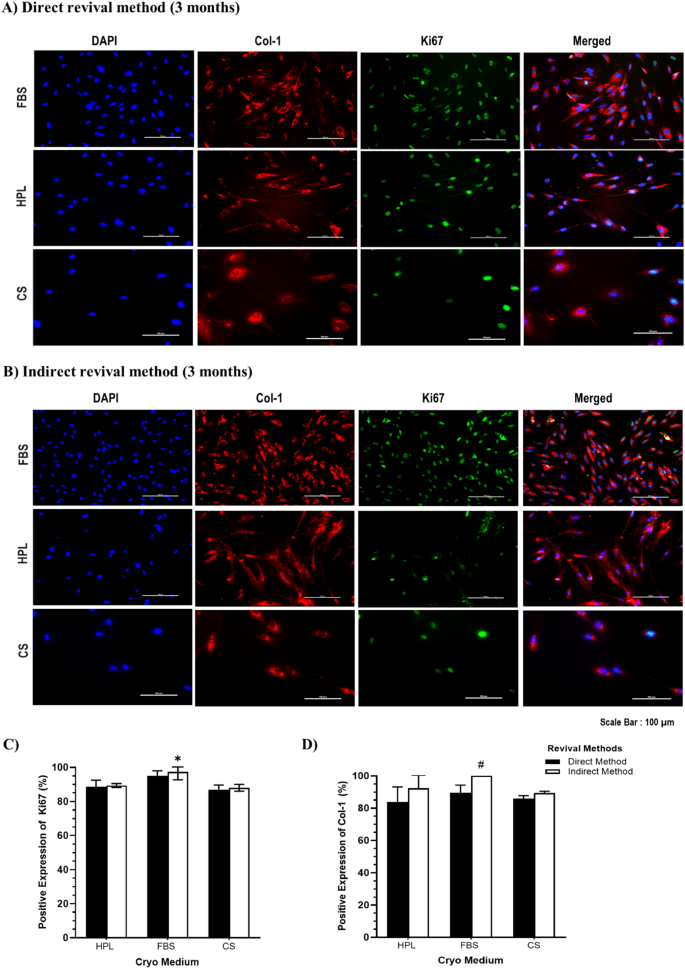
本环节的核心实验目的是验证回顾性分析得到的最优参数,并进一步评估冻存条件对细胞活力、形态与功能蛋白表达的影响。研究人员培养人真皮成纤维细胞(HDF),将其分别悬浮于FBS+10%二甲基亚砜、人血小板裂解物(HPL)+10%二甲基亚砜、CryoStor三种冻存培养基中,采用CoolCell容器程序化降温至-80℃后转移至液氮罐,分别储存1个月和3个月。复苏时采用直接与间接两种方法,复苏后检测细胞数量、活力,并通过免疫细胞化学(immunocytochemistry,ICC)染色检测增殖标记物Ki67与成纤维细胞功能标记物Ⅰ型胶原(Col-1)的表达。结果显示,冻存1个月和3个月后,FBS+10%二甲基亚砜组的活细胞数与活力均显著高于其他两组,活力维持在80%以上(n=3,P<0.05);形态学观察显示,FBS+10%二甲基亚砜组的成纤维细胞在复苏后1天即表现出良好的贴壁能力,且维持了典型的纺锤形形态;免疫细胞化学结果显示,冻存3个月后,间接复苏的FBS+10%二甲基亚砜组Ki67阳性率为97.3%±4.62(n=3,P<0.05),Col-1阳性率在1个月和3个月时均为100%(n=3,P<0.05),显著高于其他冻存培养基组。实验所用关键产品:CryoStor(Stemcell, Canada)、Ki67抗体(Abcam, UK)、Col-1抗体(Abcam, UK)、Nikon A1R共聚焦显微镜(Nikon, Japan)。
4. Biomarker研究及发现成果
本研究聚焦细胞增殖与功能相关的蛋白标记物Ki67与Col-1,系统评估了不同冻存条件下这些Biomarker的表达变化,明确了最优冻存条件对原代细胞表型维持的作用。
本研究涉及的Biomarker为细胞内蛋白标记物,其中Ki67是细胞增殖的特异性标记物,Col-1是成纤维细胞合成细胞外基质的核心功能标记物。研究采用“回顾性分析筛选最优条件→细胞实验验证活力→免疫细胞化学检测标记物表达”的完整逻辑链条,验证了这些Biomarker在冻存条件优化中的指示作用。
这些Biomarker的检测样本来源为体外培养的人真皮成纤维细胞,验证方法为免疫细胞化学染色,通过共聚焦显微镜观察并定量分析阳性细胞比例。结果显示,在FBS+10%二甲基亚砜冻存培养基中储存3个月后,间接复苏组的Ki67阳性率为97.3%±4.62(n=3,P<0.05),显著高于HPL+10%二甲基亚砜与CryoStor组;Col-1阳性率在FBS+10%二甲基亚砜组的1个月和3个月冻存样本中均为100%(n=3,P<0.05),显著高于其他两组,提示该冻存条件可有效维持成纤维细胞的增殖能力与功能表型。
该Biomarker的功能关联在于,Ki67的高表达提示细胞在冻存复苏后仍保持活跃的增殖潜能,Col-1的持续高表达则表明成纤维细胞的基质合成功能未受冻存影响。本研究的创新性在于首次系统验证了冻存条件对原代成纤维细胞增殖与功能标记物的协同影响,为原代细胞冻存后的功能评估提供了量化的Biomarker指标,相关统计学结果显示各实验组间的差异具有显著性(P<0.05),为后续原代细胞冻存方案的优化与评估提供了可靠的参考依据。
