1. 领域背景与文献引入
文献英文标题:Global transcriptome profile of the developmental principles of in vitro iPSC-to-motor neuron differentiation;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:干细胞生物学与神经发育(运动神经元再生)
人类中枢神经系统神经元缺乏再生能力,脊髓损伤、肌萎缩侧索硬化(ALS)等神经退行性疾病中,运动神经元的进行性丢失是核心病理特征,现有治疗手段难以逆转神经元损伤。诱导多能干细胞(iPSC)技术的突破为运动神经元的体外定向分化提供了可行途径,成为再生医学与疾病建模的研究热点。领域共识:iPSC向运动神经元的分化方案主要通过模拟体内神经发育的信号通路调控,如抑制转化生长因子-β(TGFβ)通路、激活 sonic hedgehog(Shh)与Wnt/β-catenin通路,但当前分化体系仍存在细胞异质性高、成熟周期长、功能成熟度不足等问题,且分化过程中全局转录组调控网络的时序变化尚未完全解析,限制了分化方案的优化与临床转化。针对这一研究空白,本研究通过全局转录组测序结合功能验证,系统解析了iPSC向运动神经元分化各阶段的基因表达谱与信号通路动态变化,为优化运动神经元分化方案、提高细胞功能成熟度提供了分子依据。
2. 文献综述解析
作者在综述部分按技术发展脉络系统梳理了iPSC向运动神经元分化的研究现状,总结了现有体系的核心机制与局限性。早期分化方案依赖细胞共培养或复杂生长因子组合,虽能获得运动神经元样细胞,但存在成分不明确、重复性差的问题;后续发展的化学小分子诱导方案通过精准调控发育信号通路,提高了分化效率,但仍面临细胞异质性高、功能成熟度不足的挑战。现有转录组研究多聚焦于单一阶段或特定通路,缺乏对分化全过程全局调控网络的时序解析,且未充分结合功能验证(如电生理活性)揭示转录组变化与细胞功能的关联。本研究的创新点在于,采用bulk RNA-seq技术覆盖分化的五个关键阶段(iPSC、神经干细胞、运动神经元前体细胞、早期运动神经元、成熟运动神经元),结合多电极阵列(MEA)功能验证与定制化通路分析工具(OPaver),系统解析了分化过程中信号通路的时序调控网络,首次揭示了钙信号通路的阶段性抑制与激活对运动神经元发育的关键作用,以及胆碱能受体亚型转换的分子机制,填补了全局转录组时序分析与功能关联的研究空白。
3. 研究思路总结与详细解析
本研究的核心目标是解析体外iPSC向运动神经元分化的全局转录组调控网络,明确各发育阶段的分子特征与关键信号通路动态变化;核心科学问题是分化过程中信号通路的时序调控如何驱动细胞命运决定与功能成熟;技术路线为“细胞分化模型构建→多阶段转录组测序→生物信息学通路分析→分子标记物验证→功能活性检测”的闭环逻辑。
3.1 细胞分化模型构建与形态学验证
实验目的:建立稳定、高效的iPSC向运动神经元分阶段诱导体系,并通过形态学与免疫标记物验证各阶段细胞身份。
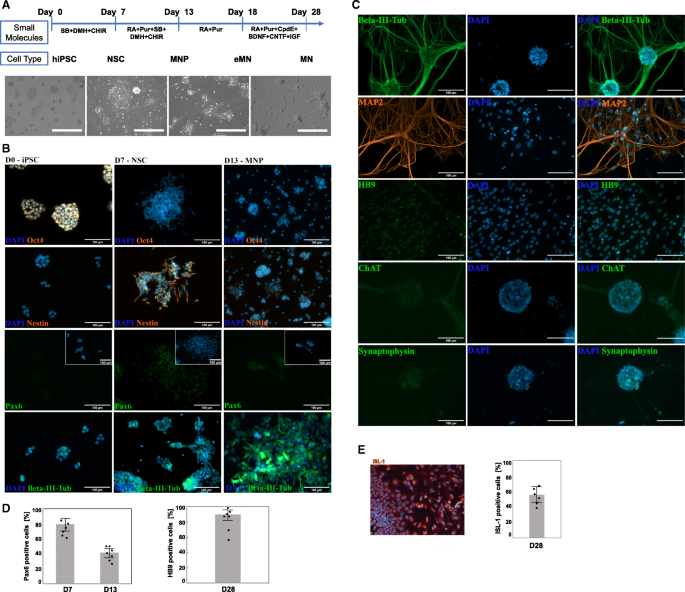
方法细节:采用WTC-11 iPSC细胞系,分四个阶段进行化学诱导:D0-D6添加CHIR99021(Wnt激活剂)、DMH-1(骨形态发生蛋白BMP抑制剂)、SB431542(TGFβ抑制剂)诱导神经干细胞(NSC);D6-D12添加全反式维甲酸(RA)与Purmorphamine(Shh激活剂)诱导运动神经元前体细胞(MNP);D12-D18维持上述诱导剂促进早期运动神经元(eMN)形成;D18-D28添加Compound E(Notch抑制剂)与神经营养因子(IGF-1、BDNF、CNTF)促进成熟运动神经元(MN)形成。通过免疫组化(IHC)检测各阶段特异性标记物:D0检测Oct4(多能性标记),D7检测Nestin、Pax6(NSC标记),D13检测III类β-微管蛋白(βIII-Tub,泛神经元标记),D28检测HB9、胆碱乙酰转移酶(ChAT)、突触素(Synaptophysin,成熟MN标记),并对标记物阳性细胞进行定量分析(n=6,每个培养物随机选取>300个细胞)。
结果解读:形态学观察显示,iPSC从紧凑集落逐渐转变为具有长突起的神经元样细胞;免疫组化结果显示,D0 Oct4阳性率100%,D7 Oct4消失,Nestin与Pax6阳性率显著升高,D13 Nestin表达下调、βIII-Tub表达上调,D28 HB9阳性率为85%±15%,Isl1阳性率为60%±12%(文献未明确提供P值,基于图表趋势推测),表明成功构建了分阶段的运动神经元分化体系。
产品关联:实验所用关键产品:ThermoFisher Scientific的Essential8培养基、vitronectin包被液、免疫组化二抗;StemCell Technology的CHIR99021、SB431542、RA;Tocris的DMH-1;Sigma的Purmorphamine;Applied Biosciences的RT-qPCR试剂盒等。
3.2 转录组测序与生物信息学分析
实验目的:解析分化各阶段的全局基因表达谱差异,筛选关键调控基因与通路。
方法细节:在D0、D7、D13、D18、D28五个时间点收集细胞样本,每个时间点设置3个生物学重复;采用Illumina TruSeq Stranded Total RNA试剂盒构建文库,进行RNA-seq测序(每个样本产生2600-4000万条reads);通过FaQCs进行质量控制,PiReT结合DESeq2进行差异表达基因(DEGs)分析(调整后p<0.0002,fold change>3);采用DAVID进行基因本体(GO)分析,LANL开发的OPaver进行KEGG通路分析。
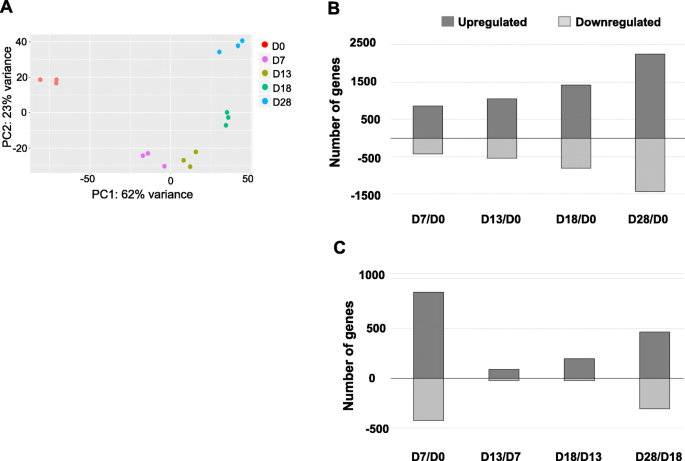
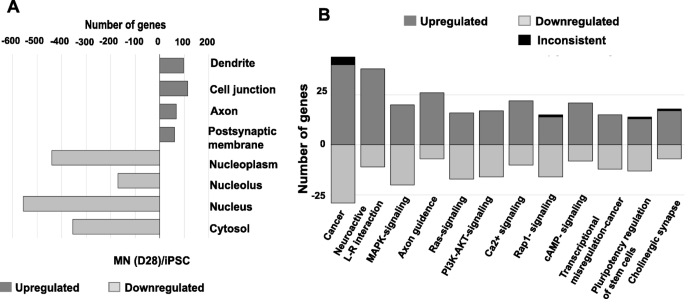
结果解读:主成分分析(PCA)显示各阶段样本聚类紧密,重复性良好;与D0 iPSC相比,D7、D13、D18、D28的DEGs数量逐渐增加,其中D7与D0的DEGs数量最多,表明早期分化阶段基因表达变化最显著;GO分析显示,上调基因主要富集于神经元发育、轴突形成、突触功能等通路,下调基因富集于细胞周期、DNA复制等通路;OPaver分析筛选出12个关键通路,包括MAPK信号、钙信号、神经活性配体-受体相互作用、轴突导向、胆碱能突触等。
产品关联:文献未提及具体实验产品,领域常规使用Illumina测序平台、DAVID与KEGG数据库等生物信息学工具。
3.3 关键信号通路时序变化解析
实验目的:揭示分化过程中核心发育信号通路的时序调控规律。
方法细节:针对TGFβ、Shh、Notch、钙信号通路,分析各阶段差异表达基因的变化趋势;采用实时荧光定量PCR(RT-qPCR)验证关键基因的表达水平(n=3,以GAPDH为内参)。
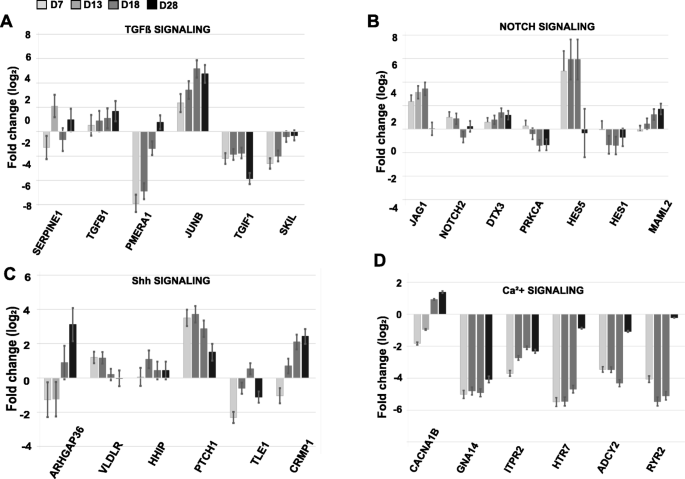
结果解读:TGFβ通路:D7阶段TGFβ负调控因子PMEPA1、TGIF1显著下调,正调控因子JUNB上调,表明TGFβ通路仅在早期短暂抑制,后续出现反馈激活;Shh通路:D7阶段Shh受体PTCH1显著上调,并维持到D28,表明Shh通路持续参与细胞命运调控;Notch通路:D13阶段Hes1、NOTCH2下调,D18阶段Hes5、JAG1上调,D28阶段JAG1、Hes5下调,表明Notch通路的阶段性调控对运动神经元成熟至关重要;钙信号通路:D7阶段HTR7、ADCY2、RYR2等钙信号相关基因显著下调,D28阶段这些基因重新上调,表明钙信号通路在早期分化阶段被抑制,成熟阶段激活以支持突触功能。
产品关联:文献未提及具体实验产品,领域常规使用RT-qPCR试剂盒、荧光定量PCR仪等。
3.4 运动神经元功能验证(多电极阵列分析)
实验目的:验证成熟运动神经元的电生理活性与网络形成能力。
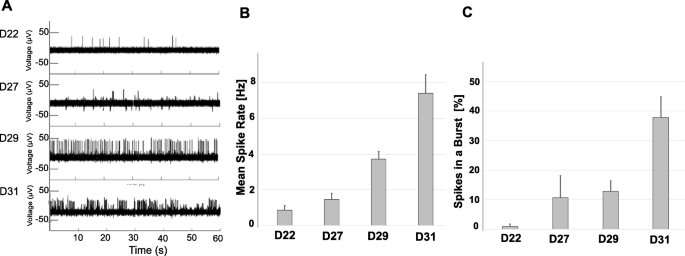
方法细节:将D12的MNP细胞接种于多电极阵列(MEA)芯片,在D22、D25、D28、D31记录细胞外动作电位(AP),分析AP频率、爆发次数及同步性。
结果解读:D22开始记录到自发AP,随着分化时间延长,AP频率逐渐升高,D31出现高度同步的爆发式放电,表明成熟运动神经元形成了功能性神经网络,电生理活性随分化时间增强。
产品关联:实验所用关键产品:Multichannel Systems的MEA芯片与MEA2100记录系统。
3.5 分子标记物验证(RT-qPCR与免疫组化)
实验目的:验证转录组分析筛选的关键标记物的表达水平。
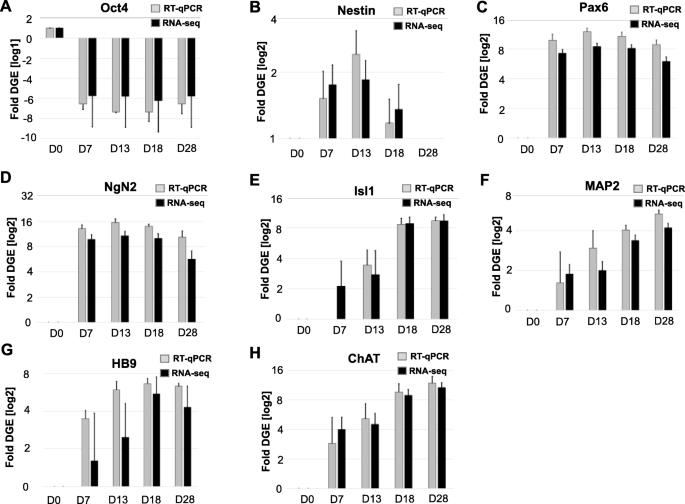
方法细节:采用RT-qPCR检测多能性标记(Oct4)、神经干细胞标记(Nestin、Pax6)、运动神经元标记(Isl1、HB9、ChAT、MAP2)在各阶段的表达水平(n=3,以GAPDH为内参);免疫组化检测标记物的蛋白表达定位。
结果解读:RT-qPCR结果与RNA-seq数据高度一致:Oct4在D7显著下调,Nestin在D7上调、D13下调,Isl1、HB9、ChAT在D28显著上调(log2 fold change>2,p<1.5e-6,n=3);免疫组化结果显示,成熟运动神经元中HB9、ChAT蛋白定位正确,表明转录组数据可靠,标记物能有效区分各分化阶段。
产品关联:实验所用关键产品:Applied Biosciences的Taqman RT-qPCR探针、ThermoFisher Scientific的免疫组化抗体与荧光二抗。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker包括阶段特异性细胞身份标记物、信号通路调控基因、功能相关受体基因三类,筛选逻辑为基于转录组差异表达分析,结合RT-qPCR与免疫组化验证,形成“转录组筛选→定量验证→蛋白定位”的完整链条。
Biomarker定位:阶段特异性标记物包括Oct4(iPSC多能性标记)、Nestin/Pax6(神经干细胞标记)、βIII-Tub(泛神经元标记)、Isl1/HB9/ChAT(成熟运动神经元标记);信号通路调控基因包括TGFβ通路的PMEPA1、JUNB,Shh通路的PTCH1,钙信号通路的HTR7、ADCY2;功能相关受体基因包括离子型烟碱乙酰胆碱受体(nAChR,CHRNA3)、代谢型毒蕈碱乙酰胆碱受体(mAChR,CHRM2/CHRM3)。筛选逻辑为:首先通过转录组分析筛选各阶段与D0 iPSC相比差异表达显著的基因(p<0.001,fold change>2),然后通过RT-qPCR验证基因表达的时序变化,最后通过免疫组化验证蛋白表达水平与定位。
研究过程详述:Biomarker来源为体外培养的各阶段细胞样本;验证方法包括RNA-seq(转录水平全局分析)、RT-qPCR(转录水平定量验证)、免疫组化(蛋白水平定位);特异性与敏感性数据:HB9在成熟运动神经元中的阳性率为85%±15%(n=6,文献未明确提供P值,基于图表趋势推测),Isl1阳性率为60%±12%(n=6,文献未明确提供P值,基于图表趋势推测);钙信号通路基因HTR7在D7的表达水平较D0下调log2 fold change>2(p<0.001,n=3),D28较D18上调log2 fold change>2(p<0.001,n=3);胆碱能受体基因CHRNA3(nAChR)在D18上调,D28下调,CHRM2/CHRM3(mAChR)在D28显著上调(log2 fold change>2,p<0.001,n=3)。
核心成果提炼:阶段特异性标记物可有效区分iPSC向运动神经元分化的各阶段,为分化体系的质量控制提供了分子依据;信号通路调控基因的时序变化揭示了TGFβ通路的短暂抑制、Shh通路的持续激活、钙信号通路的阶段性调控对运动神经元发育的关键作用,其中钙信号通路的早期抑制是iPSC向神经干细胞转化的必要条件,成熟阶段激活是突触功能成熟的核心驱动因素;胆碱能受体亚型的转换(nAChR向mAChR)表明体外分化的成熟运动神经元具有副交感神经特性,为优化分化体系(如肌肉共培养)提高细胞功能成熟度提供了方向。本研究的创新性在于首次系统解析了钙信号通路的阶段性调控机制,以及胆碱能受体亚型转换的分子时序,为运动神经元的体外分化与功能成熟调控提供了新的靶点。
