1. 领域背景与文献引入
文献英文标题:Apatinib induces endoplasmic reticulum stress-mediated apoptosis and autophagy and potentiates cell sensitivity to paclitaxel via the IRE-1α–AKT–mTOR pathway in esophageal squamous cell carcinoma;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:食管鳞状细胞癌靶向治疗与化疗增敏研究
食管鳞状细胞癌(ESCC)是东亚地区尤其是中国高发的恶性肿瘤,占中国食管癌病例的90%以上,每年新增病例超28万。尽管近年来诊断与治疗技术有所进步,但其5年生存率仍仅为15-20%,主要原因是多数患者确诊时已处于局部晚期或发生远处转移。手术是早期ESCC的主要治疗手段,而局部晚期患者需接受新辅助或辅助治疗,目前临床常用的围手术期化疗方案为铂类联合5-氟尿嘧啶或紫杉醇,但疗效仍有提升空间。在靶向治疗领域,仅3种药物(曲妥珠单抗、雷莫芦单抗、帕博利珠单抗)获FDA批准用于食管癌及胃食管结合部癌,多数靶向治疗策略仍处于基础或临床研究阶段。阿帕替尼作为新型血管内皮生长因子受体-2(VEGFR-2)酪氨酸激酶抑制剂,已获批用于晚期转移性胃癌的治疗,且在甲状腺癌、肝细胞癌等其他实体瘤中显示出显著的抗肿瘤增殖、诱导凋亡及增强化疗敏感性的作用。然而,阿帕替尼在ESCC中的作用机制仅被部分研究,其是否能增强ESCC细胞对紫杉醇的敏感性及相关分子机制尚未明确,这一研究空白限制了阿帕替尼在ESCC临床治疗中的应用,因此本研究旨在系统解析阿帕替尼对ESCC的抗肿瘤作用机制及化疗增敏效应。
2. 文献综述解析
作者对领域内现有研究的分类维度主要包括ESCC的临床治疗现状、阿帕替尼在不同实体瘤中的研究进展、内质网应激(ER应激)与自噬及凋亡的调控关系三个方面。现有研究显示,ESCC的治疗已进入化疗联合靶向治疗的时代,但获批的靶向治疗药物数量有限,多数靶向治疗仍处于探索阶段;阿帕替尼在胃癌、胆管癌、甲状腺癌等实体瘤中,可通过抑制血管生成、诱导细胞自噬、调控相关信号通路等方式发挥抗肿瘤作用,还能增强肿瘤细胞对紫杉醇、吉非替尼等化疗或靶向药物的敏感性,但在ESCC领域,仅少数研究报道阿帕替尼可通过Akt/β-catenin通路抑制肿瘤进展并增强顺铂敏感性,关于阿帕替尼诱导ER应激、自噬的具体机制,以及其对紫杉醇的增敏效应尚未见报道。同时,现有研究已证实ER应激与自噬、凋亡存在密切调控关系,自噬在ER应激下可发挥促生存或促死亡的双重作用,但在ESCC中,阿帕替尼诱导的ER应激如何调控自噬与凋亡的平衡仍不明确。本研究的创新价值在于,首次揭示了阿帕替尼通过IRE-1α–AKT–mTOR通路诱导ESCC细胞的ER应激、自噬与凋亡,明确了抑制自噬可增强阿帕替尼的促凋亡作用;同时首次证明阿帕替尼联合氯喹(CQ)可通过该通路显著增强ESCC细胞对紫杉醇的敏感性,填补了ESCC中阿帕替尼作用机制及化疗增敏研究的空白,为ESCC的新型治疗策略提供了实验依据。
3. 研究思路总结与详细解析
本研究的整体框架以“阿帕替尼对ESCC的抗肿瘤作用→机制解析→化疗增敏效应验证”为核心逻辑,研究目标是明确阿帕替尼在ESCC中的抗肿瘤作用机制及对紫杉醇的增敏效应,核心科学问题是阿帕替尼是否通过IRE-1α–AKT–mTOR通路调控ER应激、自噬与凋亡的平衡,以及联合自噬抑制剂能否增强其对紫杉醇的增敏作用,技术路线涵盖细胞实验、分子机制验证、动物实验的完整闭环。
3.1 ESCC细胞增殖、迁移与侵袭能力检测
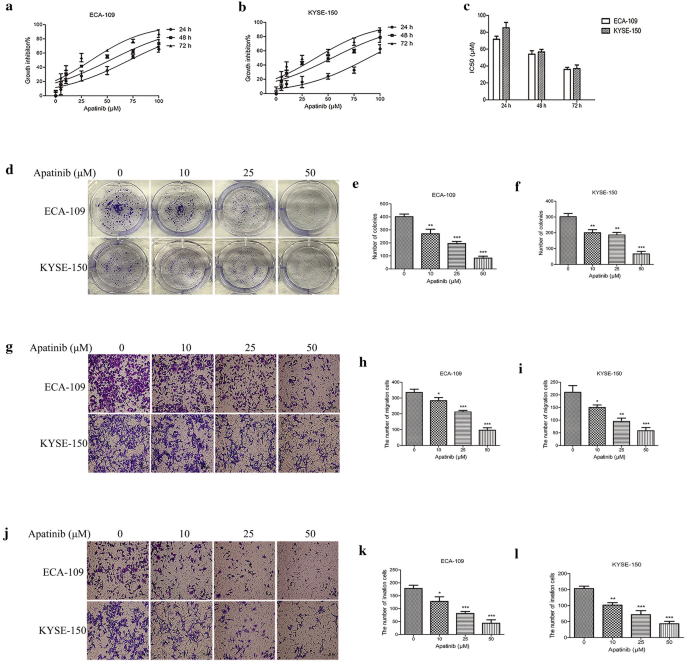
本环节的实验目的是验证阿帕替尼对ESCC细胞的体外抗肿瘤活性。实验方法为采用7种不同浓度的阿帕替尼处理ECA-109和KYSE-150两种ESCC细胞系,分别在3个时间点通过Cell Counting Kit-8(CCK-8)法检测细胞活力并计算半数抑制浓度(IC50);同时通过克隆形成实验检测细胞的长期增殖能力,Transwell实验检测细胞的迁移与侵袭能力。实验结果显示,阿帕替尼以剂量依赖的方式显著抑制ESCC细胞的活力,IC50值在两种细胞系中分别达到特定水平(n=3,P<0.05);克隆形成实验结果表明,阿帕替尼处理后细胞克隆形成数量显著减少(n=3,P<0.01);Transwell实验结果显示,阿帕替尼可显著降低ESCC细胞的迁移与侵袭能力(n=3,P<0.001)。实验所用关键产品:Cell Counting Kit-8(Dojindo, Kumamoto, Japan)、Transwell小室(领域常规使用Corning类产品)。
3.2 细胞周期阻滞与凋亡诱导效应验证
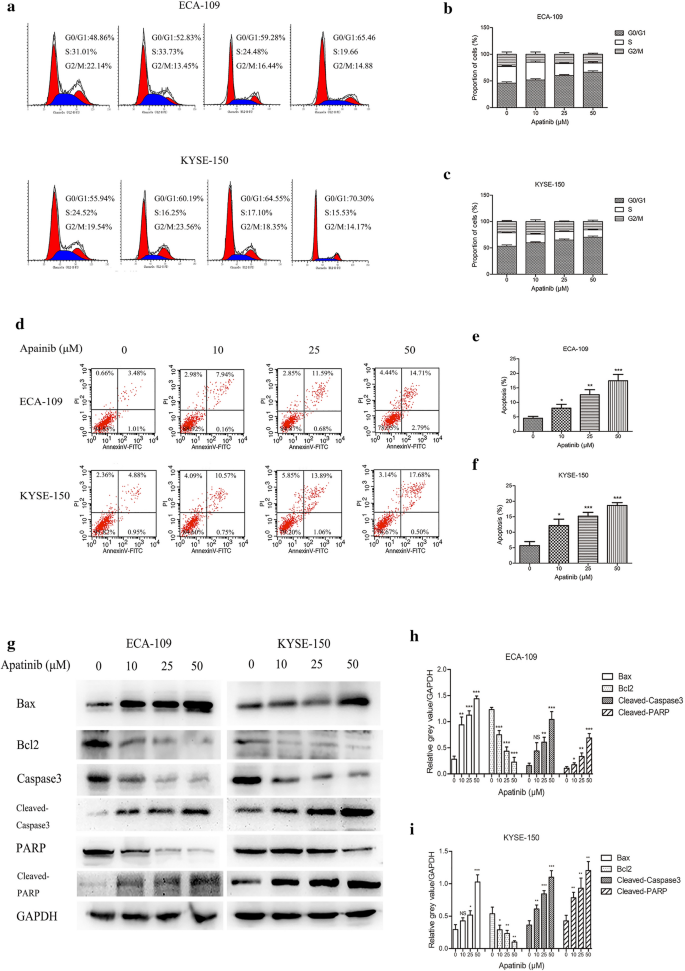
本环节的实验目的是探究阿帕替尼抑制ESCC细胞增殖的具体机制。实验方法为通过流式细胞术检测阿帕替尼处理后ESCC细胞的周期分布及凋亡率,采用蛋白质免疫印迹(Western blot)检测凋亡相关蛋白的表达水平。实验结果显示,阿帕替尼处理后,ESCC细胞被显著阻滞于G0/G1期,其中ECA-109细胞经25μM阿帕替尼处理后G0/G1期比例为59.89±1.61%,显著高于对照组的45.83±1.95%(n=3,P<0.01);流式细胞术检测结果表明,阿帕替尼可显著提高ESCC细胞的凋亡率(n=3,P<0.001);蛋白质免疫印迹结果显示,促凋亡蛋白Bax、活化的Caspase3(Cleaved-Caspase3)、活化的PARP(Cleaved-PARP)的表达水平显著上调,而抗凋亡蛋白Bcl2、总Caspase3、总PARP的表达水平显著下调(n=3,P<0.05)。实验所用关键产品:Annexin V-FITC/PI凋亡检测试剂盒(领域常规使用BD Biosciences类产品)、抗Bax、Bcl2等抗体(Cell Signaling Technology, Beverly, MA, USA)。
3.3 内质网应激与自噬激活的形态学及分子验证
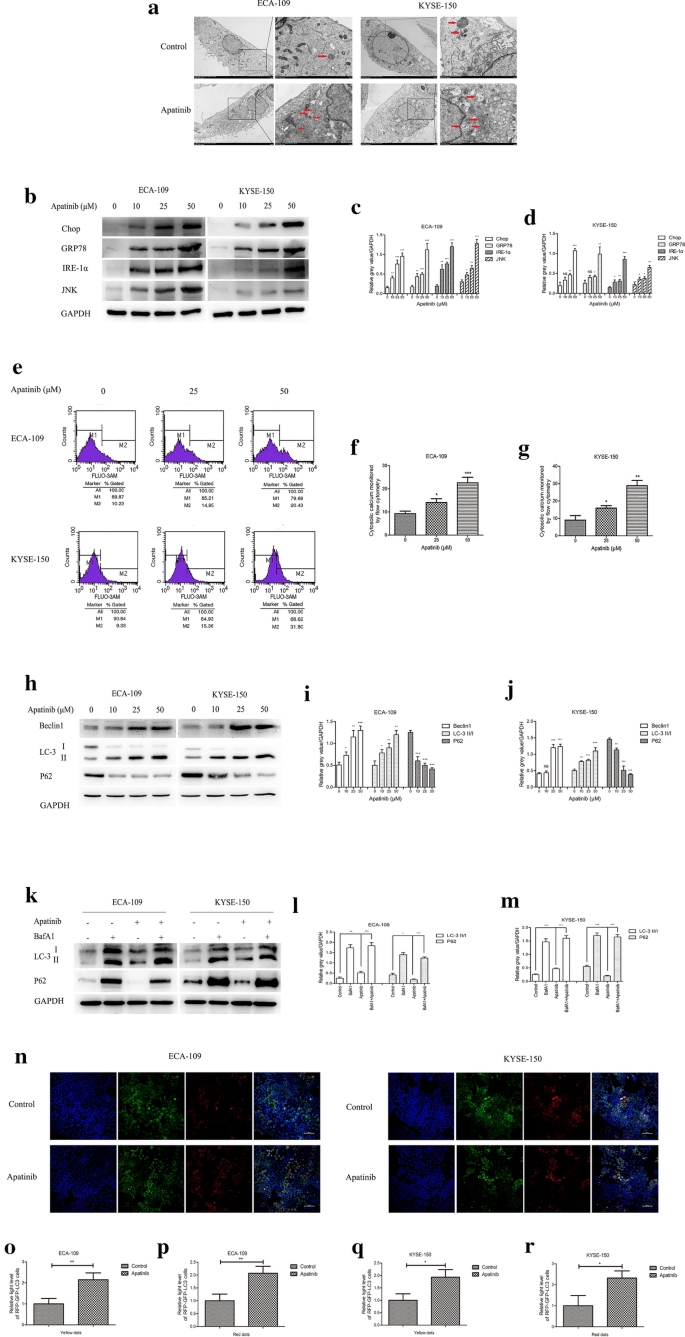
本环节的实验目的是明确阿帕替尼是否可诱导ESCC细胞发生ER应激与自噬。实验方法为通过透射电镜观察细胞超微结构变化,采用蛋白质免疫印迹检测ER应激标志物(Chop、GRP78、IRE-1α、JNK)及自噬标志物(LC3、Beclin1、P62)的表达水平,利用流式细胞术检测胞内钙离子(Ca²+)水平以验证ER应激的发生,通过RFP-GFP-LC3慢病毒转染检测自噬流的变化。实验结果显示,透射电镜下可见阿帕替尼处理后ESCC细胞的粗面内质网扩张、核糖体脱落,细胞质中形成更多自噬溶酶体,提示ER应激与自噬被激活;蛋白质免疫印迹结果显示,ER应激标志物的表达水平显著上调(n=3,P<0.01);胞内Ca²+水平显著升高(n=3,P<0.001),进一步证实ER应激的发生;自噬标志物检测结果显示,阿帕替尼处理后LC3-II/LC3-I比值升高、Beclin1表达上调、P62表达下调,联合自噬晚期抑制剂巴弗洛霉素A1(BafA1)后LC3-II的积累更为显著,RFP-GFP-LC3实验显示黄色自噬体与红色自噬溶酶体数量均显著增加,表明自噬流被增强(n=3,P<0.05)。实验所用关键产品:Fluo3 AM(Beyotime, Shanghai, China)、RFP-GFP-hLC3慢病毒(Jiman, Shanghai)、透射电镜(领域常规使用Zeiss类产品)。
3.4 IRE-1α–AKT–mTOR通路的调控机制验证
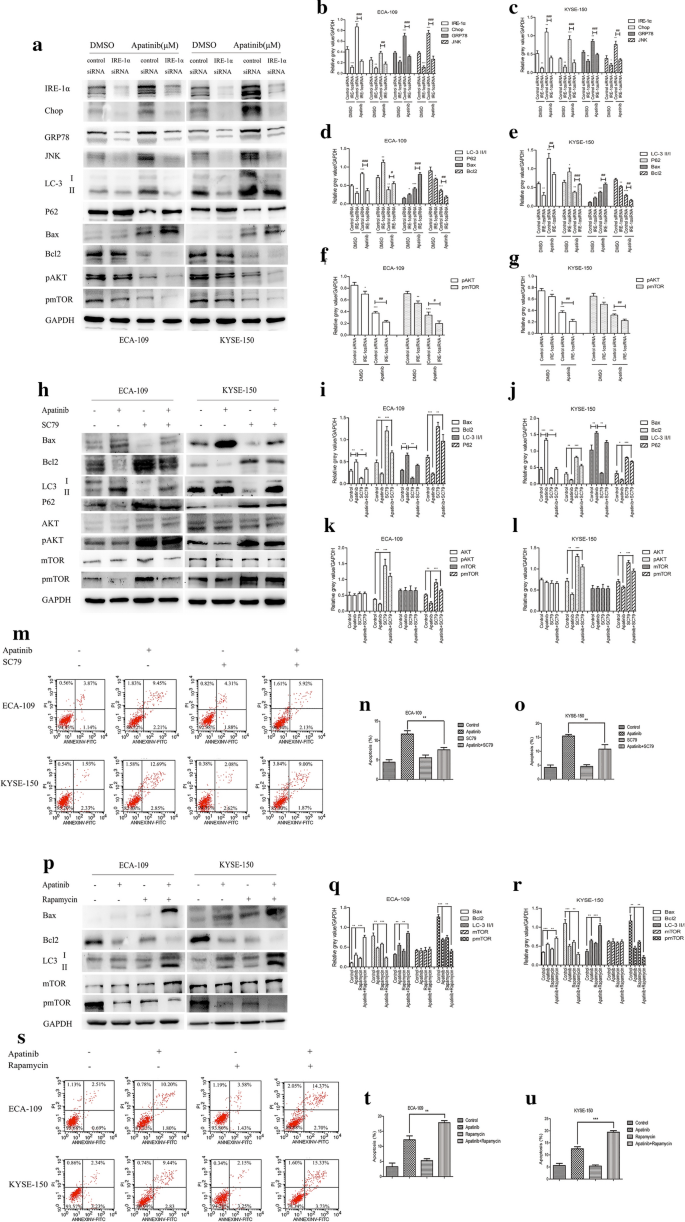
本环节的实验目的是解析阿帕替尼调控ER应激、自噬与凋亡的核心信号通路。实验方法为采用IRE-1α小干扰RNA(siRNA)转染ESCC细胞以敲低IRE-1α表达,同时使用AKT激活剂SC79、mTOR抑制剂雷帕霉素处理细胞,通过蛋白质免疫印迹检测通路相关蛋白及自噬、凋亡相关蛋白的表达水平,流式细胞术检测细胞凋亡率。实验结果显示,敲低IRE-1α可显著抑制阿帕替尼诱导的ER应激、自噬相关蛋白的表达,同时显著下调磷酸化AKT(pAKT)与磷酸化mTOR(pmTOR)的水平(n=3,P<0.05);SC79处理可逆转阿帕替尼诱导的促凋亡蛋白上调与自噬激活,而雷帕霉素处理则进一步增强阿帕替尼的促凋亡与自噬诱导作用(n=3,P<0.01)。上述结果证实,IRE-1α–AKT–mTOR通路是阿帕替尼调控ESCC细胞ER应激、自噬与凋亡的关键通路。实验所用关键产品:IRE-1α siRNA(BioeGene, Shanghai, China)、SC79、雷帕霉素(Selleck Chemicals, Houston, TX, USA)。
3.5 自噬抑制增强阿帕替尼促凋亡作用的验证
本环节的实验目的是明确自噬在阿帕替尼诱导ESCC细胞凋亡中的作用。实验方法为采用Beclin1 siRNA转染ESCC细胞以抑制自噬核心分子表达,或使用自噬抑制剂氯喹(CQ)预处理细胞,通过蛋白质免疫印迹检测凋亡相关蛋白的表达水平,流式细胞术检测细胞凋亡率,RFP-GFP-LC3慢病毒转染检测自噬流的变化。实验结果显示,敲低Beclin1后,阿帕替尼诱导的促凋亡蛋白Bax表达显著上调,抗凋亡蛋白Bcl2表达显著下调(n=3,P<0.05);CQ预处理可显著抑制自噬流(黄色自噬体数量增加、红色自噬溶酶体数量减少),同时显著增强阿帕替尼诱导的ESCC细胞凋亡率(n=3,P<0.001),且联合处理后pAKT与pmTOR的表达水平进一步下调(n=3,P<0.01)。上述结果表明,阿帕替尼诱导的自噬具有促细胞生存的作用,抑制自噬可增强其促凋亡效应。实验所用关键产品:Beclin1 siRNA(BioeGene, Shanghai, China)、氯喹(Selleck Chemicals, Houston, TX, USA)。
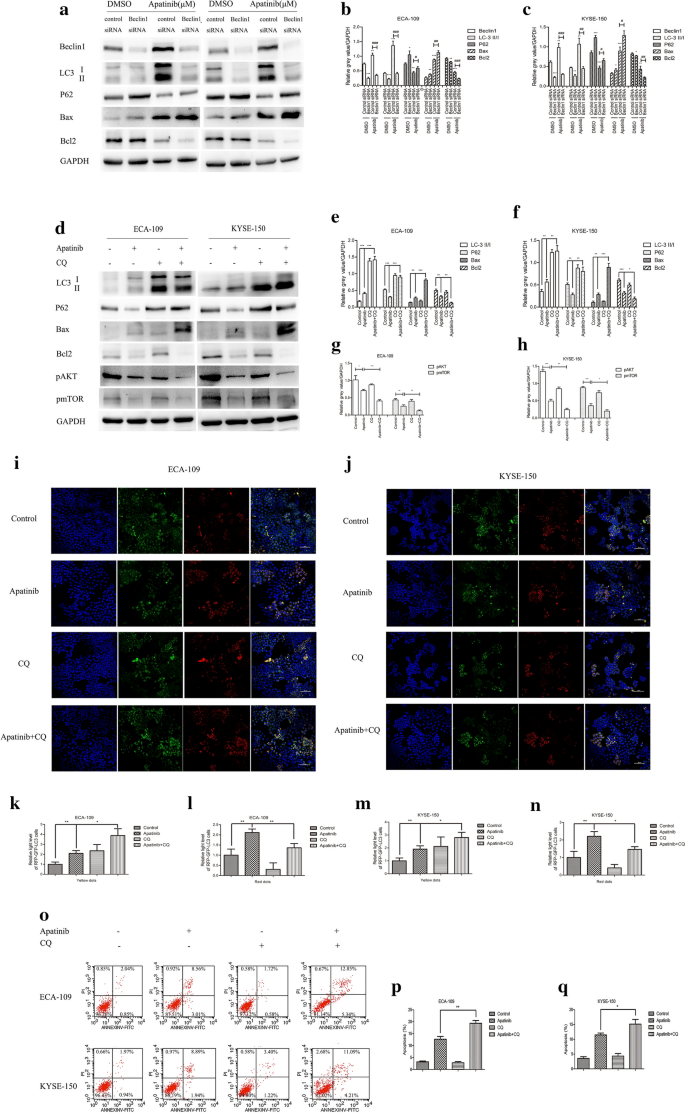
3.6 阿帕替尼联合氯喹增强ESCC细胞对紫杉醇敏感性的体外验证
本环节的实验目的是验证阿帕替尼联合CQ是否可增强ESCC细胞对紫杉醇的敏感性。实验方法为采用不同浓度的紫杉醇单独或联合阿帕替尼与CQ处理ESCC细胞,通过CCK-8法检测细胞活力并计算紫杉醇的IC50值,克隆形成实验检测细胞增殖能力,流式细胞术检测细胞凋亡率,蛋白质免疫印迹检测通路及凋亡相关蛋白的表达水平。实验结果显示,阿帕替尼联合CQ可显著降低紫杉醇的IC50值,增强紫杉醇对ESCC细胞增殖的抑制作用(n=3,P<0.001);同时显著提高紫杉醇诱导的细胞凋亡率(n=3,P<0.01);蛋白质免疫印迹结果显示,联合处理后促凋亡蛋白Bax、Cleaved-Caspase3表达显著上调,抗凋亡蛋白Bcl2及通路分子pAKT、pmTOR表达显著下调(n=3,P<0.05)。实验所用关键产品:紫杉醇(Selleck Chemicals, Houston, TX, USA)。
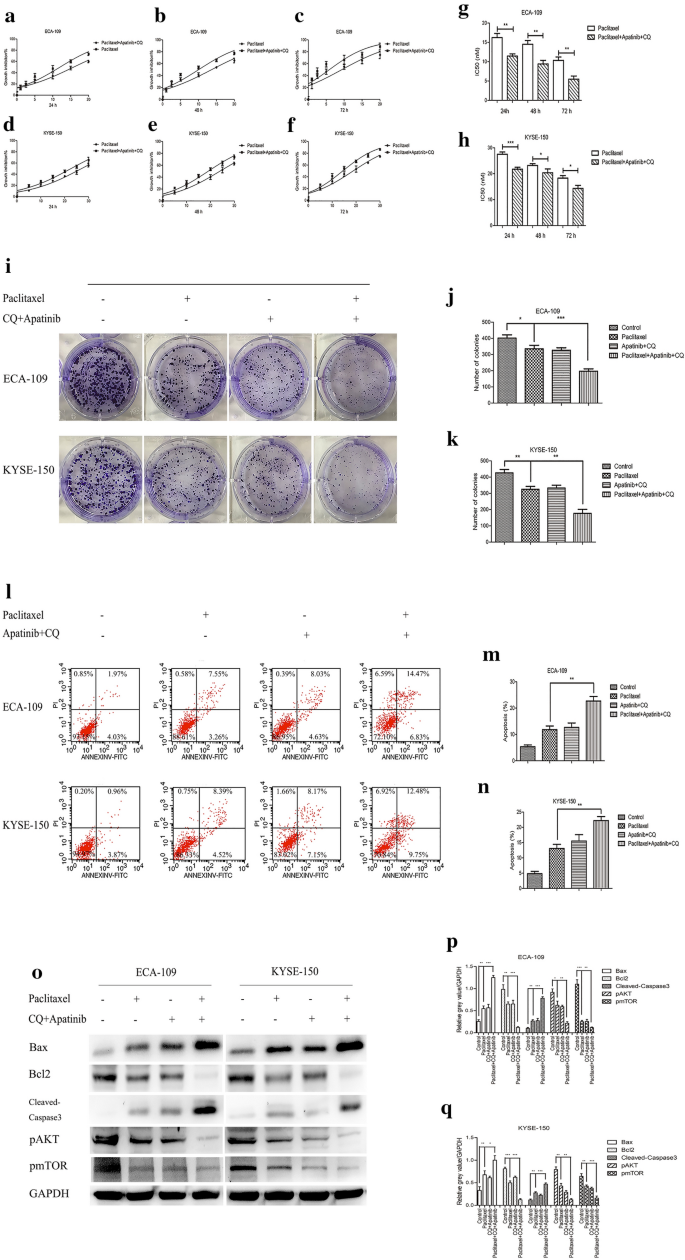
3.7 IRE-1α–AKT–mTOR通路介导化疗增敏的机制验证
本环节的实验目的是明确阿帕替尼联合CQ增敏紫杉醇的核心分子通路。实验方法为采用IRE-1α siRNA转染ESCC细胞,或使用AKT激活剂SC79、mTOR抑制剂雷帕霉素处理细胞,通过蛋白质免疫印迹检测通路及凋亡相关蛋白的表达水平,流式细胞术检测细胞凋亡率。实验结果显示,敲低IRE-1α可显著逆转阿帕替尼联合CQ对紫杉醇的增敏效应(n=3,P<0.05);SC79处理可抑制联合治疗诱导的促凋亡蛋白表达上调,而雷帕霉素处理则进一步增强该效应(n=3,P<0.01)。上述结果证实,IRE-1α–AKT–mTOR通路是阿帕替尼联合CQ增敏紫杉醇的核心调控通路。
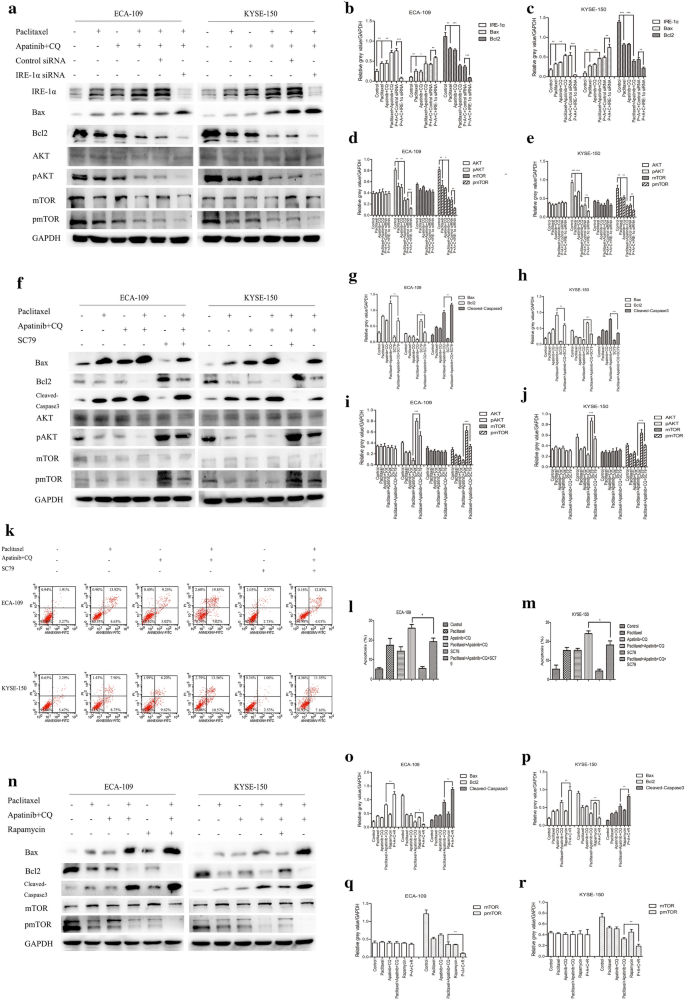
3.8 体内移植瘤模型验证联合治疗的抗肿瘤效应
本环节的实验目的是在体内水平验证阿帕替尼联合CQ增强紫杉醇抗肿瘤效应的作用。实验方法为构建ECA-109细胞裸鼠皮下移植瘤模型,将裸鼠随机分为6组(对照组、CQ组、阿帕替尼组、阿帕替尼+CQ组、紫杉醇组、紫杉醇+阿帕替尼+CQ组),给药4周后测量肿瘤体积与重量,通过免疫组化检测肿瘤组织中Ki67(增殖标志物)、Cleaved-Caspase3(凋亡标志物)的表达水平,采用TUNEL法检测肿瘤组织的凋亡率。实验结果显示,阿帕替尼+CQ组的肿瘤体积与重量显著低于阿帕替尼单药组(体积307.00±42.01 mm³ vs 693.33±67.99 mm³,n=6,P<0.01;重量533.33±108.73 mg vs 906.67±70.40 mg,n=6,P<0.05);紫杉醇+阿帕替尼+CQ组的肿瘤体积与重量显著低于紫杉醇单药组(体积86.83±24.29 mm³ vs 417.33±24.78 mm³,n=6,P<0.001;重量192.33±27.88 mg vs 570.00±106.14 mg,n=6,P<0.01);免疫组化结果显示,联合治疗组Ki67表达显著下调,Cleaved-Caspase3表达显著上调,TUNEL法检测的凋亡率显著升高(n=6,P<0.001)。实验所用关键产品:裸鼠(中国科学院上海动物研究所)、TUNEL检测试剂盒(Roche Applied Science, USA)。
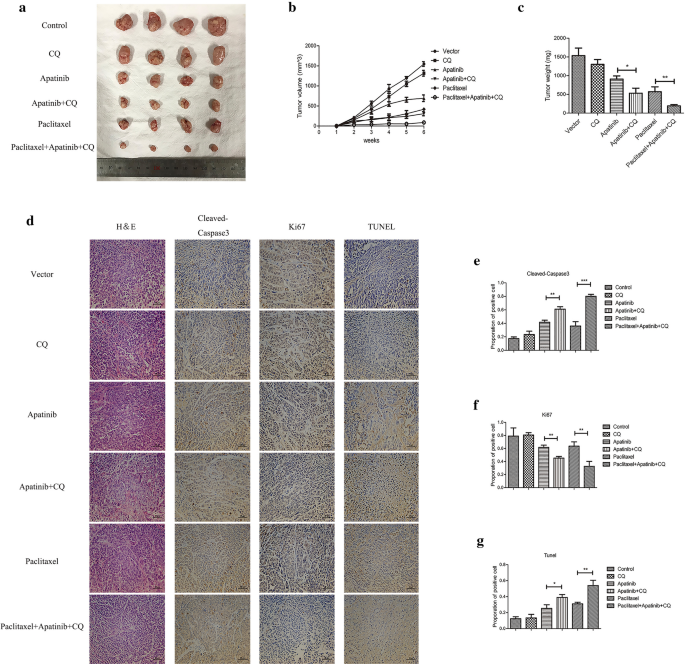
4. Biomarker研究及发现成果
本研究涉及的核心生物标志物包括ER应激相关标志物(IRE-1α、Chop、GRP78)、信号通路标志物(pAKT、pmTOR)、凋亡相关标志物(Bax、Bcl2、Cleaved-Caspase3)及自噬相关标志物(LC3、Beclin1、P62)。这些生物标志物的筛选与验证逻辑为:首先通过阿帕替尼处理ESCC细胞后的分子表达变化初步筛选出差异表达分子,随后通过siRNA敲低、通路激活剂/抑制剂处理验证其在阿帕替尼调控ER应激、自噬与凋亡中的功能,最后通过体内移植瘤模型验证其在联合治疗中的作用。
研究过程中,这些生物标志物的来源为ESCC细胞系及裸鼠移植瘤组织,验证方法包括蛋白质免疫印迹、免疫组化、流式细胞术、TUNEL法等。其中,IRE-1α作为ER应激的关键分子,其表达上调是阿帕替尼诱导后续通路激活的起始事件,敲低IRE-1α可显著抑制阿帕替尼的抗肿瘤效应(n=3,P<0.05);pAKT与pmTOR作为通路下游分子,其活性变化直接调控自噬与凋亡的平衡,抑制其活性可增强阿帕替尼的促凋亡作用;Bax、Bcl2作为凋亡调控的核心分子,其表达比值可直接反映细胞的凋亡状态,阿帕替尼联合治疗后Bax/Bcl2比值显著升高(n=3,P<0.01)。
核心研究成果为:明确了IRE-1α–AKT–mTOR通路是阿帕替尼调控ESCC细胞ER应激、自噬与凋亡的关键通路,同时也是阿帕替尼联合CQ增强ESCC细胞对紫杉醇敏感性的核心机制;该通路中的IRE-1α、pAKT、pmTOR及凋亡相关分子Bax、Bcl2可作为ESCC靶向治疗联合化疗的潜在生物标志物,为ESCC的个体化治疗提供了新的靶点与策略。此外,本研究首次证实抑制自噬可增强阿帕替尼对ESCC的促凋亡作用,为ESCC的自噬靶向治疗提供了实验依据。
