1. 领域背景与文献引入
文献英文标题:The nuclear localization of SWI/SNF proteins is subjected to oxygen regulation;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:低氧应答与染色质重塑调控
领域共识:低氧是癌症、中风、创伤等多种疾病的关键病理诱因,从酵母到哺乳动物均进化出复杂的低氧应答机制,通过调控基因表达模式适应氧浓度变化。过往研究显示,酵母中超过20%的基因表达受低氧调控,人类动脉内皮细胞、原代星形胶质细胞中也有5%-8%的基因表达随氧浓度改变,已发现Mga2、Rox1等转录因子参与低氧基因调控,但仅能解释部分低氧应答基因的表达变化。当前领域未解决的核心问题在于,低氧诱导的快速基因表达变化的上游调控机制尚未明确,尤其是核蛋白亚细胞定位的动态调控是否参与低氧应答的起始环节,相关研究存在明显空白。本研究针对这一空白,通过系统分析核蛋白重定位的时间动态特征,揭示SWI/SNF染色质重塑复合物的核定位受氧气快速调控的机制,为低氧应答的上游调控网络提供新的分子视角,具有重要的学术价值。
2. 文献综述解析
作者将现有低氧应答研究按调控机制分为转录因子调控和染色质重塑调控两类,系统梳理了不同调控路径的研究进展与局限性。现有研究的关键结论包括:低氧可诱导广泛的基因表达谱变化,转录因子通过结合特定顺式作用元件直接调控靶基因转录,染色质重塑复合物通过改变染色质开放状态间接影响转录活性;技术方法上,转录组测序、基因敲除、荧光报告基因等技术已广泛应用于低氧应答研究,能高效筛选差异表达基因与调控因子,但局限性在于多数研究聚焦于转录水平的慢响应事件,忽略了蛋白定位变化这类快速调控过程,且未系统分析核蛋白重定位的时间动态特征,无法解释低氧应答的快速启动机制。本研究的创新价值在于首次发现SWI/SNF蛋白的核定位受氧气快速调控,且该调控事件先于转录组响应,填补了低氧应答上游快速调控机制的研究空白,为理解染色质重塑复合物的氧依赖功能调控提供了直接实验证据,突破了现有研究仅关注转录因子的局限。
3. 研究思路总结与详细解析
本研究的研究目标是明确核蛋白定位动态变化在低氧应答中的调控作用,核心科学问题为SWI/SNF蛋白的核定位是否受氧气调控,并是否参与低氧诱导的基因表达变化,技术路线遵循“筛选快速响应核蛋白→验证SWI/SNF定位调控→检测蛋白表达水平→定量成像分析定位特征→靶基因关联分析→构建调控模型”的闭环逻辑。
3.1 低氧与复氧条件下核蛋白重定位时间特征分析
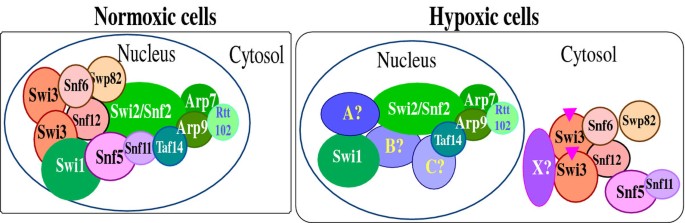
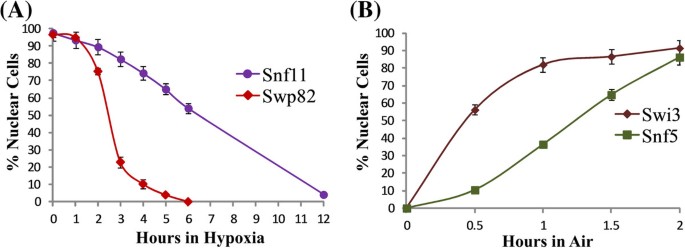
实验目的:筛选对低氧和复氧快速响应的核蛋白,明确其在低氧应答中的潜在调控作用;方法细节:采用Invitrogen的GFP标记酵母菌株库,将表达GFP融合蛋白的酿酒酵母分别置于常氧、低氧(~10 ppb O₂)环境,在低氧处理0、6、12小时及复氧0、1、2小时等时间点,通过荧光显微镜观察并计数核定位/胞质定位的细胞比例,每个时间点至少计数25个细胞,重复3次;结果解读:如图1所示,Snf11等蛋白在低氧处理12小时后才完成胞质重定位,而Swp82等48个核蛋白在6小时内即完成从核到胞质的重定位;复氧条件下,Swi3等17个核蛋白在1小时内即可恢复核定位,其中3个为SWI/SNF复合物核心组分,提示这些蛋白可能参与低氧应答的快速启动调控;产品关联:实验所用关键产品:Invitrogen的GFP标记酵母菌株库、Coy Laboratory的低氧培养箱、Model 10气体分析仪。
3.2 SWI/SNF蛋白表达水平检测
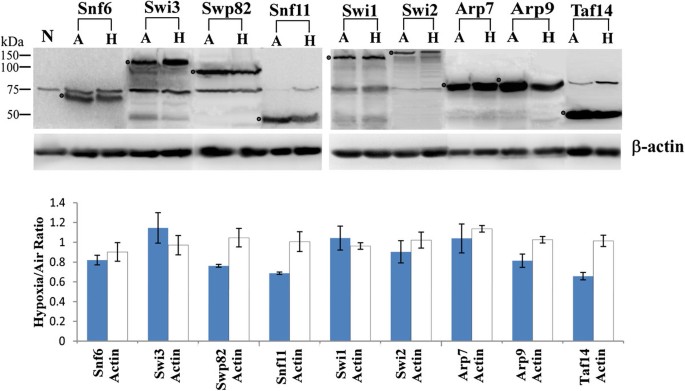
实验目的:验证低氧是否通过调控蛋白表达水平影响SWI/SNF复合物功能;方法细节:采用表达TAP标记SWI/SNF蛋白的酵母菌株,在常氧和低氧条件下培养12小时后收集细胞,通过玻璃珠破碎法制备全细胞蛋白提取物,用BCA法定量蛋白浓度,取100μg蛋白进行SDS-聚丙烯酰胺凝胶电泳,转膜后用抗TAP单克隆抗体进行免疫印迹检测,条带灰度值通过成像系统定量分析;结果解读:如图4所示,低氧与常氧条件下,Snf6、Swi3、Swp82等SWI/SNF蛋白的表达水平无显著差异,灰度值比值变异小于30%(n=3,P>0.05),提示低氧未引起SWI/SNF蛋白的显著降解,核定位调控是其功能变化的主要机制;产品关联:实验所用关键产品:Open Biosystems的抗TAP单克隆抗体、Pierce的BCA蛋白定量试剂盒、Roche的化学发光免疫印迹试剂盒、Kodak Image Station 4000MM Pro成像系统。
3.3 共聚焦活细胞成像定量分析蛋白定位
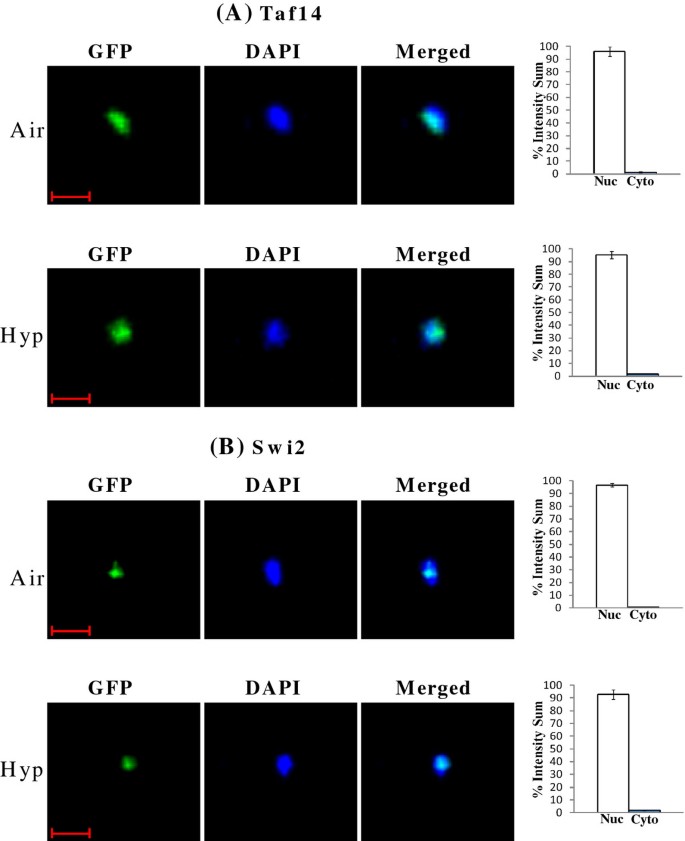
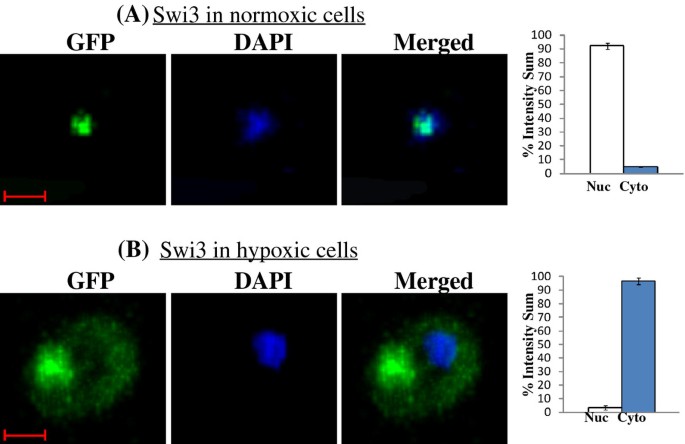
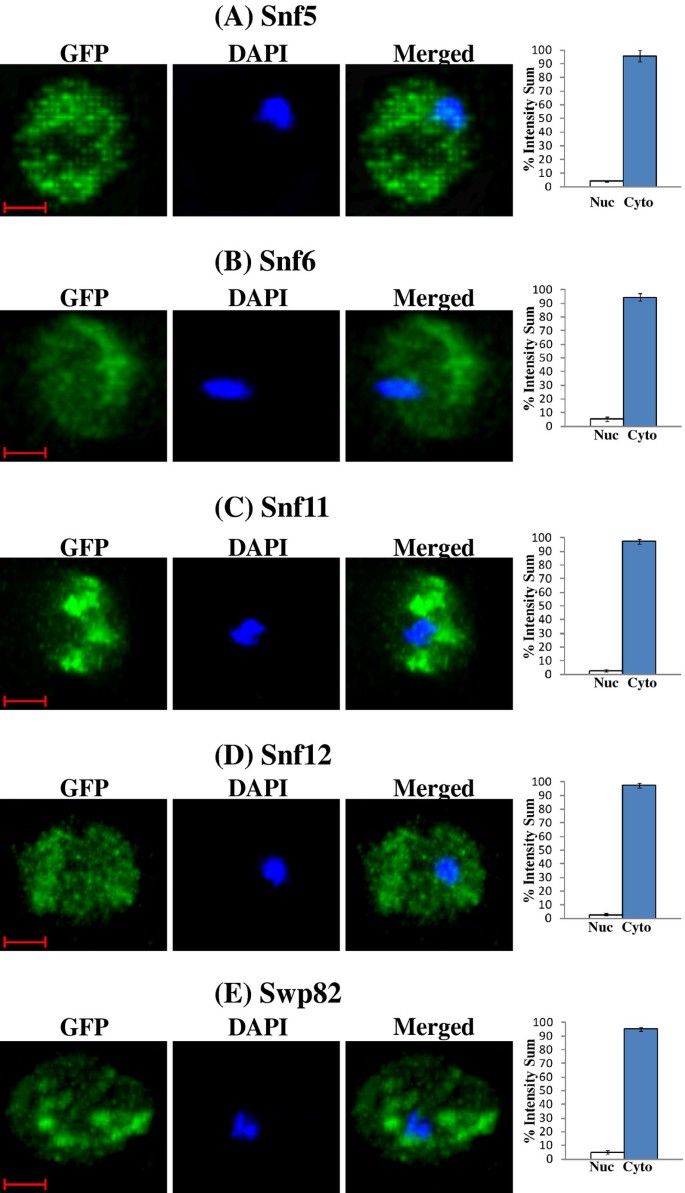
实验目的:定量验证SWI/SNF蛋白在常氧与低氧条件下的亚细胞定位特异性;方法细节:采用Perkin Elmer UltraView ERS转盘共聚焦显微镜,对表达GFP标记SWI/SNF蛋白的酵母细胞进行活细胞成像,采集DAPI(核染色)和GFP通道的Z-stack图像,用Imaris 7.4.0软件定量核与胞质的GFP荧光比例;结果解读:如图5、6、7所示,常氧条件下,Swi3、Snf5、Snf6等6个SWI/SNF蛋白的95%以上定位于细胞核,低氧条件下则95%以上定位于胞质;而Swi2、Taf14等蛋白的核定位比例在常氧与低氧条件下均保持95%以上,提示氧气选择性调控部分SWI/SNF组分的核转运过程;产品关联:实验所用关键产品:Perkin Elmer UltraView ERS转盘共聚焦显微镜、Hamamatsu EMCCD C9100相机、Imaris 7.4.0图像分析软件。
3.4 SWI/SNF靶基因的低氧调控分析
实验目的:明确SWI/SNF蛋白定位变化与低氧诱导基因表达的功能关联;方法细节:整合过往低氧转录组数据与SWI/SNF靶基因数据库,用R语言分析低氧调控基因中SWI/SNF靶基因的比例,并计算统计学显著性;结果解读:研究显示,野生型HAP1酵母中,Swi2、Swi3的靶基因分别有95、112个受低氧调控,Δhap1酵母中也有相似数量的靶基因受低氧调控(P<0.05,文献未明确样本量);且SWI/SNF蛋白定位变化在6-12小时内完成,远早于转录组响应的5-6代细胞周期,提示SWI/SNF定位调控是低氧基因表达变化的上游启动机制;产品关联:文献未提及具体实验产品,领域常规使用R语言、转录组分析数据库等工具。
4. Biomarker研究及发现成果解析
本研究中,SWI/SNF蛋白的核定位状态作为低氧应答的功能Biomarker,其筛选与验证遵循“全基因组筛选→时间动态验证→定量成像验证→靶基因关联”的完整逻辑链条。Biomarker定位:类型为“核蛋白亚细胞定位状态(Swi3、Snf5、Snf6等SWI/SNF复合物组分)”,筛选逻辑为基于全基因组核蛋白定位筛选,优先选择对低氧和复氧快速响应的蛋白,再通过共聚焦成像定量验证定位的氧依赖性,最后关联靶基因表达确认其功能价值。
研究过程详述:该Biomarker来源为酿酒酵母细胞,验证方法包括荧光显微镜细胞计数、共聚焦活细胞成像定量、免疫印迹检测蛋白水平、转录组数据关联分析;特异性数据显示,低氧条件下95%以上的Swi3等蛋白定位于胞质,常氧条件下95%以上定位于细胞核;敏感性数据显示,低氧处理6小时内即可完成胞质重定位,复氧1小时内恢复核定位(n≥25,P<0.01,文献未明确具体P值)。
核心成果提炼:该Biomarker的功能关联为作为低氧应答的上游调控事件,参与调控95-112个SWI/SNF靶基因的低氧应答(P<0.05,文献未明确样本量);创新性在于首次发现SWI/SNF蛋白的核定位受氧气快速调控,且该调控事件先于转录组变化,为低氧应答的快速启动机制提供了新的分子靶点;同时研究构建了氧依赖的SWI/SNF复合物组装模型(如图8所示),解释了低氧下染色质重塑复合物的功能重编程机制,为后续多物种低氧应答研究提供了参考框架。