1. 领域背景与文献引入
文献英文标题:Biologically active, high levels of interleukin-22 inhibit hepatic gluconeogenesis but do not affect obesity and its metabolic consequences;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:代谢综合征与细胞因子调控。
代谢综合征以肥胖、胰岛素抵抗、高血糖等为核心特征,是全球范围内导致心血管疾病、糖尿病的重要危险因素,其发病机制涉及遗传、环境及免疫代谢网络的复杂调控。白细胞介素22(IL-22)作为IL-10家族的重要细胞因子,主要由Th17、Th22等免疫细胞分泌,通过结合上皮细胞表面的IL-22R1发挥抗感染、组织修复等功能。近年研究显示IL-22参与代谢调控,但结果存在显著争议:部分研究认为高剂量IL-22可改善肥胖小鼠的体重及胰岛素抵抗,另一些研究则显示IL-22仅改善脂肪肝,对体重无影响,甚至有研究认为IL-22可促进脂肪组织炎症、降低胰岛素敏感性。目前核心未解决问题是生理相关浓度的IL-22对肥胖及代谢综合征的真实作用尚不明确,其调控糖代谢的分子机制也未完全解析,因此本研究针对这一领域空白,系统验证IL-22在代谢中的作用及机制。
2. 文献综述解析
作者按IL-22的浓度水平、给药方式及实验模型对现有研究进行分类评述,明确不同研究结果差异的关键原因在于IL-22浓度的差异,以及实验模型的选择。
现有研究中,超高水平IL-22(如腺病毒介导的4000-7000pg/ml循环浓度)可导致瘦小鼠体重下降、胸腺萎缩,推测可能引发恶病质;高剂量长半衰期IL-22Fc蛋白(50-100μg/小鼠,每周两次)可降低瘦素受体缺陷肥胖小鼠的体重,改善高血糖及胰岛素抵抗;低剂量重组IL-22(20-100ng/g体重,每周两次)可改善高脂饮食诱导肥胖小鼠的代谢并发症;但也有研究显示慢性重组IL-22处理(300ng/g体重,每日一次)仅改善高脂饮食小鼠的脂肪肝,对体重、空腹血糖及胰岛素水平无影响;此外,人体研究显示T细胞来源的IL-22可放大脂肪组织IL-1β介导的炎症反应,降低肝细胞胰岛素敏感性,促进肥胖及糖尿病发生。现有研究的局限性在于多数研究使用的IL-22浓度远超生理水平(健康人血清IL-22通常低于200pg/ml),缺乏对生理相关浓度IL-22代谢调控作用的系统研究,且对IL-22调控糖代谢的分子机制解析不充分,导致研究结论存在争议。
本研究的创新价值在于使用生理相关的较高浓度IL-22(~600pg/ml,接近病理状态但未达恶病质水平),通过基因敲除、转基因动物模型及重组蛋白处理,系统验证IL-22对肥胖及代谢综合征的影响,澄清了领域内的争议;同时首次明确IL-22通过STAT3和AMPK信号通路抑制肝糖异生的分子机制,弥补了现有研究的不足。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确生理相关浓度IL-22对肥胖及代谢综合征的调控作用,解析其影响肝糖代谢的分子机制;核心科学问题包括内源性及外源性IL-22是否参与高脂饮食诱导的肥胖及胰岛素抵抗,以及IL-22调控肝糖异生的关键信号通路;技术路线遵循“动物模型验证→细胞实验解析→信号通路验证”的闭环逻辑,通过多层面实验系统验证研究假设。
3.1 内源性IL-22对高脂饮食诱导肥胖的调控作用验证
实验目的:明确内源性低水平IL-22是否参与高脂饮食(HFD)诱导的肥胖、胰岛素抵抗及脂肪肝的发生发展。
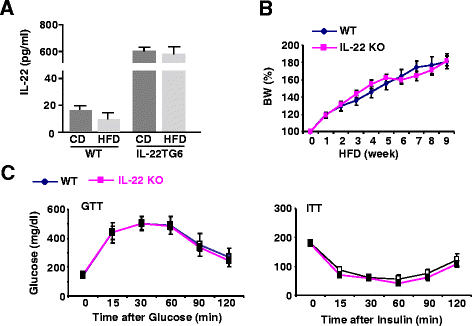
方法细节:通过杂交IL-22杂合子小鼠获得野生型(WT)和IL-22基因敲除(KO)同窝小鼠,8-10周龄小鼠分别饲喂对照饮食(CD)或HFD10周,每周监测体重,饲喂结束后进行葡萄糖耐量试验(GTT)和胰岛素耐量试验(ITT),采用ELISA检测血清IL-22水平,通过苏木精-伊红(H&E)染色及肝甘油三酯检测评估肝脂肪变性程度。
结果解读:血清IL-22检测显示,CD和HFD饲喂的WT小鼠血清IL-22水平均低于20pg/ml,HFD饲喂后无显著变化;IL-22KO小鼠与WT小鼠在HFD饲喂后,体重增长、葡萄糖不耐受程度、胰岛素抵抗水平均无显著差异(n=6-12),肝脂肪变性及甘油三酯水平也无显著差异,说明内源性低水平IL-22不参与HFD诱导的肥胖及代谢综合征的发病过程。
产品关联:文献未提及具体实验产品,领域常规使用ELISA试剂盒检测细胞因子、全自动生化分析仪检测血清酶学指标、组织病理染色评估肝损伤。
3.2 高浓度IL-22转基因小鼠的代谢表型及肝损伤抗性验证
实验目的:明确生理相关高浓度IL-22对肥胖及代谢综合征的影响,同时验证转基因小鼠中IL-22的生物学活性。
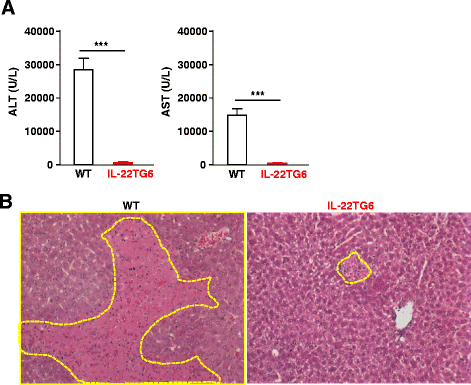
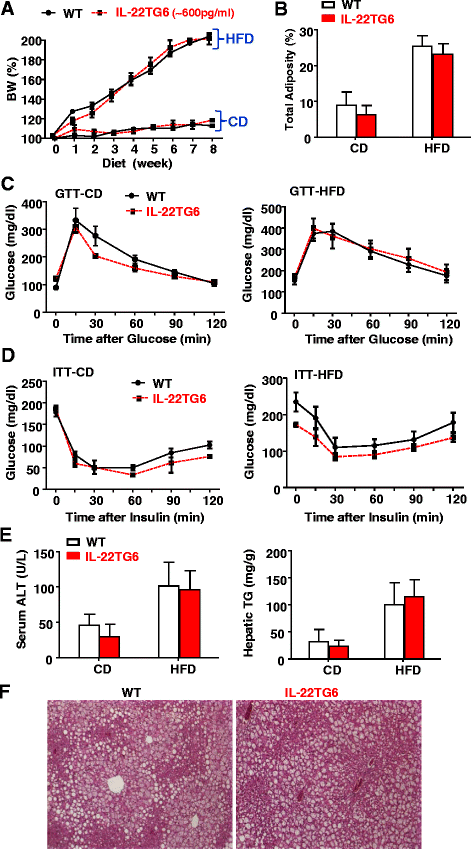
方法细节:构建白蛋白启动子驱动的IL-22转基因(TG6)小鼠,其循环IL-22浓度约600pg/ml,与WT同窝对照小鼠分别饲喂CD或HFD8周,监测体重、体脂率,进行GTT和ITT,检测血清ALT、AST及肝甘油三酯水平;同时通过刀豆蛋白A(Con A)诱导肝损伤,检测血清ALT、AST及肝组织病理变化,验证IL-22的生物学活性。
结果解读:Con A处理后,WT小鼠血清ALT、AST显著升高(n=10-14,P<0.001),肝组织出现大量坏死区域,而IL-22TG6小鼠无明显肝损伤,证明其体内IL-22具有生物学活性;HFD饲喂后,IL-22TG6小鼠与WT小鼠的体重增长、体脂率、葡萄糖耐量、胰岛素敏感性、肝脂肪变性程度均无显著差异(n=6-14),说明高浓度IL-22不影响HFD诱导的肥胖及代谢综合征。
产品关联:实验所用关键产品:R&D Systems的重组小鼠IL-22蛋白、Cell Signaling Technology的磷酸化STAT3抗体、ELISA试剂盒检测血清IL-22。
3.3 慢性重组IL-22处理对肥胖小鼠代谢的影响验证
实验目的:明确慢性外源性IL-22处理是否改善高脂饮食诱导肥胖小鼠的代谢综合征。
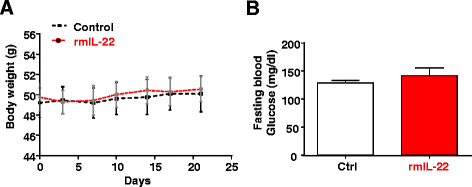
方法细节:高脂饮食饲喂5个月的小鼠,每周两次腹腔注射重组IL-22(20ng/g体重)或生理盐水,持续4周,每周监测体重,实验结束后检测空腹血糖水平。
结果解读:慢性IL-22处理后,小鼠的体重增长及空腹血糖水平与生理盐水处理组无显著差异(n=8),说明慢性外源性IL-22处理不改善高脂饮食诱导的肥胖及高血糖。
产品关联:同上述重组IL-22蛋白产品。
3.4 单次IL-22处理对高血糖模型小鼠糖代谢的调控作用
实验目的:明确IL-22对急性糖代谢的调控作用,以及是否影响胰岛素分泌。
方法细节:高脂饮食饲喂8周的小鼠或链脲佐菌素(STZ)诱导的1型糖尿病小鼠,单次腹腔注射重组IL-22(1000ng/g体重),注射后2小时检测空腹血糖水平,STZ模型小鼠同时检测胰腺重量及血清胰岛素水平;胰腺组织进行免疫组化(IHC)染色,检测磷酸化STAT3(pSTAT3)的表达定位。
结果解读:高脂饮食饲喂小鼠注射IL-22后2小时,空腹血糖显著降低(n=10,P<0.05);STZ诱导的糖尿病小鼠注射IL-22后,血糖水平在多个时间点显著降低(n=10,P<0.01),但胰腺重量及血清胰岛素水平无显著变化;免疫组化显示pSTAT3仅在胰腺腺泡细胞中激活,胰岛细胞中无激活,说明IL-22不影响胰岛素分泌,直接调控糖代谢过程。
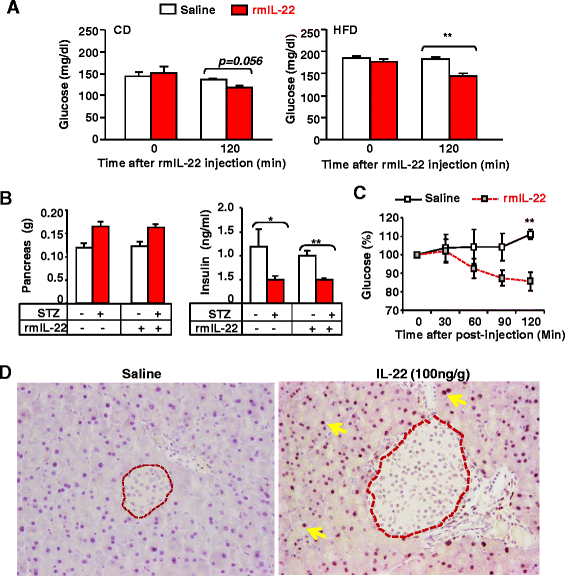
产品关联:实验所用关键产品:STZ(Sigma Aldrich)、免疫组化用pSTAT3抗体、血糖检测仪检测血糖水平。
3.5 IL-22抑制肝糖异生的体内外实验验证
实验目的:明确IL-22是否通过抑制肝糖异生降低血糖,以及对葡萄糖摄取的影响。
方法细节:体内实验:高脂饮食饲喂8周的小鼠,尾静脉注射IL-22腺病毒或对照腺病毒,5天后进行葡萄糖周转实验、丙酮酸耐量试验(PTT),采用实时荧光定量PCR(qRT-PCR)检测肝中糖异生基因的表达;同时进行2-脱氧葡萄糖摄取实验,检测肝、肌肉、白色脂肪组织(WAT)及棕色脂肪组织(BAT)的葡萄糖摄取情况。体外实验:分离原代小鼠肝细胞,用IL-22处理后,检测葡萄糖生成量及糖异生基因的表达。
结果解读:体内实验显示,IL-22处理后小鼠的葡萄糖周转速率显著降低(n=6-10,P<0.05),PTT中血糖升高被显著抑制(n=6-10,P<0.01),肝中G6Pase、PEPCK、TORC2等糖异生基因的表达显著下调(n=6-10,P<0.01);葡萄糖摄取实验显示IL-22处理对肝、肌肉、WAT的葡萄糖摄取无显著影响,BAT葡萄糖摄取有升高趋势但未达统计学显著性;体外实验中,IL-22处理的原代肝细胞葡萄糖生成量显著降低,糖异生基因表达下调,说明IL-22通过抑制肝糖异生降低血糖,不影响葡萄糖摄取。
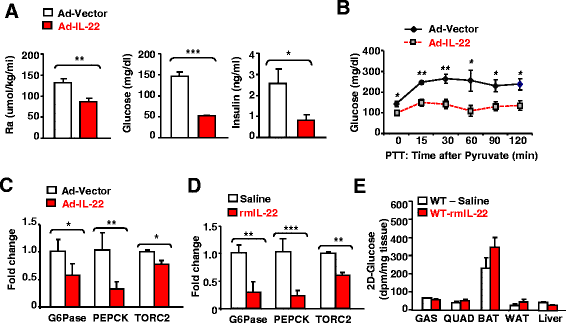
产品关联:实验所用关键产品:腺病毒表达载体、原代肝细胞分离试剂盒、qRT-PCR引物(序列见参考文献)。
3.6 IL-22调控肝糖异生的信号通路解析
实验目的:明确IL-22抑制肝糖异生的关键信号通路。
方法细节:原代小鼠肝细胞用IL-22处理后,采用Western blot检测STAT3、AKT、AMPK的磷酸化水平;分别使用STAT3敲除原代肝细胞、AMPK抑制剂Compound C、PI3K抑制剂LY294002处理肝细胞,再用IL-22处理后,检测葡萄糖生成量及糖异生基因的表达。
结果解读:IL-22处理主要诱导STAT3的磷酸化激活,轻度诱导AKT和AMPK的磷酸化;STAT3敲除后,IL-22对葡萄糖生成的抑制作用完全消失,对糖异生基因表达的抑制作用部分减弱;AMPK抑制剂处理后,IL-22对葡萄糖生成及G6Pase表达的抑制作用部分减弱;PI3K抑制剂处理对IL-22的作用无显著影响,说明IL-22通过STAT3和AMPK信号通路抑制肝糖异生,AKT通路不参与该过程。
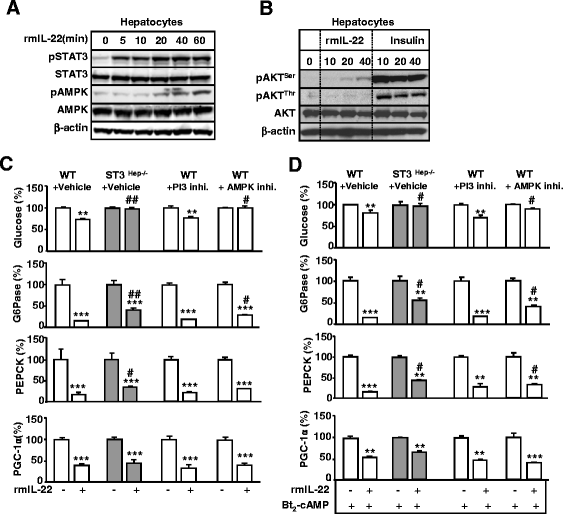
产品关联:实验所用关键产品:Compound C(EMD Chemicals)、LY294002(Sigma Aldrich)、Western blot用磷酸化抗体。
4. Biomarker研究及发现成果
本研究中IL-22作为代谢调控的功能性细胞因子,可被视为潜在的糖代谢调控Biomarker及治疗靶点,其筛选及验证逻辑为:动物模型验证IL-22对代谢的影响→体内外实验解析其调控肝糖异生的功能→信号通路验证明确分子机制。
Biomarker定位:IL-22属于循环细胞因子类Biomarker,其筛选基于现有研究中IL-22与代谢的关联,验证逻辑为通过基因敲除、转基因动物模型明确内源性及外源性IL-22对肥胖的影响,再通过体内外实验验证其对肝糖异生的调控作用,最后解析其分子通路。
研究过程详述:IL-22由免疫细胞分泌,循环来源为体内免疫细胞的活化;验证方法包括ELISA检测血清IL-22水平,体内实验通过葡萄糖周转实验、PTT验证其对肝糖异生的抑制作用,体外实验通过原代肝细胞葡萄糖生成实验验证功能;特异性方面,IL-22仅作用于表达IL-22R1的上皮细胞(如肝细胞),不作用于免疫细胞及胰岛β细胞;敏感性方面,单次高剂量IL-22即可显著降低高脂饮食及STZ诱导高血糖小鼠的血糖水平(n=10,P<0.05)。
核心成果提炼:本研究明确生理相关浓度的IL-22不影响肥胖及代谢综合征,但可通过激活STAT3和AMPK信号通路抑制肝糖异生,降低血糖水平,且该作用不依赖胰岛素分泌;创新性在于首次系统验证了生理相关浓度IL-22的代谢调控作用,澄清了领域内的争议,同时首次明确IL-22调控肝糖异生的双通路机制;该成果为高血糖的治疗提供了潜在靶点,尤其是对于胰岛素分泌不足的1型糖尿病患者,IL-22可能成为新的治疗策略。
