1. 领域背景与文献引入
文献英文标题:THOC5, a member of the mRNA export complex, contributes to processing of a subset of wingless/integrated (Wnt) target mRNAs and integrity of the gut epithelial barrier;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:RNA加工调控、肠道上皮稳态与Wnt信号通路
THO复合物是转录/输出(TREX)复合物的核心亚单位,最初在酿酒酵母中被发现,参与转录延伸、核RNA输出及基因组稳定性维持。在高等真核生物中,THO复合物包含THOC1至THOC7共7个成员,其中THOC5作为mRNA输出蛋白,仅调控约1%的基因表达,此前研究已证实其在造血干细胞维持及细胞因子介导的造血过程中不可或缺,但在造血系统外的细胞分化功能及相关病理变化中的作用尚未明确。领域共识:THOC5缺失仅影响特定亚群mRNA的加工,不干扰整体poly(A)+RNA的核输出,但对于其在胃肠道等再生器官中的功能,以及是否参与Wnt等关键信号通路下游mRNA的调控,仍存在显著研究空白。因此,本研究通过构建他莫昔芬诱导的THOC5全身敲除小鼠模型,系统探究THOC5在多器官中的功能及病理机制,填补该领域的研究缺口。
2. 文献综述解析
作者对领域内现有研究按“研究系统(酵母、细胞系、小鼠模型)”和“功能方向(造血调控、mRNA输出)”进行分类评述。现有研究关键结论显示,酵母中THO复合物核心功能为参与转录延伸与mRNA输出;高等真核生物细胞系研究表明,THOC5是酪氨酸激酶的底物,受细胞外信号调控,其缺失仅导致少量基因(约1%)表达下调,且这些基因多参与细胞分化过程;此前干扰素诱导的THOC5敲除小鼠模型证实,THOC5对造血细胞存活至关重要,但该模型可能受干扰素的协同作用影响,无法全面反映THOC5在多器官中的功能。现有技术方法的优势在于,细胞系研究可精准定位THOC5调控的mRNA亚群,干扰素诱导模型可研究造血系统的急性变化,但局限性也较为明显:干扰素诱导模型存在细胞因子干扰,未涉及胃肠道等再生器官的研究,且未明确THOC5与Wnt信号通路的关联。本研究的创新价值在于,首次构建他莫昔芬诱导的全身THOC5敲除小鼠,排除干扰素的干扰,系统揭示THOC5在造血系统、胃肠道、肝肾等多器官中的功能差异;首次证实THOC5对Wnt信号通路下游特定亚群mRNA的加工不可或缺,且其缺失会导致肠道上皮屏障破坏与败血症;明确THOC5在终末分化器官(肝、肾)中对整体mRNA输出无影响,揭示真核生物中存在多种mRNA输出通路。
3. 研究思路总结与详细解析
本研究的核心目标是探究THOC5在造血系统外的细胞分化功能及病理机制,核心科学问题为“THOC5是否调控Wnt信号通路下游mRNA加工并维持肠道上皮稳态”,技术路线遵循“模型构建→多器官病理检测→信号通路靶标验证→机制解析”的闭环逻辑。
3.1 他莫昔芬诱导THOC5敲除小鼠模型构建与验证
实验目的:构建可诱导的全身THOC5敲除小鼠模型,验证不同器官中THOC5的敲除效率与蛋白表达变化。
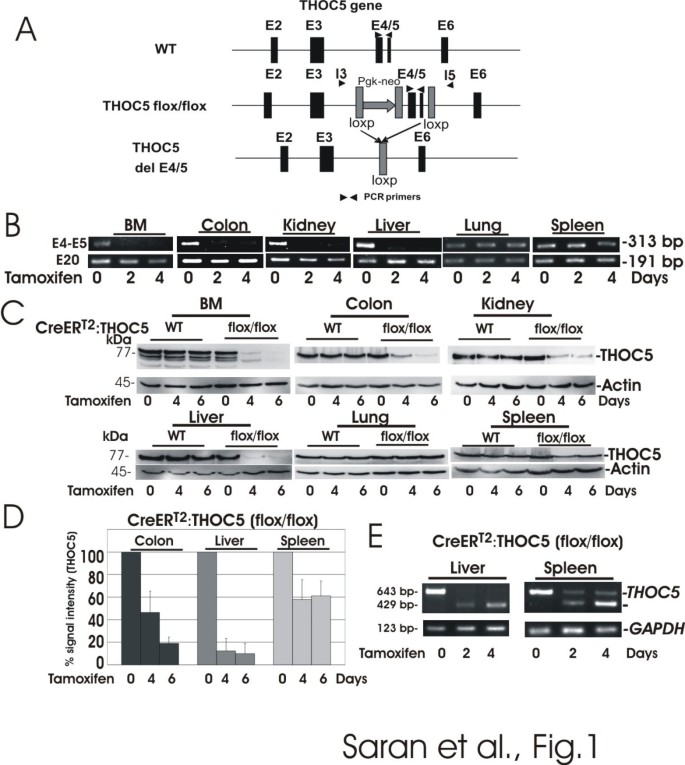
方法细节:将THOC5(flox/flox)小鼠与Rosa26-Cre ER^{T2}小鼠交配,获得他莫昔芬诱导型敲除小鼠;对5-9周龄小鼠腹腔注射他莫昔芬(1mg/20g体重),两次注射间隔2天;在注射后0、2、4、6天收集骨髓、结肠、肾、肝、肺、脾等器官样本,通过PCR检测基因组DNA中THOC5外显子4/5的缺失情况,免疫印迹检测THOC5蛋白表达水平,RT-PCR检测THOC5 mRNA的剪接形式。
结果解读:PCR结果显示,注射他莫昔芬2天后,骨髓、结肠、肾、肝中THOC5外显子4/5完全缺失,肺和脾中仅部分缺失;免疫印迹结果显示,敲除小鼠的骨髓、结肠、胃、空肠、肾、肝中THOC5蛋白水平在6天内降至不足20%,脾中仅降低40%;RT-PCR结果显示,肝中仅检测到缺失外显子4/5的THOC5 mRNA,脾中同时存在野生型和缺失型mRNA,表明THOC5在不同器官中的敲除效率存在差异。
产品关联:文献提及的关键产品包括:Sigma的他莫昔芬、Roche的High Pure RNA Isolation kit、Qiagen的Omniscript reverse transcriptase kit、Santa Cruz的GAPDH和肌动蛋白抗体、Cell Signaling的活化半胱天冬酶3、半胱天冬酶3和组蛋白H3抗体、自制的THOC5单克隆抗体等。
3.2 THOC5缺失对多器官病理变化的影响
实验目的:检测THOC5缺失后造血系统、肝、肾、胃肠道等器官的病理变化,明确THOC5的器官特异性功能。
方法细节:收集注射他莫昔芬后0-6天的小鼠器官样本,骨髓细胞经May-Grünwald和苏木精染色观察细胞形态;脾组织称重并计数细胞数量,免疫组化检测CD3、PAX5、Ki67阳性细胞;肝和肾组织进行免疫组化检测活化半胱天冬酶3,分离核和细胞质RNA检测白蛋白、转铁蛋白mRNA的输出情况;胃肠道组织经苏木精-伊红染色观察病理结构,免疫组化检测THOC5、Ki67、活化半胱天冬酶3的表达;心脏血液接种于血琼脂平板培养细菌,通过SOLiD 5500XL系统鉴定菌株类型。
结果解读:骨髓中核细胞数量在注射后2天开始下降,6天后几乎消失,表明THOC5缺失导致造血细胞凋亡;脾重量降至约一半,B细胞(PAX5阳性)和增殖细胞(Ki67阳性)数量显著减少,T细胞(CD3阳性)无明显变化;肝和肾中未观察到炎症或凋亡细胞,白蛋白和转铁蛋白mRNA的核输出未受影响,表明THOC5在终末分化器官中对整体mRNA输出无作用;胃肠道中,小肠长度缩短至一半,上皮绒毛紊乱缩短,隐窝(肠道干细胞区域)出现扩张和坏死,Ki67阳性增殖细胞显著减少,活化半胱天冬酶3阳性凋亡细胞在注射后3天出现在隐窝,5天遍布整个绒毛;血液培养显示,注射后4天开始出现细菌菌落,5-7天所有敲除小鼠血液中均有大量细菌,97%为γ-变形菌(包括大肠杆菌),表明肠道上皮屏障破坏导致细菌移位和败血症,最终导致小鼠死亡。
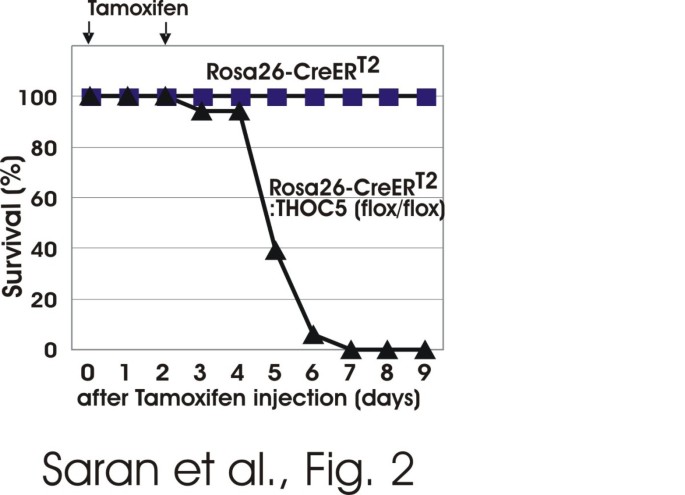
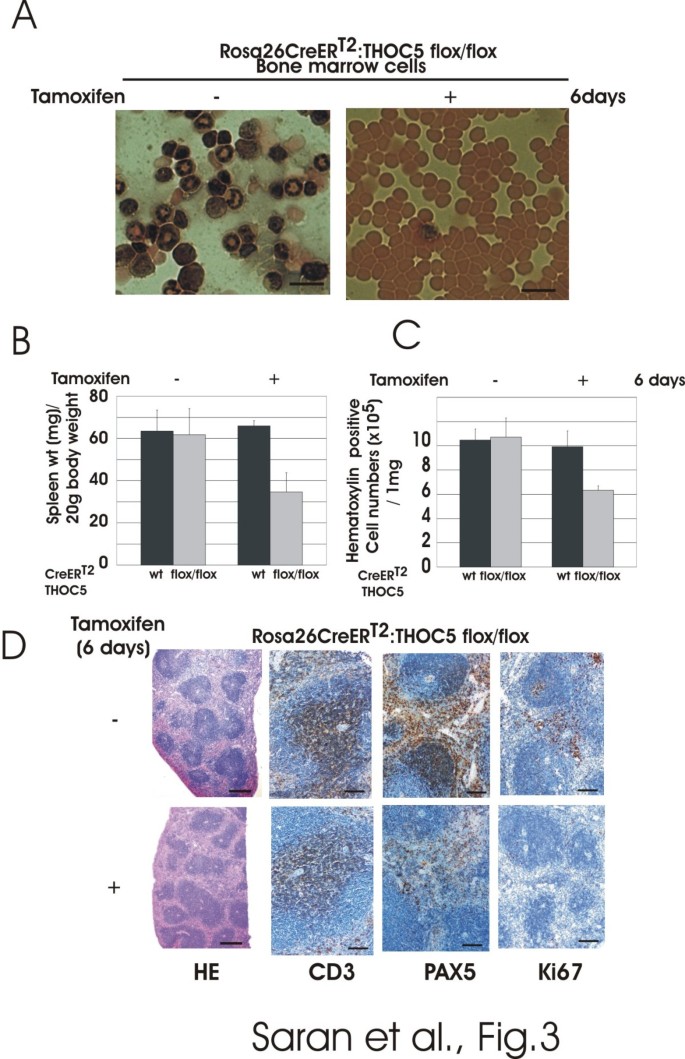
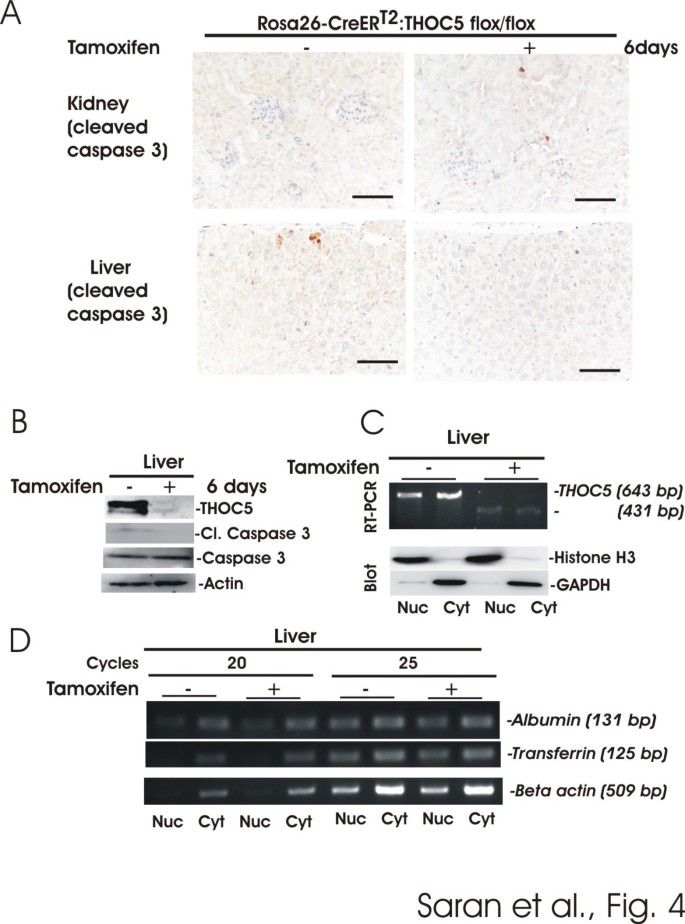
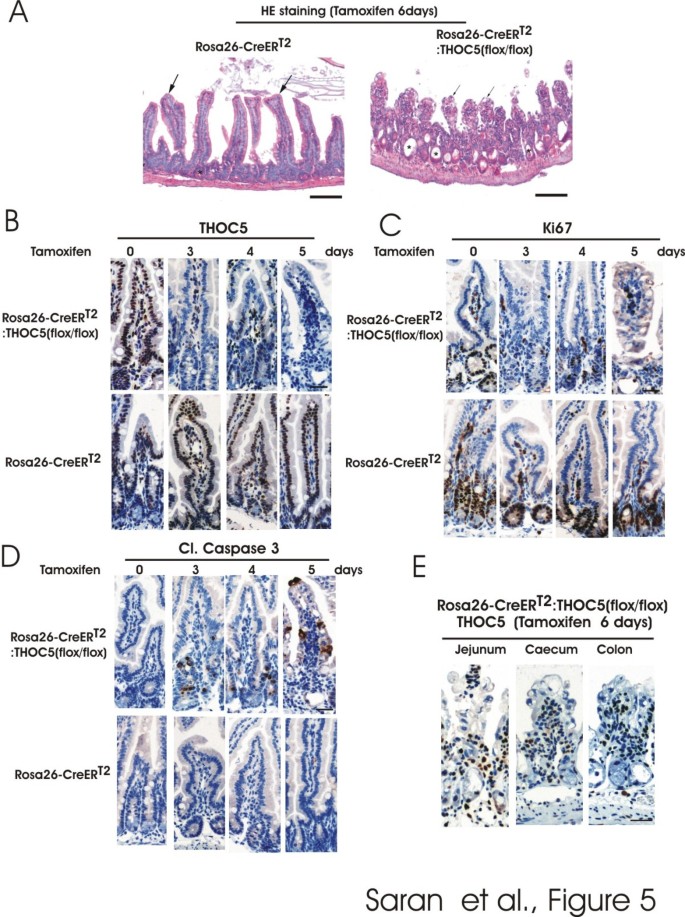
产品关联:文献提及的关键产品包括:Dakocytomation的Ki67和CD3抗体、BD Biosciences的PAX5抗体、Roche的抗地高辛-罗丹明抗体、Life technologies的SOLiD 5500XL测序系统等。
3.3 THOC5对Wnt信号通路下游mRNA加工的调控作用
实验目的:验证THOC5是否参与Wnt信号通路下游特定mRNA的加工,明确其调控的mRNA亚群及机制。
方法细节:对敲除小鼠小肠组织进行原位杂交,检测Sox9、Ascl2、Fn1等Wnt靶基因的mRNA表达;通过免疫沉淀分离THOC5-mRNA复合物,RT-PCR检测结合的Wnt靶基因mRNA;分离THOC5缺失的小鼠胚胎成纤维细胞(MEF)和骨髓来源巨噬细胞的核与细胞质RNA,检测Sox9、Ascl2 mRNA的输出情况;检测核内Sox9 mRNA的剪接与未剪接形式。
结果解读:原位杂交结果显示,THOC5缺失后,Sox9和Ascl2的mRNA表达显著降低,Fn1 mRNA表达无变化;免疫沉淀结果显示,Sox9、Ascl2、Snai1、Wnt11、Survivin等Wnt靶基因mRNA可与THOC5结合,而MMP2、Fn1则不能;核质分离RNA检测显示,THOC5缺失后,Sox9和Ascl2的剪接体mRNA输出显著减少,核内未剪接的Sox9 mRNA积累,表明THOC5不仅参与这些mRNA的核输出,还参与其剪接加工;此外,Toll样受体靶基因Ptgs2的mRNA也可与THOC5结合,表明THOC5也参与Toll样受体信号通路的mRNA加工。
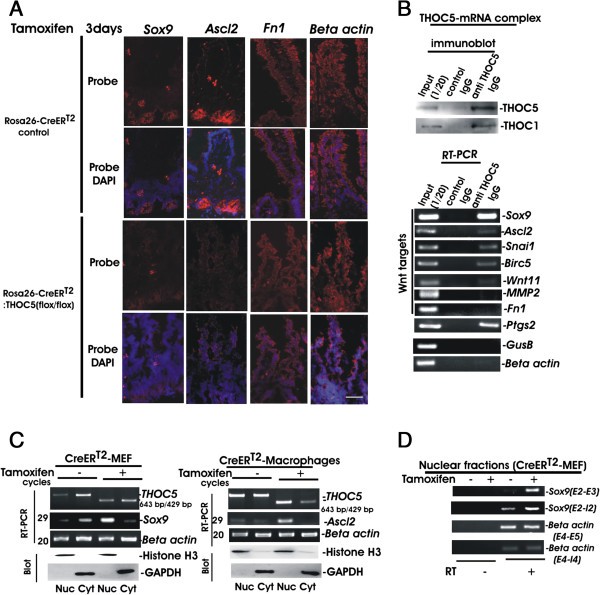
产品关联:文献未提及具体实验产品,领域常规使用RNA原位杂交试剂盒、免疫沉淀试剂盒、RT-PCR相关试剂等。
4. Biomarker研究及发现成果
Biomarker定位:本研究中,THOC5调控的Wnt信号通路下游特定亚群mRNA(Sox9、Ascl2等)可作为肠道上皮干细胞功能的潜在Biomarker,筛选与验证逻辑为:首先通过原位杂交筛选THOC5缺失后表达显著变化的Wnt靶基因,再通过免疫沉淀验证这些mRNA与THOC5的直接结合,最后通过核质分离实验验证其加工与输出依赖THOC5。研究过程详述:这些mRNA来源于肠道上皮干细胞及分化细胞,验证方法包括原位杂交检测组织中表达水平、免疫沉淀检测与THOC5的结合能力、核质分离RT-PCR检测mRNA的核输出与剪接情况;特异性方面,仅特定Wnt靶基因(Sox9、Ascl2等)依赖THOC5调控,而Fn1等Wnt靶基因不受影响;敏感性方面,THOC5缺失后,Sox9和Ascl2的mRNA在肠道隐窝中几乎完全消失,其核输出效率显著降低。核心成果提炼:首次发现THOC5是Wnt信号通路下游特定亚群mRNA加工的关键调控因子,这些mRNA的正常表达是维持肠道上皮干细胞功能与上皮屏障完整性的必要条件;THOC5本身可作为维持肠道上皮稳态和造血系统功能的关键调控因子,其缺失导致的肠道细菌移位与败血症是小鼠死亡的核心原因;本研究未提供ROC曲线、风险比(HR)等统计学数据,但明确了THOC5调控的mRNA亚群及其在肠道上皮稳态中的核心作用,为肠道疾病的治疗靶点筛选提供了新方向。
