1. 领域背景与文献引入
文献英文标题:Isolation, culture, and characterization of chicken intestinal epithelial cells;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:家禽肠道生物学与细胞体外模型
家禽肠道上皮细胞是营养吸收与病原体防御的核心载体,在家禽营养研发、肠道病理机制研究中,可靠的体外细胞模型是关键工具。领域共识:传统研究多采用哺乳动物永生化细胞系(如人肠上皮细胞系Caco-2),这类模型成本低、易培养,但无法精准模拟鸡肠道的物种特异性生理特征,也难以用于鸡源病原体(如球虫、产气荚膜梭菌)的互作研究。当前领域的核心问题是,已有的鸡原代肠上皮细胞培养方法普遍存在细胞存活时间短(仅7-10天)、无法形成功能完整的上皮单层、缺乏关键屏障功能验证(如跨上皮电阻检测)、污染控制不足等缺陷,限制了其在实际研究中的应用。针对这一空白,本研究旨在开发一套可长期维持鸡原代肠上皮细胞(cIECs)存活与功能的培养体系,为家禽肠道研究提供更贴近体内生理状态的体外模型。
2. 文献综述解析
本文综述部分以时间线与技术局限性为核心分类维度,系统梳理了鸡原代肠上皮细胞培养领域的研究进展。现有研究中,2004年Immerseel等首次建立鸡结肠上皮细胞原代培养模型,可用于沙门氏菌互作研究,但细胞仅能存活3天;同年Dimier-Poisson等分离的鸡肠上皮细胞可被球虫感染,但未报道细胞存活时间;2015年Yuan等优化了酶解条件,使细胞存活时间延长至9天,但缺乏完整的上皮细胞特性鉴定;2017年Kaiser与2019年Bai的模型虽能维持细胞形态,但存活时间仍仅为7-10天;2018年Bar Shira的模型验证了细胞的免疫应答功能,但未开展跨上皮电阻等屏障功能检测;Rath等建立的鸡肠上皮细胞系则存在上皮形态缺失的问题,紧密连接蛋白定位异常。这些研究的优势在于逐步探索了鸡肠上皮细胞的分离与培养条件,为后续研究奠定了基础,但普遍存在存活时间短、功能验证不完整、污染控制能力弱等局限性。
与现有研究相比,本研究的核心创新点在于首次实现鸡原代肠上皮细胞在Transwell支架上的培养,并完成跨上皮电阻(TEER)检测,证明细胞可形成功能完整的上皮屏障;通过优化酶解组合、培养基配方与污染控制策略,将细胞存活时间延长至12天,远超此前模型的存活时长;同时完成了细胞的分子标记、增殖通路激活与屏障功能的系统性鉴定,填补了领域内长期稳定鸡肠上皮细胞模型的空白。
3. 研究思路总结与详细解析
本研究的核心目标是建立可长期存活、功能完整的鸡原代肠上皮细胞体外培养模型,核心科学问题为如何优化分离与培养条件,以维持细胞的上皮特性与屏障功能并延长存活时间,技术路线遵循“细胞分离→污染控制→活力与特性鉴定→功能验证”的闭环逻辑,通过分阶段优化培养条件,实现细胞的长期稳定培养与功能验证。
3.1 鸡胚肠上皮细胞分离与初始培养
本环节的实验目的是从鸡胚十二指肠组织中分离获得高活性的肠上皮细胞聚集体。方法细节为取19日龄SPF鸡胚十二指肠,去除脂肪与黏液后剪碎,采用胶原酶与透明质酸酶混合液37℃消化30分钟,通过100μm与40μm滤网反向过滤获得>40μm的细胞聚集体,接种于0.8mg/mL Matrigel包被的培养板,初始培养基添加丁酸钠以促进肠干细胞向吸收型上皮细胞分化。结果解读:细胞聚集体在24小时内贴壁并从增殖灶迁移扩散(图1),5天达到汇合状态,7天呈现典型的上皮细胞鹅卵石形态,12天内保持良好的细胞形态与活力。
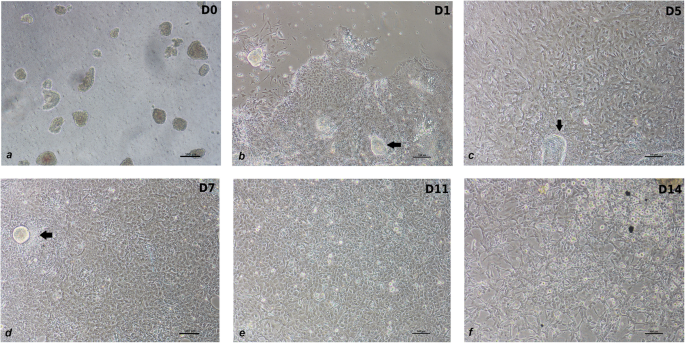
实验所用关键产品:Matrigel基质(Corning, Cat.#356234)、PrestoBlue®细胞活力试剂(Thermo Fisher Scientific, Cat.#A13262)、胶原酶-透明质酸酶混合消化液。
3.2 污染细胞去除策略验证
本环节的实验目的是有效排除内皮细胞、成纤维细胞等污染细胞,纯化肠上皮细胞群体。方法细节为通过反向过滤收集<40μm的污染细胞作为阳性对照,将分离的cIECs分别培养于含10%胎牛血清(FBS)的培养基与含0.1mg/mL肝素+2%FBS的培养基,通过免疫荧光检测波形蛋白(VIM)标记污染细胞。结果解读:含肝素与低FBS的培养基可显著抑制污染细胞的贴壁与增殖(图3),cIECs在培养7天与11天的免疫荧光检测中均为波形蛋白阴性(图9),证明细胞群体无杂细胞污染;阳性对照的污染细胞波形蛋白表达阳性(图2),验证了检测方法的可靠性。
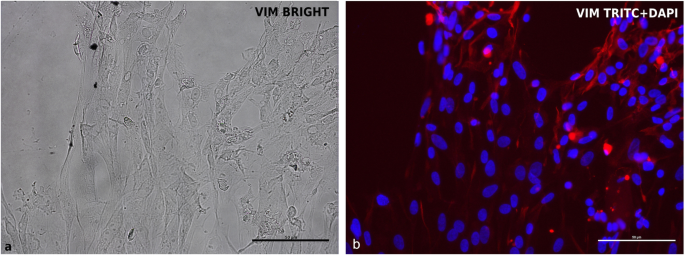
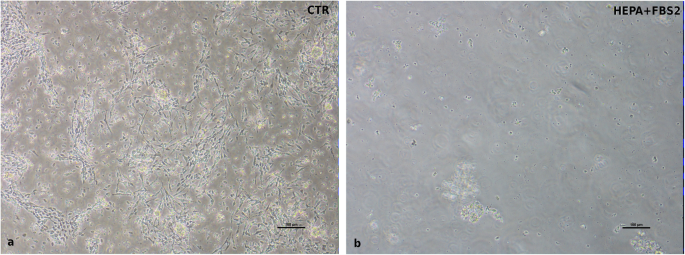
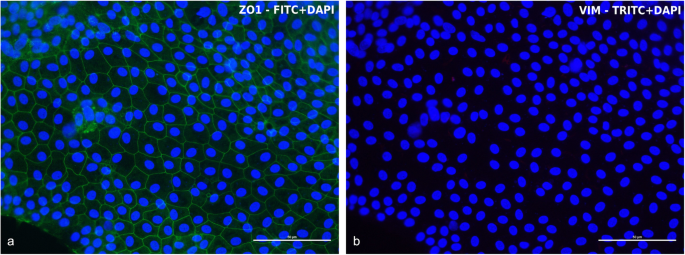
实验所用关键产品:肝素钠、抗波形蛋白单克隆抗体(详见原文Table4)。
3.3 细胞活力与增殖能力检测
本环节的实验目的是评估cIECs的长期存活能力与增殖活性。方法细节为采用PrestoBlue®试剂在培养1、2、4、7、9、11、12、14天检测细胞活力,通过EdU掺入实验标记S期增殖细胞,对比对照组与生长因子处理组的增殖差异。结果解读:cIECs在12天内活力保持稳定,荧光值无显著差异(n=8,P>0.05),14天活力显著下降(图4);添加生长因子组的EdU阳性细胞比例显著高于对照组(n=4,P<0.05),证明生长因子可有效维持细胞的增殖活性(图8)。
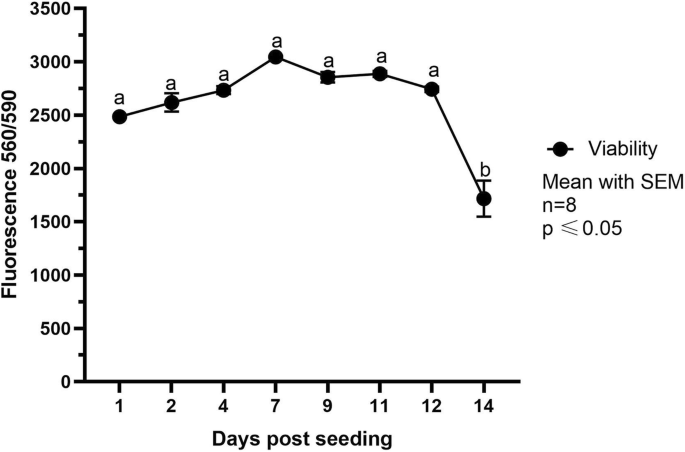
实验所用关键产品:PrestoBlue®细胞活力试剂(Thermo Fisher Scientific, Cat.#A13262)、EdU-Click 488试剂盒(Sigma-Aldrich, Cat.#BCK-EDU488)。
3.4 上皮细胞分子标记鉴定
本环节的实验目的是验证cIECs的上皮细胞特性与干细胞群体存在。方法细节为通过实时荧光定量PCR(RT-PCR)检测上皮标记物(E-钙粘蛋白、紧密连接蛋白1、闭合蛋白、细胞角蛋白18/20、绒毛蛋白)与干细胞标记物(LGR5、SOX9)的转录水平,通过免疫荧光检测蛋白表达与定位。结果解读:RT-PCR显示cIECs在培养48小时与7天均稳定表达上皮与干细胞标记物,两个时间点的转录水平无显著差异(n=4,P>0.05,图5);免疫荧光检测显示92%的细胞表达细胞角蛋白18,97%表达绒毛蛋白,100%表达紧密连接蛋白1与闭合蛋白(图7),证明细胞始终维持上皮细胞特性,且无杂细胞污染。
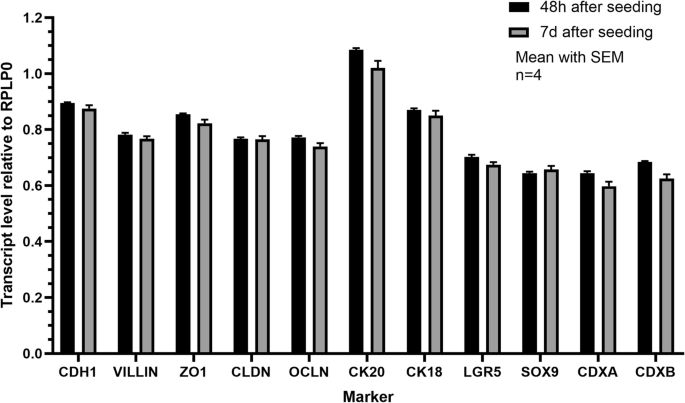
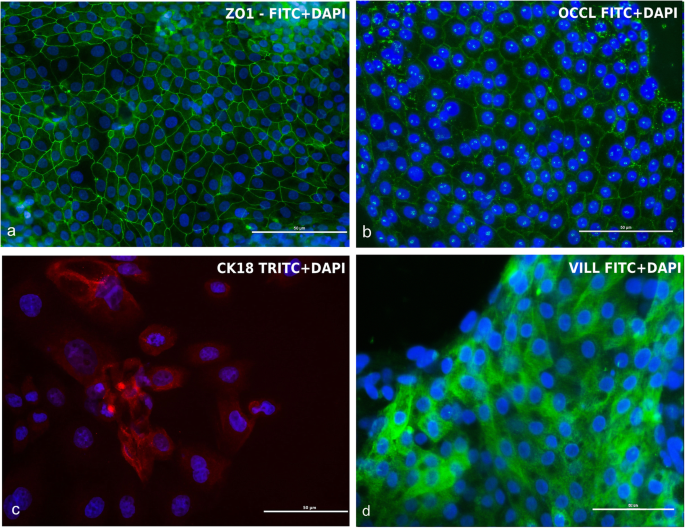
实验所用关键产品:上皮标记物单克隆抗体(详见原文Table4)、RT-PCR引物(Sigma-Aldrich)。
3.5 Wnt/EGF增殖通路激活验证
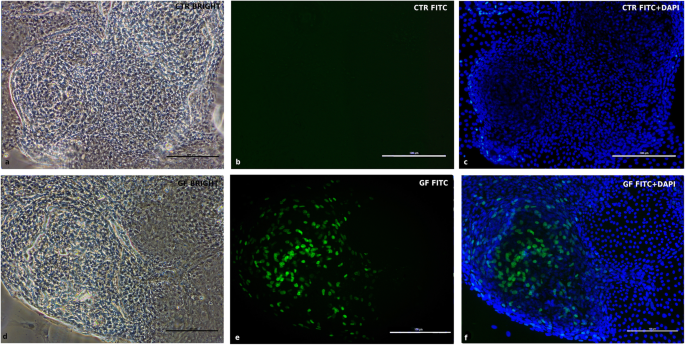
本环节的实验目的是验证生长因子对cIECs增殖通路的调控作用。方法细节为将cIECs分为对照组与生长因子处理组(添加R-spondin1、Noggin、CHIR99021、人表皮生长因子hEGF),培养5天后通过RT-PCR检测Wnt与EGF通路下游基因的表达,通过免疫荧光验证蛋白表达。结果解读:生长因子处理组的LEF1、c-Myc、MAPK1、EGFR基因表达显著上调(n=3,P<0.05),AXIN2基因表达下调(图6),证明Wnt与EGF通路被有效激活;免疫荧光显示c-Myc与MAPK1蛋白在生长因子处理组的表达显著高于对照组(图10、11),进一步验证通路激活效果。
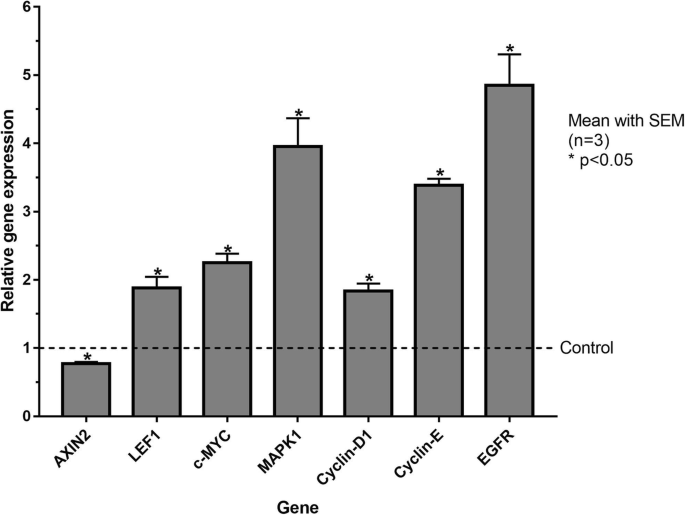
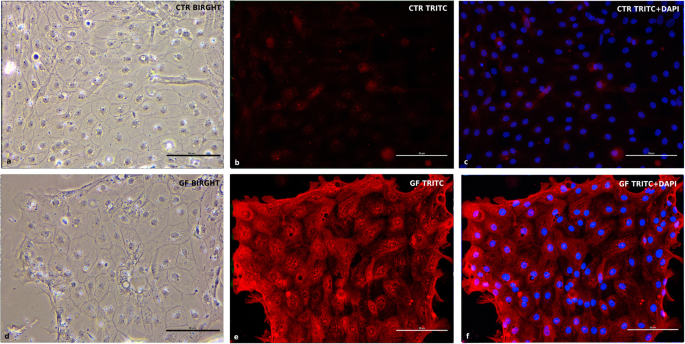
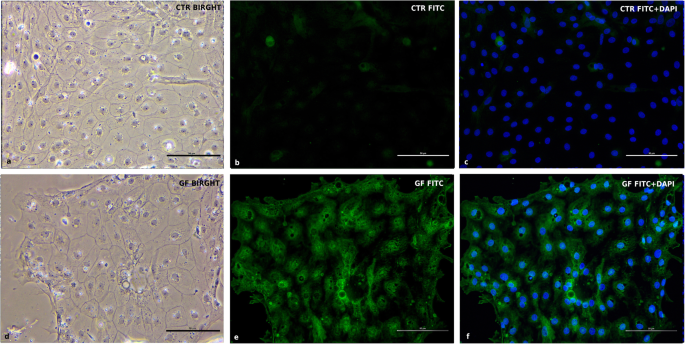
实验所用关键产品:R-spondin1、Noggin、CHIR99021、hEGF等生长因子,通路标记物单克隆抗体(详见原文Table4)。
3.6 细胞极化与屏障功能鉴定
本环节的实验目的是验证cIECs形成功能完整上皮屏障的能力。方法细节为将cIECs接种于2.5mg/mL Matrigel包被的Transwell支架,培养14天,每日检测跨上皮电阻(TEER)值以评估屏障功能。结果解读:TEER值从培养第2天的10Ω·cm²逐渐升高至第7天的64Ω·cm²,并维持稳定至第12天(n=4,P<0.05,图12),证明细胞可形成极化的上皮单层,具备完整的屏障功能,这一结果为模型用于肠道营养吸收、病原体侵袭等研究提供了功能学依据。
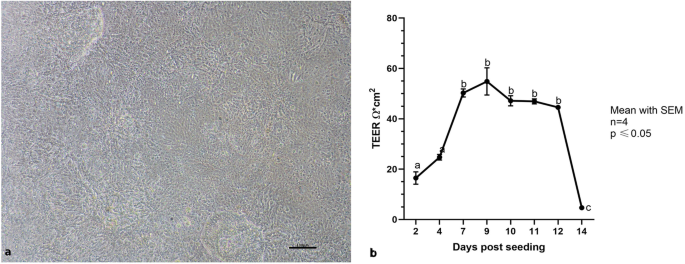
实验所用关键产品:Transwell支架(Corning, Cat.#3495)、Millicell ERS-2跨上皮电阻检测仪(Millipore, Cat.#MERS00002)。
4. Biomarker研究及发现成果
Biomarker定位与筛选逻辑
本研究涉及的Biomarker分为三类:上皮细胞特异性标记物(细胞角蛋白18、紧密连接蛋白1、闭合蛋白、绒毛蛋白、E-钙粘蛋白)、肠干细胞标记物(LGR5、SOX9)、增殖通路激活标记物(LEF1、c-Myc、MAPK1)。筛选与验证逻辑为:先通过RT-PCR检测转录水平初步筛选,再通过免疫荧光验证蛋白表达与定位,最后结合功能实验(TEER)验证标记物与细胞功能的相关性,形成“转录-蛋白-功能”的完整验证链条。
研究过程与数据解析
Biomarker的来源为19日龄鸡胚十二指肠分离的原代肠上皮细胞,验证方法包括RT-PCR定量检测转录水平、免疫荧光定性检测蛋白表达与定位、TEER检测屏障功能。特异性方面,免疫荧光显示上皮标记物的阳性率为92%-100%,波形蛋白(杂细胞标记)阳性率为0,证明标记物的特异性;敏感性方面,RT-PCR可稳定检测到标记物的转录表达,且培养48小时与7天的表达水平无显著差异,证明标记物的稳定性。屏障功能验证中,TEER值达到64Ω·cm²,与其他小肠上皮细胞系的TEER范围(50-100Ω·cm²)一致,证明细胞屏障功能的完整性。
核心成果提炼
本研究的核心Biomarker成果包括:首次鉴定鸡原代肠上皮细胞长期培养中的稳定标记物谱,证明细胞可同时维持分化上皮细胞与干细胞群体的存在;通过Wnt/EGF通路标记物的表达变化,明确生长因子维持细胞增殖的分子机制;首次通过TEER检测证明鸡原代肠上皮细胞可形成功能完整的上皮屏障,TEER值稳定维持至培养第12天(n=4,P<0.05)。这些成果为鸡肠上皮细胞模型的标准化鉴定提供了参考标记,同时证明本研究建立的模型具备长期存活与功能完整的特性,可用于家禽肠道营养、病理与药物筛选等领域的研究。
