1. 领域背景与文献引入
文献英文标题:Hypoxia and TGF-β1 lead to endostatin resistance by cooperatively increasing cancer stem cells in A549 transplantation tumors;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:肺癌抗血管生成治疗耐药机制。
肺癌是全球癌症相关死亡的首要原因,占所有癌症死亡的30%,尽管抗血管生成治疗等手段取得了阶段性进展,但多数患者最终会出现耐药导致治疗失败。内皮抑素是中国临床广泛使用的内源性广谱抗血管生成药物,可通过抑制血管内皮生长因子与内皮细胞结合、诱导内皮细胞凋亡等多种途径发挥抗肿瘤作用,但已有研究发现其耐药现象,且仅明确髓源性抑制细胞参与部分耐药机制,肿瘤微环境中其他细胞及因子的作用尚未完全阐明。领域共识:癌症干细胞是肿瘤耐药、复发的关键细胞亚群,缺氧和转化生长因子-β1(TGF-β1)是肿瘤微环境的核心特征性因子,三者单独参与多种抗肿瘤药物耐药的研究已见报道,但三者协同作用在内皮抑素耐药中的机制尚未明确,这一空白为本文研究提供了必要性,旨在揭示内皮抑素耐药中癌症干细胞增加的驱动机制,为逆转耐药提供新的靶点和理论依据。
2. 文献综述解析
作者按耐药相关的细胞类群与细胞因子两大维度对现有研究进行分类评述,明确现有研究已证实癌症干细胞、TGF-β1、缺氧各自参与多种抗肿瘤药物耐药,但三者协同作用在内皮抑素耐药中的研究存在空白,本文首次探讨缺氧与TGF-β1协同调控癌症干细胞导致内皮抑素耐药的机制。
现有研究显示,抗血管生成治疗耐药的机制涉及肿瘤微环境中的多种细胞与因子,细胞类群方面,癌症干细胞通过处于细胞周期G0期、高表达耐药相关蛋白等机制逃避抗肿瘤药物杀伤,调节性T细胞、肿瘤相关成纤维细胞等也可通过免疫抑制、重塑肿瘤基质等促进耐药;细胞因子方面,TGF-β1在肿瘤进展阶段可通过诱导上皮间质转化、免疫抑制等促进耐药,缺氧可通过激活缺氧诱导因子-1α(HIF-1α)维持癌症干细胞特性,进而导致耐药。这些研究的优势在于分别明确了单一细胞或因子的耐药作用,局限性在于多单独探讨各因素的作用,缺乏对多因素协同作用的研究,尤其是在内皮抑素这一特定抗血管生成药物耐药中的协同机制尚未被揭示。
通过对比现有研究的空白,本研究的创新点在于首次发现内皮抑素治疗后,肿瘤微环境中缺氧加剧与TGF-β1水平升高可协同增加癌症干细胞比例,进而导致耐药,这一发现填补了内皮抑素耐药机制中多因素协同作用的研究空白,为后续逆转耐药的策略开发提供了新的方向。
3. 研究思路总结与详细解析
本研究的研究目标是明确内皮抑素耐药中癌症干细胞增加的驱动机制,核心科学问题为缺氧与TGF-β1是否通过协同作用增加A549移植瘤中的癌症干细胞导致耐药,技术路线遵循“动物实验验证耐药现象与细胞因子变化→体外实验验证协同作用→信号通路机制探索”的闭环逻辑。
3.1 动物移植瘤模型构建与内皮抑素耐药验证
实验目的:构建A549肺癌细胞NOD/SCID小鼠移植瘤模型,验证内皮抑素长期处理后的耐药现象。
方法细节:将5×10^6个A549细胞接种于NOD/SCID小鼠右侧腋窝皮下,待肿瘤体积达500-650mm³时,将小鼠随机分为内皮抑素组(12.5mg/kg尾静脉注射,n=7)与生理盐水组(n=7),连续给药12天,定期检测肿瘤体积。
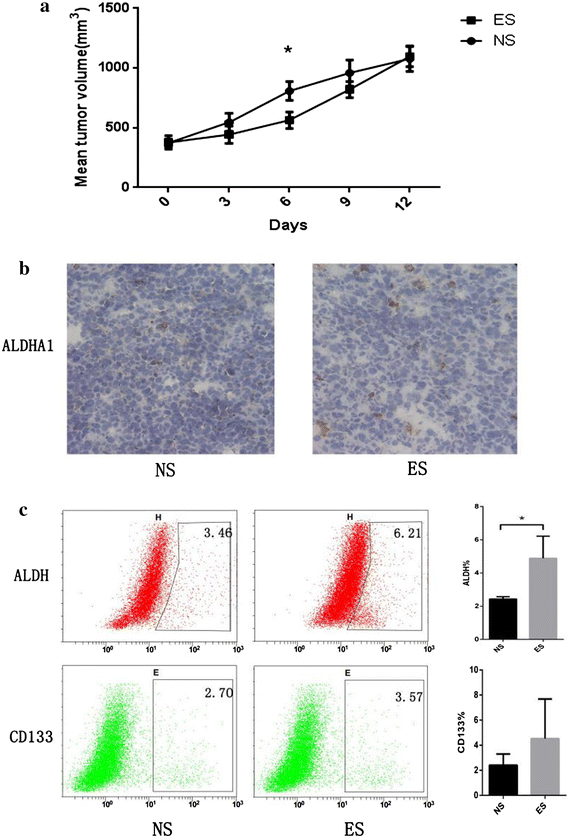
结果解读:给药12天后,内皮抑素组与生理盐水组的肿瘤体积无显著差异,提示小鼠移植瘤对内皮抑素产生耐药。
产品关联:文献未提及具体实验产品,领域常规使用细胞系培养试剂、动物实验给药装置、肿瘤体积测量工具等。
3.2 癌症干细胞比例检测
实验目的:检测内皮抑素处理后A549移植瘤中癌症干细胞的比例变化。
方法细节:采用流式细胞术检测肿瘤细胞中乙醛脱氢酶(ALDH)阳性细胞比例,采用免疫组化检测肿瘤组织中ALDH家族成员A1(ALDHA1)及CD133的表达水平,统计阳性细胞比例并进行统计学分析。
结果解读:流式细胞术结果显示,内皮抑素组ALDH阳性细胞比例显著高于生理盐水组(P=0.0292,n=7);免疫组化结果显示,内皮抑素组ALDHA1阳性细胞比例升高,CD133阳性细胞比例虽有升高但无统计学意义,提示内皮抑素处理后移植瘤中肺癌干细胞比例增加。
产品关联:实验所用关键产品:流式细胞仪(BD Biosciences FACS Aria SORP)、ALDH检测试剂盒(StemCell Technologies Aldefluor kit)、ALDHA1抗体(Abcam)、CD133抗体(Miltenyi Biotec PE-CD133/AC133)。
3.3 肿瘤微环境因子检测
实验目的:检测内皮抑素处理后A549移植瘤中血管密度、缺氧状态及细胞因子的变化。
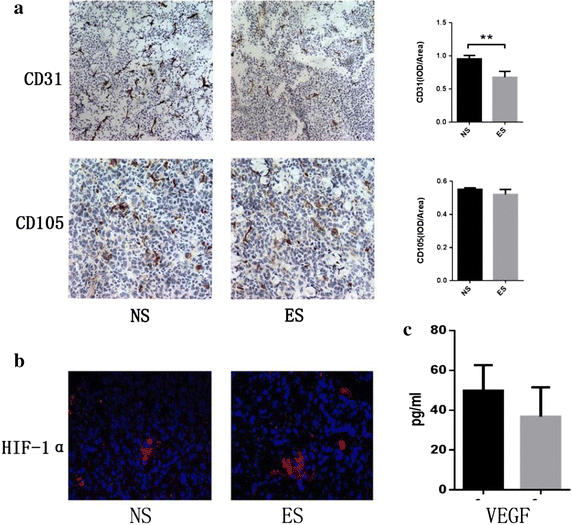
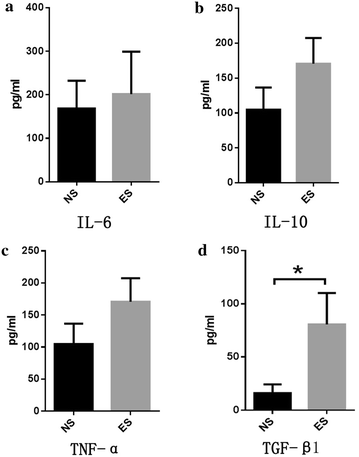
方法细节:采用免疫组化检测肿瘤组织中CD31、CD105的表达以评估微血管密度,采用免疫荧光检测HIF-1α的表达以反映缺氧状态,采用酶联免疫吸附试验(ELISA)检测肿瘤组织中TGF-β1、肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)、白细胞介素-10(IL-10)的水平。
结果解读:免疫组化结果显示,内皮抑素组CD31阳性细胞比例显著低于生理盐水组(P<0.001,n=7),CD105阳性细胞比例虽有降低但无统计学意义,提示微血管密度降低;免疫荧光结果显示,内皮抑素组HIF-1α表达水平升高,提示肿瘤缺氧加剧;ELISA结果显示,内皮抑素组TGF-β1水平显著升高(P=0.0217,n=7),TNF-α、IL-6、IL-10水平虽有升高但无统计学意义。
产品关联:实验所用关键产品:CD31抗体(Biolegend)、HIF-1α免疫荧光检测试剂、ELISA试剂盒(eBioscience或R&D Systems)。
3.4 体外缺氧与TGF-β1协同作用验证
实验目的:验证缺氧与TGF-β1是否协同增加A549细胞中的癌症干细胞比例。
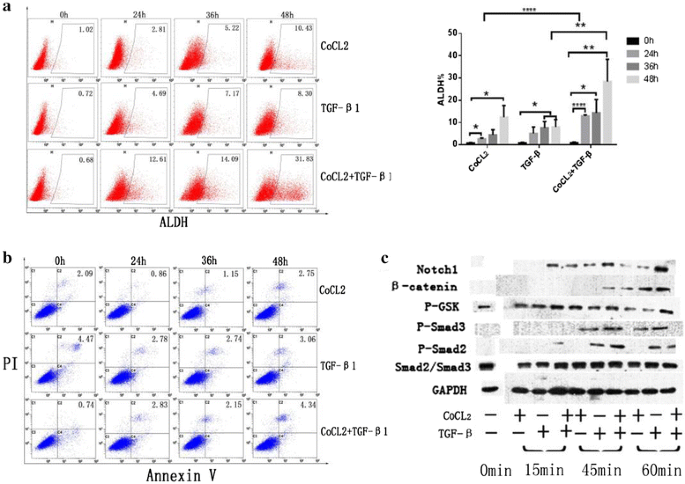
方法细节:采用氯化钴(CoCl₂,100μmol/L)模拟缺氧环境,采用重组人TGF-β1(10ng/mL)处理A549细胞,设置对照组、缺氧组、TGF-β1组、缺氧+TGF-β1组,处理24-48小时后,采用流式细胞术检测ALDH阳性细胞比例,采用流式细胞术检测细胞凋亡情况。
结果解读:流式细胞术结果显示,缺氧组、TGF-β1组的ALDH阳性细胞比例均高于对照组,且缺氧组的诱导作用强于TGF-β1组,缺氧+TGF-β1组的ALDH阳性细胞比例显著高于单独处理组(P<0.01,n=3);细胞凋亡检测结果显示,各处理组与对照组的细胞凋亡率无显著差异,提示处理未导致细胞凋亡,ALDH阳性细胞比例升高是干细胞特性增强的结果。
产品关联:实验所用关键产品:重组人TGF-β1(Biolegend)、氯化钴(分析纯试剂)、流式细胞仪(BD Biosciences FACS Aria SORP)。
3.5 信号通路机制探索
实验目的:探讨缺氧与TGF-β1协同增加癌症干细胞的下游信号通路。
方法细节:采用蛋白质免疫印迹法检测各处理组中Notch1、β-连环蛋白(β-catenin)、磷酸化Smad2(P-Smad2)、磷酸化Smad3(P-Smad3)的蛋白表达水平,以甘油醛-3-磷酸脱氢酶(GAPDH)为内参。
结果解读:蛋白质免疫印迹法结果显示,缺氧组、TGF-β1组、缺氧+TGF-β1组的Notch1、β-catenin、P-Smad2、P-Smad3蛋白表达水平均高于对照组,且缺氧+TGF-β1组的表达水平显著高于单独处理组,提示缺氧与TGF-β1可通过激活Notch、Wnt/β-catenin及Smad信号通路协同增强A549细胞的干细胞特性。

产品关联:文献未提及具体抗体产品,领域常规使用Notch1、β-catenin、P-Smad2、P-Smad3等信号通路相关抗体、蛋白质免疫印迹检测试剂。
4. Biomarker研究及发现成果
本研究涉及的Biomarker包括肺癌干细胞标记物(ALDH、CD133、ALDHA1)、肿瘤微环境因子(TGF-β1、HIF-1α),筛选与验证逻辑为“动物实验检测内皮抑素处理后Biomarker变化→体外实验验证Biomarker的调控作用→信号通路机制探索”,形成完整的逻辑链条。
Biomarker来源为A549小鼠移植瘤组织及体外培养的A549细胞,验证方法包括流式细胞术(ALDH、CD133)、免疫组化(ALDHA1、CD31、CD105)、免疫荧光(HIF-1α)、ELISA(TGF-β1等细胞因子)、蛋白质免疫印迹法(信号通路蛋白)。特异性与敏感性数据方面,动物实验中,内皮抑素组ALDH阳性细胞比例较对照组显著升高(P=0.0292,n=7),TGF-β1水平显著升高(P=0.0217,n=7);体外实验中,缺氧+TGF-β1组ALDH阳性细胞比例较对照组升高约2倍(文献未明确提供具体数值,基于图表趋势推测),且差异具有统计学意义(P<0.01,n=3)。
本研究的核心成果为首次证实内皮抑素治疗后,肿瘤微环境中缺氧加剧与TGF-β1水平升高可协同增加肺癌干细胞比例,进而导致耐药,其中Notch、Wnt/β-catenin及Smad信号通路参与这一调控过程。该Biomarker的功能关联在于,ALDH、CD133阳性肺癌干细胞比例升高可作为内皮抑素耐药的潜在标志物,TGF-β1与HIF-1α可作为逆转耐药的潜在干预靶点;创新性在于首次揭示了缺氧与TGF-β1协同调控肺癌干细胞导致内皮抑素耐药的机制,为肺癌抗血管生成治疗耐药的研究提供了新的视角。
