1. 领域背景与文献引入
文献英文标题:H-RN, a peptide derived from hepatocyte growth factor, inhibits corneal neovascularization by inducing endothelial apoptosis and arresting the cell cycle;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:眼科学-角膜新生血管与抗血管生成治疗
正常角膜的透明性依赖于其无血管状态,但创伤、炎症、感染等多种病理过程可诱发角膜新生血管,该过程虽能在一定程度上促进伤口愈合,却会通过侵入角膜基质、引发出血、瘢痕形成等途径严重损害角膜透明度,导致视力下降,甚至破坏角膜免疫赦免状态、降低角膜移植成功率。领域共识:角膜新生血管是全球第二大致盲原因,也是发达国家最常见的角膜盲类型。当前临床治疗方案包括直接抗血管生成药物(如贝伐单抗、雷珠单抗)、间接抗炎药物(如糖皮质激素)、激光光凝、光动力疗法等,但存在诸多局限性:直接抗血管生成药物年治疗成本极高且可能引发全身不良反应;糖皮质激素长期使用会增加感染、白内障、青光眼的风险;物理治疗需多次操作,易引发角膜损伤等并发症。在生物药物研发领域,肽类药物相比蛋白类药物具有更低的免疫原性、更高的水溶性和更稳定的生产工艺,已成为抗血管生成药物的重要研究方向,但针对角膜新生血管的低毒高效肽类药物仍较为缺乏。此前研究已发现来源于肝细胞生长因子Kringle 1结构域的H-RN肽对视网膜新生血管有抑制作用,本文进一步将其拓展至角膜新生血管领域,通过体内外实验系统验证其抗血管生成作用,并明确其分子机制,为角膜新生血管的治疗提供新的候选药物。
2. 文献综述解析
本文综述围绕角膜新生血管的临床危害、现有治疗方案的局限性及抗血管生成肽类药物的研发现状展开,作者按“临床治疗手段-生物药物研发”的维度对现有研究进行分类梳理。现有研究表明,角膜新生血管可显著降低患者视力,甚至导致失明,临床常用的直接抗血管生成药物虽能有效抑制血管生成,但高昂的成本限制了其广泛应用,且存在潜在的全身不良反应;激光光凝、光动力疗法等物理治疗手段需精准控制能量参数,否则易引发角膜穿孔、瘢痕加重等严重并发症;抗炎药物虽能间接抑制血管生成,但长期使用的安全性问题不容忽视。在生物药物研发领域,肽类药物因低免疫原性、高水溶性、易规模化生产等优势,已成为抗血管生成药物的重要发展方向,但针对角膜新生血管的肽类药物研究仍处于起步阶段,且缺乏对作用机制的深入阐明。本文的创新价值在于,首次将已在视网膜新生血管模型中验证活性的H-RN肽拓展至角膜新生血管领域,通过体内外实验系统验证其抗血管生成作用,并明确其通过诱导内皮细胞凋亡和细胞周期阻滞的双重机制,弥补了现有研究中针对角膜新生血管的低毒高效肽类药物的空白,为角膜新生血管的治疗提供了新的思路。
3. 研究思路总结与详细解析
本文整体研究思路为“体外细胞功能验证→体内动物模型验证→作用机制探究”的闭环,核心目标是明确H-RN对VEGF诱导的角膜新生血管的抑制作用及分子机制,核心科学问题是H-RN如何调控内皮细胞的生物学行为以发挥抗血管生成作用。
3.1 体外内皮细胞增殖抑制实验
实验目的:验证H-RN对VEGF诱导的人脐静脉内皮细胞(HUVEC)增殖的抑制作用。
方法细节:将HUVEC接种于96孔板(4.8×10³细胞/孔),培养24h后血清饥饿过夜,随后分别用VEGF(100ng/ml)单独处理、VEGF联合不同浓度H-RN(0、1μM、10μM、100μM、1mM)或乱序肽处理24h,采用MTS法检测细胞增殖活性,每组实验重复3次。
结果解读:如图1所示,与对照组相比,VEGF单独处理可显著促进HUVEC增殖(p<0.05);随着H-RN浓度升高,细胞增殖抑制作用逐渐增强,1mM H-RN时达到最大抑制效果(p<0.05),而乱序肽对细胞增殖无显著影响(p>0.05),表明H-RN可特异性抑制VEGF诱导的内皮细胞增殖。
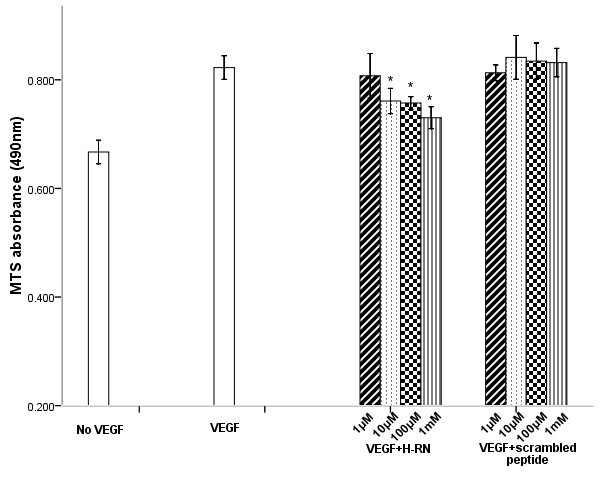
产品关联:实验所用关键产品:Promega的CellTiter96 AQueous One Solution Cell Proliferation Assay(MTS)试剂盒、Sigma-Aldrich的VEGF蛋白。
3.2 内皮细胞迁移能力检测
实验目的:探究H-RN对VEGF诱导的HUVEC迁移的抑制作用。
方法细节:将饥饿后的HUVEC与不同浓度H-RN(1nM、10nM、100nM、1μM)或乱序肽预孵育30min,接种于Transwell上室,下室加入含VEGF(100ng/ml)的无血清培养基,孵育24h后,用棉签去除上室未迁移的细胞,固定并染色下室的迁移细胞,随机选取5个×200视野计数细胞数量,每组实验重复3次。
结果解读:如图2所示,与对照组相比,VEGF可显著促进HUVEC迁移(p<0.001);H-RN在100nM及1μM浓度时可显著抑制细胞迁移(p<0.001),而乱序肽在1μM浓度下仍无抑制作用(p>0.05),表明H-RN可特异性阻断VEGF诱导的内皮细胞迁移。
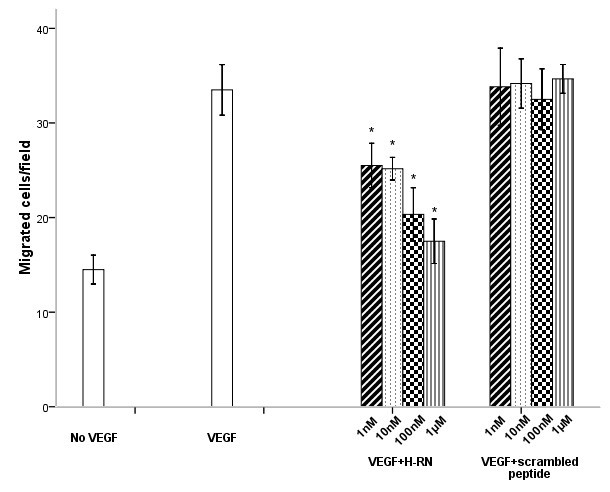
产品关联:实验所用关键产品:Corning的Transwell小室、Gram染色试剂、Olympus的光学显微镜。
3.3 内皮细胞管形成实验
实验目的:验证H-RN对VEGF诱导的HUVEC管形成(血管样结构生成)的抑制作用。
方法细节:将Matrigel包被于96孔板,饥饿后的HUVEC与不同浓度H-RN或乱序肽预孵育30min,接种于包被好的孔板中,加入含VEGF(100ng/ml)的无血清培养基,孵育18h后,通过倒置显微镜观察管形成情况,并用Image-Pro Plus软件定量分析管长度,每组实验重复3次。
结果解读:如图3所示,VEGF可显著诱导HUVEC形成完整的血管样结构(p<0.001);H-RN在100μM及以上浓度时可显著抑制管形成(p<0.001),而乱序肽在任何浓度下均无抑制作用(p>0.05),表明H-RN可有效阻断内皮细胞的血管分化过程。
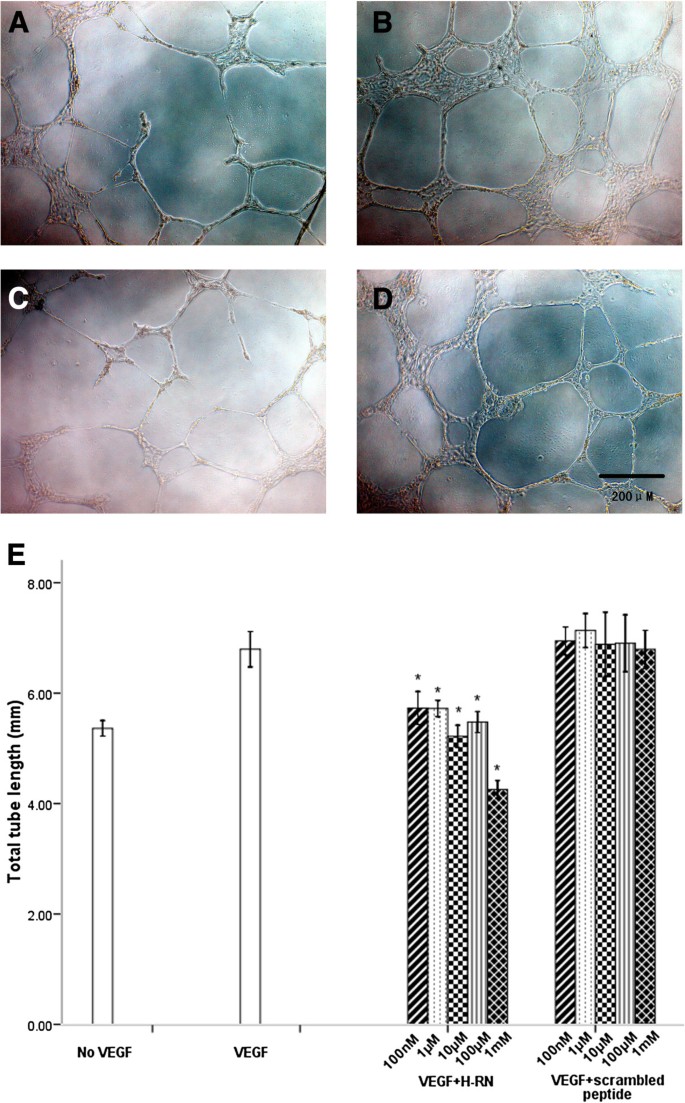
产品关联:实验所用关键产品:BD Biosciences的Matrigel基质胶、Olympus的倒置显微镜、Image-Pro Plus图像分析软件。
3.4 体内角膜新生血管模型验证
实验目的:在动物模型中验证H-RN对VEGF诱导的角膜新生血管的抑制作用。
方法细节:将7-9周龄C57BL/6J小鼠分为4组(每组n=8),采用角膜微袋模型,将含PBS、VEGF(160ng)、VEGF+1μg H-RN、VEGF+5μg H-RN的缓释微丸植入角膜基质袋,术后7天麻醉小鼠,通过立体显微镜观察角膜新生血管生长情况,测量血管最长长度和血管累及的时钟小时数,计算血管面积。
结果解读:如图4所示,PBS组无明显新生血管,VEGF组角膜新生血管生长旺盛,而H-RN处理组血管面积显著减小,其中5μg H-RN组抑制作用更明显(p<0.05),表明H-RN在体内可有效抑制VEGF诱导的角膜新生血管。
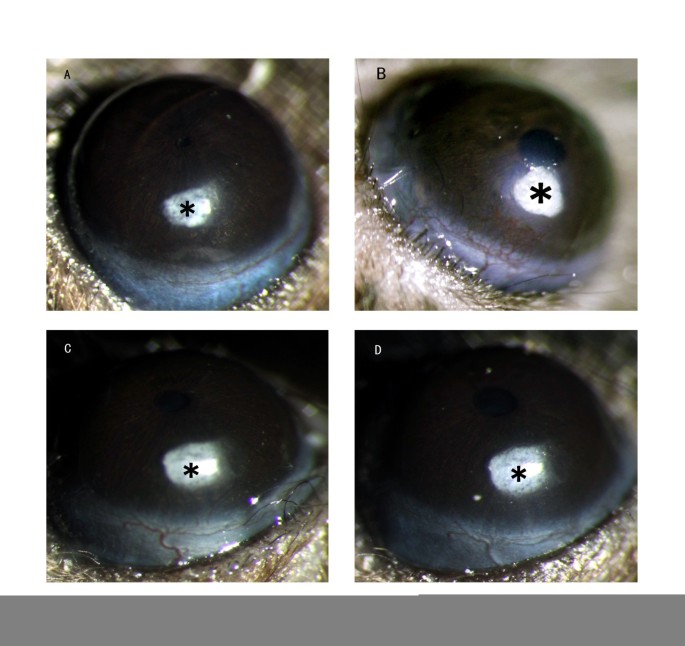
产品关联:实验所用关键产品:polyHEMA缓释微丸、2%水合氯醛麻醉剂、Olympus的SZX2-ILLT立体显微镜。
3.5 内皮细胞凋亡检测
实验目的:探究H-RN是否通过诱导内皮细胞凋亡发挥抗血管生成作用。
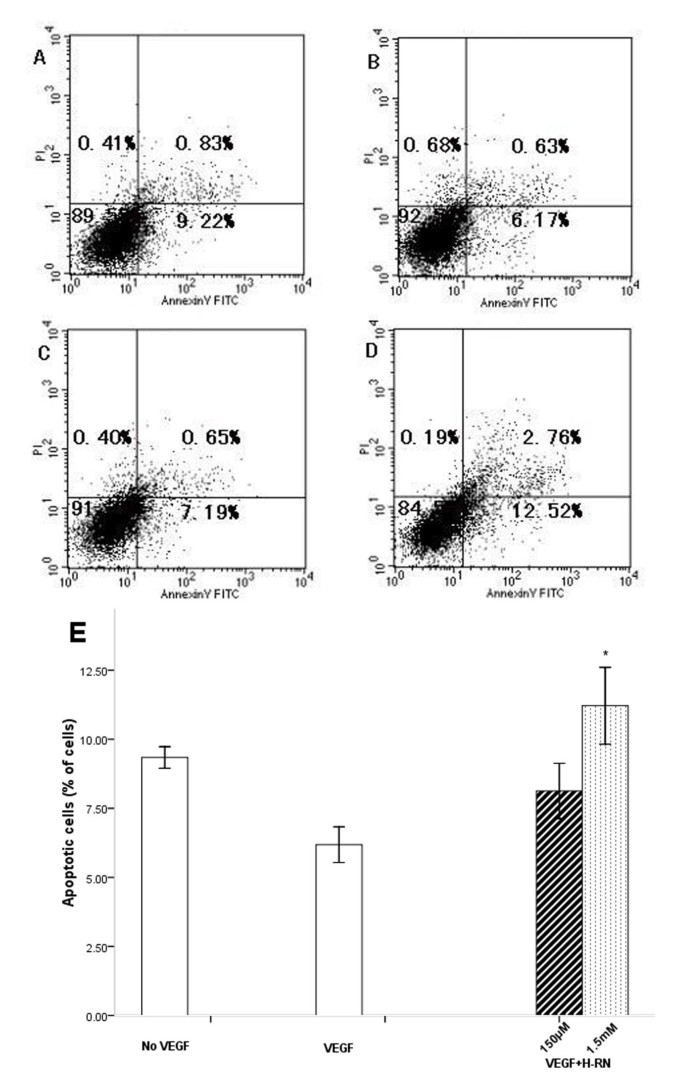
方法细节:将饥饿后的HUVEC与不同浓度H-RN(150μM、1.5mM)预孵育30min,加入VEGF(100ng/ml)处理24h,采用Annexin V-FITC/PI双染色法,通过流式细胞术检测细胞凋亡率,每组实验重复3次。
结果解读:如图5所示,对照组早期凋亡率为9.35±0.27%,VEGF处理后早期凋亡率降至4.76±0.41%,表明VEGF可保护内皮细胞免受凋亡;而150μM和1.5mM H-RN处理后,早期凋亡率分别回升至5.62±0.14%和9.50±0.51%(n=3,p<0.001),表明H-RN可逆转VEGF的抗凋亡作用,诱导内皮细胞凋亡。
产品关联:实验所用关键产品:Invitrogen的Annexin V-FITC/PI凋亡检测试剂盒、BD Biosciences的FACS Calibur流式细胞仪。
3.6 细胞周期分析
实验目的:探究H-RN是否通过阻滞内皮细胞周期发挥抗血管生成作用。
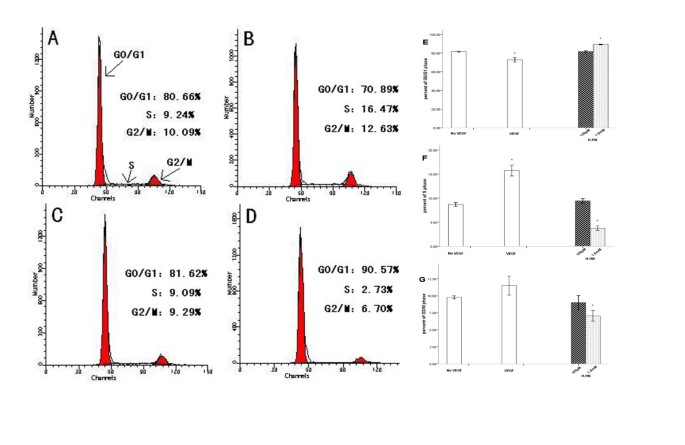
方法细节:将饥饿后的HUVEC与H-RN(150μM、1.5mM)或VEGF处理24h,用70%乙醇固定细胞,PI染色后通过流式细胞术分析细胞周期分布,每组实验重复3次。
结果解读:如图6所示,对照组G0/G1期细胞比例为81.53%,S期为8.70%;VEGF处理后S期细胞比例升至15.73%(n=3,p<0.05),表明VEGF可促进细胞进入增殖期;而1.5mM H-RN处理后,G0/G1期细胞比例升至89.20%,S期和G2/M期细胞比例显著降低(n=3,p<0.05),表明H-RN可将细胞周期阻滞于G0/G1期,抑制细胞增殖。
产品关联:实验所用关键产品:BD Biosciences的FACS Calibur流式细胞仪、PI染色试剂、RNase A酶。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker为H-RN肽段,属于治疗性抗血管生成生物标志物,其筛选与验证逻辑为“前期视网膜新生血管模型活性验证→本次角膜新生血管体内外功能验证→作用机制阐明”的完整链条。
Biomarker定位:H-RN是来源于肝细胞生长因子 kringle 1结构域的小分子肽段(氨基酸序列RNPRGEEGGPW,分子量1254.34Da),其筛选逻辑为前期研究发现其对视网膜新生血管有抑制作用,本次研究进一步验证其在角膜新生血管中的活性,并明确其作用机制。
研究过程详述:H-RN通过固相多肽合成法制备,经高效液相色谱(HPLC)和质谱(MS)鉴定纯度与结构;验证方法包括体外HUVEC的增殖、迁移、管形成实验,体内小鼠角膜微袋模型实验,以及流式细胞术检测凋亡和细胞周期;特异性方面,乱序肽无任何抑制作用,表明H-RN的活性依赖于特定的氨基酸序列;敏感性数据显示,体外实验中1mM H-RN可达到最大增殖抑制效果,体内实验中5μg H-RN即可显著抑制角膜新生血管面积(n=8,p<0.05)。
核心成果提炼:H-RN作为抗血管生成肽段,其功能关联为可有效抑制VEGF诱导的角膜新生血管,其创新性在于首次在角膜新生血管模型中验证H-RN的活性,并阐明其通过逆转VEGF的抗凋亡作用(早期凋亡率从4.76%升至9.50%,n=3,p<0.001)和阻滞细胞周期于G0/G1期(G0/G1期比例从81.53%升至89.20%,n=3,p<0.05)的双重机制发挥作用。该成果为角膜新生血管的治疗提供了一种低毒高效的候选肽类药物,具有潜在的临床转化价值,相比现有治疗药物,H-RN具有更低的有效剂量和更短的治疗周期,且生产成本更低,有望成为角膜新生血管治疗的新选择。
