1. 领域背景与文献引入
文献英文标题:An update on novel approaches for diagnosis and treatment of SARS-CoV-2 infection;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:冠状病毒病(COVID-19)诊断与治疗
2019年底新型冠状病毒(SARS-CoV-2)引发的冠状病毒病(COVID-19)在全球暴发,截至2021年6月,累计确诊病例超1.8亿,死亡超390万,给全球公共卫生和经济造成严重危机。
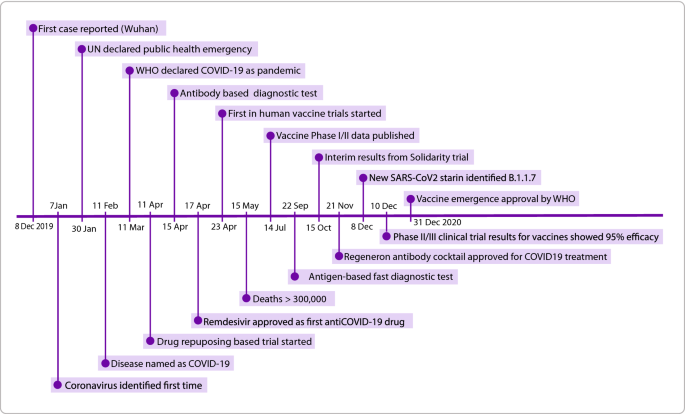
领域共识:SARS-CoV-2是一种有包膜的正链信使核糖核酸(mRNA)病毒,基因组约30kb,编码刺突蛋白(S)、包膜蛋白(E)、膜蛋白(M)和核衣壳蛋白(N)等结构蛋白,病毒通过S蛋白的受体结合域(RBD)与宿主细胞的血管紧张素转换酶2(ACE2)等受体结合实现入侵。疫情期间,病毒不断出现变异,2020年2月出现的D614G突变株传染性增强,随后Alpha、Beta、Gamma、Delta等变异株相继出现,给诊断准确性、治疗效果和疫苗保护力带来挑战。
现有诊断方法中,逆转录聚合酶链反应(RT-PCR)是检测SARS-CoV-2的金标准,但存在检测耗时、需要专业技术人员和设备的局限性;床旁检测(POC)方法虽能快速出结果,但部分产品的敏感性和特异性有待提升。治疗方面,瑞德西韦、地塞米松等药物获紧急使用授权,单克隆抗体可有效中和病毒,但变异株的出现可能导致抗体逃逸;疫苗研发取得快速进展,灭活疫苗、信使核糖核酸疫苗、腺病毒载体疫苗等相继获批,但仍需应对变异株的挑战。在此背景下,本文通过跨学科综述的方式,整合了人工智能、纳米技术、规律间隔成簇短回文重复序列(CRISPR)技术、质谱技术等多领域的新型诊断与治疗方法,旨在为不同学科的研究者提供全面的技术概览,助力资源优先分配与后续研究。
2. 文献综述解析
本文作者以COVID-19的诊断、治疗与疫苗开发为核心框架,按技术类型对领域内现有研究进行分类整合,涵盖分子生物学、纳米科学、人工智能、临床医学等多学科方向,系统梳理了各技术的优势、局限性及应用前景,凸显了跨学科技术在COVID-19防控中的重要价值。
现有研究的关键结论显示,诊断领域,逆转录聚合酶链反应因高特异性仍为金标准,床旁检测可实现快速筛查,但不同平台的敏感性差异较大;治疗领域,抗病毒药物、抗炎药物可改善患者预后,单克隆抗体能有效中和病毒,但易受变异株影响;疫苗领域,多种平台的疫苗已进入临床应用,信使核糖核酸疫苗展现出高效的保护力,但对变异株的保护效果有所下降。技术方法优势方面,逆转录聚合酶链反应的检测特异性可达99%以上,床旁检测可在数小时内出结果,单克隆抗体具有精准的靶向性;局限性方面,逆转录聚合酶链反应检测耗时通常需4-6小时,部分床旁检测的敏感性仅为70%-80%,单克隆抗体对携带特定突变的变异株中和活性显著降低,疫苗对Delta等变异株的保护力下降。
本文的创新价值在于,首次跨学科整合了多个领域的新型技术,不仅涵盖传统的诊断与治疗方法,还纳入了人工智能辅助诊断、CRISPR基因编辑治疗、纳米药物递送等前沿技术,弥补了此前单一领域综述的局限性,为跨学科研究团队提供了全面的技术参考,有助于推动多学科交叉的COVID-19防控技术研发。
3. 研究思路总结与详细解析
本文为系统性综述研究,核心目标是全面总结COVID-19诊断、治疗与疫苗开发的跨学科新型技术,明确各技术的应用场景与发展潜力,核心科学问题是如何通过多学科技术融合提升COVID-19的诊断效率、治疗效果与疫苗保护力,技术路线为:系统检索领域内最新研究文献→按诊断、治疗、疫苗开发三大方向分类→每个方向下按技术类型细分并梳理核心研究结果→总结各技术的优势、局限性及未来研究方向。
3.1 新型诊断技术综述
实验目的:梳理并总结COVID-19的新型跨学科诊断技术,弥补现有诊断方法的不足,提升检测的快速性、敏感性与可及性。
方法细节:通过PubMed、Web of Science等数据库检索2020-2021年发表的相关研究,整合多重实时逆转录聚合酶链反应、CRISPR-based、纳米基、质谱基、人工智能辅助等诊断技术的核心数据与研究结论。
结果解读:多重实时逆转录聚合酶链反应技术可同时检测SARS-CoV-2与流感病毒A/B,其中Norz等开发的检测方法对三种病毒的敏感性分别为98.1%、97.7%、100%(文献未明确样本量及P值);CRISPR-based诊断技术中,DETECTR、SHERLOCK等方法获美国FDA紧急使用授权,Rauch等开发的无需预扩增的CRISPR-Cas13a检测可在30分钟内达到100 copies/ml的敏感性,且可通过手机显微镜读取结果;纳米基诊断技术中,Moitra等开发的金纳米颗粒比色法可在10分钟内检测SARS-CoV-2的N基因,Seo等开发的场效应管传感器可检测低浓度的S蛋白;质谱技术中,Nachtigall等开发的基质辅助激光解吸电离质谱(MALDI-MS)结合机器学习检测鼻咽拭子样本,准确率达93.9%,假阳性率7%,假阴性率5%(文献未明确样本量及P值);人工智能辅助诊断包括基于症状、咳嗽声的自我筛查工具,以及基于CT影像、血液数据的临床诊断模型,其中Jiang等开发的模型预测患者死亡率的准确率达94%(文献未明确样本量及P值)。
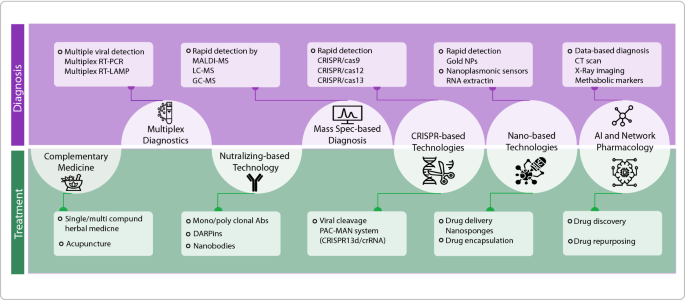
产品关联:文献未提及具体实验产品,领域常规使用逆转录聚合酶链反应试剂盒、CRISPR-Cas蛋白试剂、金纳米颗粒材料、MALDI质谱仪、人工智能算法平台等。
3.2 新型治疗技术综述
实验目的:梳理并总结COVID-19的新型跨学科治疗技术,包括中和因子、CRISPR基因编辑治疗、纳米药物递送、人工智能药物重定位、传统医药等,为临床治疗提供新的策略。
方法细节:系统检索领域内关于COVID-19治疗的最新研究,按技术类型整合各方法的作用机制、临床进展与核心数据。
结果解读:中和因子方面,Casirivimab与Imdevimab联合使用获FDA紧急使用授权,用于轻中度COVID-19患者;多克隆抗体如SAB-185处于临床研究阶段,可降低病毒逃逸风险;纳米抗体如Gai等开发的NB11-59可有效阻断S蛋白RBD与ACE2的结合,抑制病毒感染;DARPins如MP0420对Alpha、Beta等变异株仍具有高效的中和活性;CRISPR基因编辑治疗方面,Abbott等开发的PAC-MAN系统可在人肺上皮细胞系中抑制SARS-CoV-2的RdRP蛋白和N蛋白表达,抑制率分别为85%和70%(n=3,文献未明确P值);纳米药物递送方面,脂质纳米颗粒被用于信使核糖核酸疫苗的递送,Zhang等开发的细胞纳米海绵可通过表达ACE2中和SARS-CoV-2;人工智能药物重定位方面,通过机器学习从4895种药物中筛选出10种潜在的抗SARS-CoV-2化合物,网络医学方法发现托瑞米芬可阻断ACE2与S蛋白的结合;传统医药方面,Valizadeh等的临床研究显示纳米姜黄素可降低COVID-19患者血清中的IL-6和IL-1β水平(文献未明确样本量及P值),连花清瘟胶囊获中国国家药品监督管理局批准用于改善COVID-19症状。
产品关联:文献未提及具体实验产品,领域常规使用单克隆抗体药物、CRISPR递送载体、纳米药物载体、人工智能药物筛选平台、传统中药制剂等。
3.3 疫苗开发新进展综述
实验目的:总结COVID-19疫苗开发的现有平台与新型技术,包括已获批疫苗与处于研究阶段的候选疫苗,为疫苗研发提供参考。
方法细节:检索WHO疫苗研发数据库及相关研究文献,整合各疫苗平台的技术原理、临床进展与核心数据,并开发在线仪表盘提供疫苗更新信息。
结果解读:已获批疫苗包括灭活疫苗(科兴CoronaVac、国药BBIBP-CorV)、信使核糖核酸疫苗(辉瑞BNT162b2、Moderna mRNA1273)、腺病毒载体疫苗(卫星V、牛津-阿斯利康AZD1222、强生Ad26.COV2.S);新型疫苗平台包括植物基疫苗(烟草表达SARS-CoV-2核衣壳蛋白)、酵母表达病毒样颗粒(VLP)疫苗;作者开发的在线仪表盘(http://vafaeelab.com/COVID19_vaccine.html)可提供全球获批疫苗及临床阶段疫苗的最新信息。
产品关联:文献未提及具体实验产品,领域常规使用疫苗生产平台(灭活、信使核糖核酸、腺病毒载体)、植物表达系统、酵母表达系统等。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker涵盖病毒学Biomarker、宿主炎症Biomarker与代谢组学Biomarker三大类,通过多技术平台的筛选与验证,为COVID-19的诊断、治疗与预后评估提供了多维度的指标体系。
Biomarker定位方面,病毒学Biomarker包括SARS-CoV-2的N、E、S、ORF1ab基因及S蛋白RBD,筛选逻辑为基于病毒基因组的保守区域设计检测靶点,通过逆转录聚合酶链反应、CRISPR、质谱等技术验证;宿主炎症Biomarker包括IL-6、IL-1β、C反应蛋白(CRP)等,筛选逻辑为基于COVID-19患者的炎症反应特征,通过酶联免疫吸附试验(ELISA)、实时荧光定量PCR等技术验证;代谢组学Biomarker包括呼出气体中的乙醛、辛醛等挥发性有机物,筛选逻辑为基于患者的代谢特征,通过气相色谱-离子迁移谱(GC-IMS)等技术验证。
研究过程详述显示,病毒学Biomarker的来源为患者鼻咽拭子、血液、痰液等样本,验证方法包括逆转录聚合酶链反应(检测限可达100 copies/ml)、CRISPR检测(检测限可达100 copies/ml)、质谱检测(检测限可达10^4 PFU/ml);宿主炎症Biomarker的来源为患者血清样本,验证方法包括ELISA(IL-6检测限可达1 pg/ml)、实时荧光定量PCR(IL-6 mRNA表达水平检测);代谢组学Biomarker的来源为患者呼出气体样本,验证方法为GC-IMS(准确率可达80%,文献未明确样本量及P值)。
核心成果提炼显示,病毒学Biomarker可作为COVID-19的诊断指标,其中N基因因保守性高被广泛用于逆转录聚合酶链反应检测;S蛋白RBD可作为治疗靶点,单克隆抗体、纳米抗体可靶向结合该区域阻断病毒入侵;宿主炎症Biomarker中,IL-6水平升高与COVID-19患者的重症化及死亡风险相关(文献未明确提供具体风险比、样本量及P值);代谢组学Biomarker可作为快速筛查指标,区分疑似COVID-19患者与健康人群。本文的创新性在于首次跨学科整合了病毒学、宿主炎症与代谢组学Biomarker,为COVID-19的全流程防控提供了多维度的Biomarker策略,弥补了单一Biomarker的局限性。
