1. 领域背景与文献引入
文献英文标题:Regulation of triglyceride metabolism by glucocorticoid receptor;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:代谢生物学(甘油三酯代谢调控、糖皮质激素信号通路)
甘油三酯稳态是维持哺乳动物能量代谢平衡的核心环节,脂生成与脂解过程的动态平衡保障了机体在禁食、进食等不同生理状态下的能量供需稳定。领域共识:糖皮质激素作为关键内分泌调节因子,在脂代谢调控中发挥复杂且双向的作用——禁食状态下促进脂肪细胞脂解,为肝脏和骨骼肌供能;进食状态下协同胰岛素参与脂生成,提升营养利用效率。领域发展关键节点可分为三个阶段:早期生理实验阶段(20世纪70-80年代)发现糖皮质激素对脂代谢的生理调控作用;分子生物学阶段(90年代-21世纪初)鉴定了部分受糖皮质激素调控的脂代谢相关基因;高通量技术阶段(21世纪10年代后)借助染色质免疫沉淀测序(ChIP-seq)等技术,开始全基因组范围内筛选糖皮质激素受体(GR)的直接靶基因。当前研究热点聚焦于糖皮质激素信号紊乱与代谢疾病的关联,如库欣综合征患者的脂肪分布异常、胰岛素抵抗、脂肪肝等,但未解决的核心问题包括:GR调控甘油三酯代谢的系统性靶基因网络尚未明确,GR与其他转录因子的协同调控机制仍不清晰,不同脂肪组织部位的特异性调控逻辑有待阐明。针对上述研究空白,本文通过整合现有研究数据,系统性概述GR调控脂生成与脂解通路的靶基因及其转录调控机制,为理解糖皮质激素相关代谢疾病的发病机制及后续治疗靶点开发提供理论基础。
2. 文献综述解析
作者以GR调控的代谢通路为核心分类维度,将现有研究分为脂生成通路调控、脂解通路调控及转录调控因子协同作用三个方向,系统梳理了GR在甘油三酯代谢中的调控网络。
现有研究的关键结论显示,糖皮质激素在不同生理状态下对甘油三酯代谢的调控具有双向性:禁食时通过促进脂肪细胞脂解,将甘油三酯分解为游离脂肪酸供机体供能;进食时则协同胰岛素激活脂生成通路,促进能量储存。库欣综合征患者的临床表型进一步证实了糖皮质激素的调控特异性——腹部、锁骨上等中心脂肪部位脂肪堆积,而四肢皮下脂肪减少,体现了其对不同脂肪组织的差异化调控。技术方法层面,ChIP-seq技术的应用实现了全基因组范围内GR结合区域的鉴定,为筛选GR直接靶基因提供了高通量手段,但现有研究仍存在局限性:多数靶基因的功能验证仅停留在细胞系或动物模型层面,缺乏临床样本的直接验证;部分GR结合区域的功能未被充分证实,传统报告基因实验无法完全模拟内源性基因组的调控环境;对GR与其他转录因子的协同调控机制研究较为零散,缺乏系统性整合。本文的创新价值在于首次系统性整合了GR调控甘油三酯代谢的靶基因网络,明确了脂生成与脂解通路中的GR直接靶基因及间接调控基因,同时深入探讨了GR与Med1、肝X受体(LXR)等转录调控因子的协同作用机制,填补了GR转录调控复合物在甘油三酯代谢中作用的研究空白,为代谢疾病的精准治疗提供了更全面的分子基础。
3. 研究思路总结与详细解析
本文以系统性整合现有研究为核心思路,研究目标是明确GR调控甘油三酯代谢的靶基因网络及转录调控机制,核心科学问题是GR如何通过转录调控维持或紊乱甘油三酯稳态,技术路线为按脂生成、脂解通路分类梳理GR靶基因,结合ChIP-seq数据鉴定直接靶基因,探讨转录调控复合物的协同作用。
3.1 脂生成通路GR靶基因的系统分析
实验目的为鉴定GR在脂生成通路中的直接与间接靶基因,明确其与胰岛素的协同调控机制。方法细节上,作者整合了3T3-L1脂肪细胞的ChIP-seq研究数据,分析脂生成相关基因的GR结合区域分布;通过报告基因实验验证GR结合区域的糖皮质激素响应活性;同时结合细胞系与动物模型的基因表达数据,验证糖皮质激素对脂生成基因的调控作用。结果解读显示,乙酰辅酶A羧化酶1、乙酰辅酶A羧化酶2、脂肪酸合酶、硬脂酰辅酶A去饱和酶1、甘油-3-磷酸酰基转移酶3等基因的基因组区域存在GR结合区域,其中除溶血磷脂酸酰基转移酶2外,其余基因的GR结合区域均可介导糖皮质激素响应,提示为GR直接靶基因;糖皮质激素与胰岛素具有协同调控作用,两者共同处理时,乙酰辅酶A羧化酶1、乙酰辅酶A羧化酶2和脂肪酸合酶的基因表达水平显著高于单独处理组,体现了激素间的正交互作用。
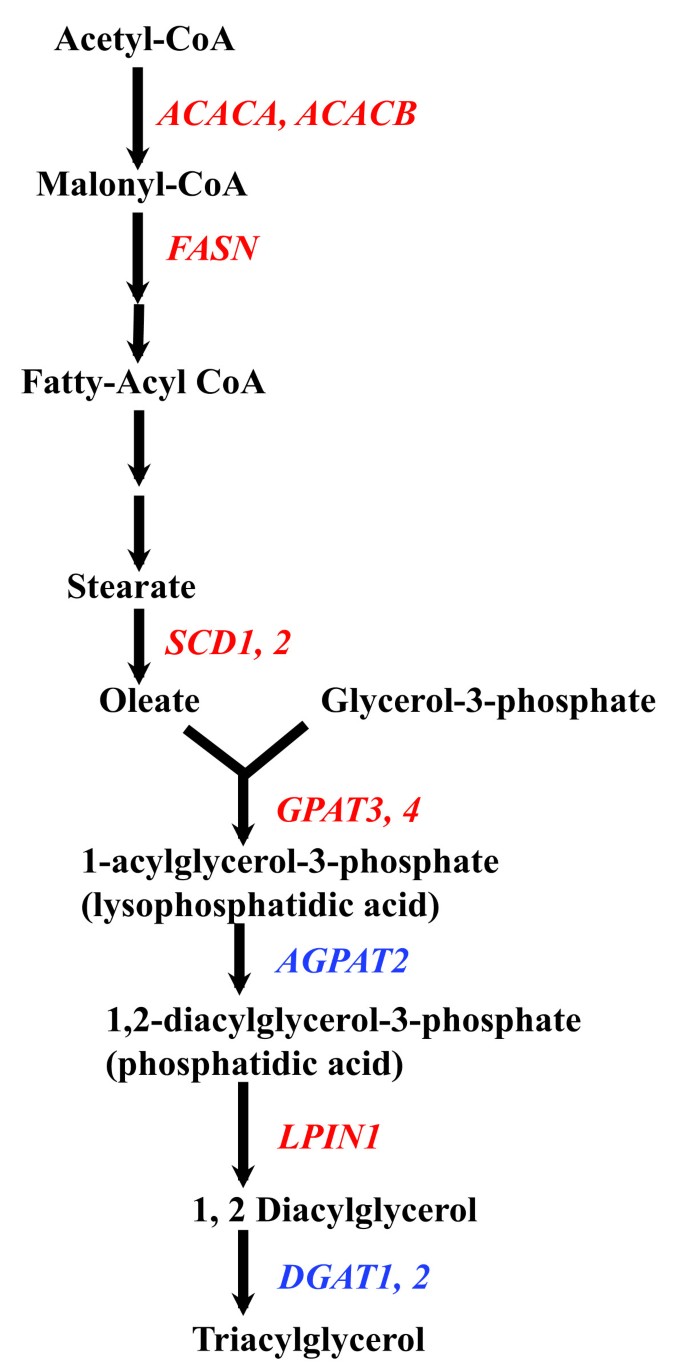
产品关联:文献未提及具体实验产品,领域常规使用ChIP-seq试剂盒、实时荧光定量PCR试剂、报告基因检测系统等。
3.2 脂解通路GR靶基因的功能解析
实验目的为解析GR在脂解通路中的靶基因及调控机制,明确其对cAMP信号通路的调控作用。方法细节上,作者梳理了脂解相关基因的GR调控研究,结合ChIP-seq数据鉴定GR结合区域;通过血管生成素样蛋白4(ANGPTL4)基因敲除小鼠模型,验证其在糖皮质激素诱导脂解中的功能;同时分析糖皮质激素对脂肪细胞cAMP水平的影响及分子机制。结果解读显示,激素敏感性脂肪酶和单酰基甘油脂肪酶的基因组区域存在GR结合区域,为GR直接靶基因;脂肪甘油三酯脂肪酶的表达可能通过GR上调叉头框蛋白O1间接调控;糖皮质激素通过两种机制激活cAMP-PKA通路:一是抑制磷酸二酯酶3B的表达,减少cAMP的水解;二是诱导ANGPTL4的表达,ANGPTL4通过激活cAMP通路促进脂解,ANGPTL4敲除小鼠的糖皮质激素诱导脂解作用显著减弱,证实了其关键调控作用。
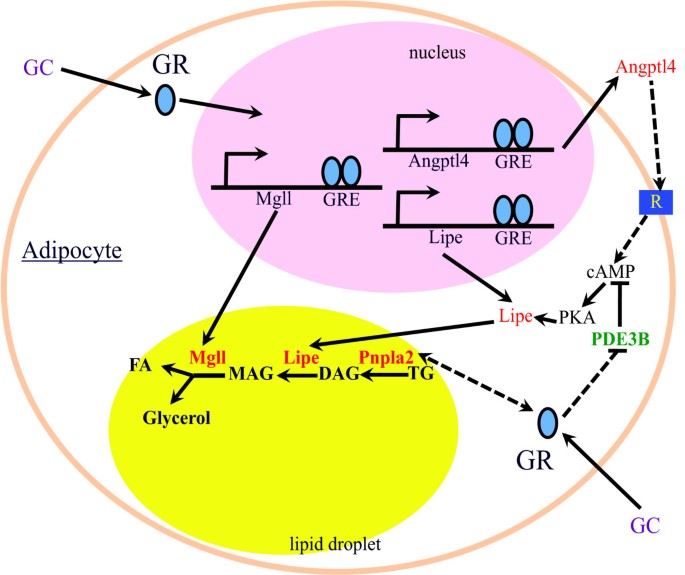
产品关联:文献未提及具体实验产品,领域常规使用基因编辑工具(如CRISPR-Cas9系统)、酶联免疫吸附实验试剂盒、cAMP检测试剂等。
3.3 GR与转录调控因子的协同作用研究
实验目的为探讨GR与其他转录调控因子在甘油三酯代谢中的协同调控机制,明确其对代谢疾病表型的影响。方法细节上,作者分析了中介体复合物亚基Med1敲除小鼠的糖皮质激素诱导脂肪肝表型;通过ChIP实验验证LXR与GR在靶基因调控中的竞争结合作用。结果解读显示,Med1作为GR的共激活因子,参与糖皮质激素对脂氧化基因的抑制作用,肝脏特异性Med1敲除小鼠的糖皮质激素诱导脂肪肝表型显著减轻,原因是脂氧化基因的表达抑制作用减弱;未配体结合的LXRβ可作为共激活因子促进GR的靶基因转录,而LXR配体则通过竞争结合糖皮质激素响应元件,抑制GR的转录激活作用,从而改善糖皮质激素诱导的高血糖症状。产品关联:文献未提及具体实验产品,领域常规使用免疫共沉淀试剂盒、ChIP实验试剂、基因敲除动物模型等。
4. Biomarker研究及发现成果解析
本文作为综述性研究,系统性梳理了GR调控甘油三酯代谢的潜在Biomarker,包括GR直接靶基因及其表达产物,为代谢疾病的Biomarker筛选提供了候选基因库。
Biomarker定位方面,文中涉及的Biomarker主要为GR靶基因及其表达产物,类型包括分泌蛋白(如ANGPTL4)、代谢酶(如激素敏感性脂肪酶、单酰基甘油脂肪酶)、转录调控因子(如Hes1、脂磷蛋白1),筛选与验证逻辑为:基于ChIP-seq技术鉴定GR结合区域,筛选潜在直接靶基因;通过细胞系、动物模型的功能实验验证其在甘油三酯代谢中的调控作用;结合临床疾病表型(如库欣综合征)分析其与代谢紊乱的关联。研究过程详述:ANGPTL4作为分泌型蛋白,在禁食状态下被糖皮质激素诱导表达,通过激活cAMP通路促进脂解,ANGPTL4敲除小鼠可抵抗糖皮质激素诱导的脂肪肝和高脂血症,提示其可作为糖皮质激素诱导代谢紊乱的潜在Biomarker;脂磷蛋白1具有双重功能,既参与甘油三酯合成的酶学反应(磷脂酸磷酸酶活性),又在禁食时参与脂氧化基因的转录调控;Hes1作为转录抑制因子,被糖皮质激素抑制后,肝脏脂解酶基因表达降低,导致肝脏甘油三酯积累。特异性与敏感性数据方面,文中未提供临床样本的ROC曲线、敏感性及特异性数值,但动物模型实验证实ANGPTL4的功能缺失可显著改善糖皮质激素诱导的代谢紊乱表型,提示其具有较高的功能特异性。核心成果提炼:ANGPTL4作为GR直接靶基因,是糖皮质激素诱导脂解的关键介质,其表达异常与脂肪肝、高脂血症密切相关;脂磷蛋白1的双重功能揭示了甘油三酯代谢调控的复杂性;Hes1通过调控肝脏脂解过程影响甘油三酯积累。创新性在于首次系统性整合了GR调控甘油三酯代谢的潜在Biomarker网络,为代谢疾病的早期诊断、预后评估提供了候选靶点,同时为后续Biomarker的临床验证奠定了理论基础。
