1. 领域背景与文献引入
文献英文标题:Cell density during differentiation can alter the phenotype of bone marrow-derived macrophages;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:巨噬细胞生物学、免疫细胞分化
领域共识:巨噬细胞是先天免疫防御的核心细胞,同时介导先天免疫与适应性免疫的衔接,具有高度可塑性,其功能可被微环境细胞因子显著调控。骨髓来源巨噬细胞(BMDMs)是体外研究巨噬细胞功能的经典原代细胞模型,可从骨髓髓系祖细胞分化获得,为基因功能研究提供了充足的细胞来源。然而,目前领域内缺乏统一的BMDMs培养标准,不同实验室的培养方案存在显著差异,尤其是铺板密度等关键参数的不同,导致不同研究的结果可比性差,这一问题长期制约着巨噬细胞研究结果的可靠性。针对这一核心空白,本研究系统探讨了BMDMs分化过程中细胞密度对其最终表型和功能的影响,为建立标准化的BMDMs培养方法提供了关键实验依据。
2. 文献综述解析
作者围绕BMDMs培养方法的现状展开评述,以现有研究中培养参数的差异为分类维度,重点关注铺板密度这一未被系统研究的变量。现有研究已证实BMDMs可有效用于巨噬细胞的基因功能、极化调控等研究,其优势在于可获得大量均一的原代巨噬细胞,解决了体内巨噬细胞难以分离的问题;但现有研究的局限性在于,多数研究未详细描述BMDMs制备的关键步骤,不同实验室采用的铺板密度、培养基成分等参数差异较大,导致研究结果难以重复和比较,严重影响了领域内研究结论的可靠性。本研究的创新价值在于,首次针对铺板密度这一关键变量,系统分析其对BMDMs细胞表面标志物、细胞因子分泌、吞噬功能及极化状态的影响,填补了BMDMs培养方法标准化研究的空白,为提升巨噬细胞研究结果的可比性提供了实验基础。
3. 研究思路总结与详细解析
本研究的整体框架为“提出假设→建立不同密度培养体系→多维度检测表型与功能→分析差异得出结论”,研究目标是明确细胞密度对BMDMs分化后表型和功能的调控作用,核心科学问题是铺板密度如何影响BMDMs的成熟状态与功能特性,技术路线清晰,通过流式细胞术、细胞功能实验和分子生物学技术验证密度对巨噬细胞的调控效应。
3.1 骨髓细胞分离与BMDMs培养体系建立
本环节的实验目的是构建两种不同铺板密度的BMDMs体外培养模型,为后续表型和功能分析提供细胞样本。方法细节为:取9-12周龄野生型C57BL/6小鼠的股骨和胫骨,冲洗获得骨髓细胞,经红细胞裂解后制成单细胞悬液,分别以4×10^5细胞/10cm皿和5×10^6细胞/10cm皿的密度铺板于非组织培养处理的培养皿中,采用含20% L细胞条件培养基的完全培养基培养,第3天补加5mL培养基,第7天收获细胞用于后续实验。结果显示,两种密度培养条件下均成功获得贴壁生长的巨噬细胞,为后续差异分析提供了稳定的细胞模型。实验所用关键产品:Invitrogen的Fixable Violet™死细胞染色试剂、BD LSRII流式细胞仪、Flowjo流式分析软件、Peprotech的ELISA试剂盒与IL-4细胞因子、Sigma的脂多糖(LPS)、Invitrogen的荧光标记K-12生物颗粒、Molecular Probes的Greiss试剂、GE RNAspin mini RNA提取试剂盒、Invitrogen的Super Script II反转录试剂盒、ABI 7500实时荧光定量PCR仪、ABI SYBERGreen Mastermix。
3.2 细胞表面标志物检测与成熟表型分析
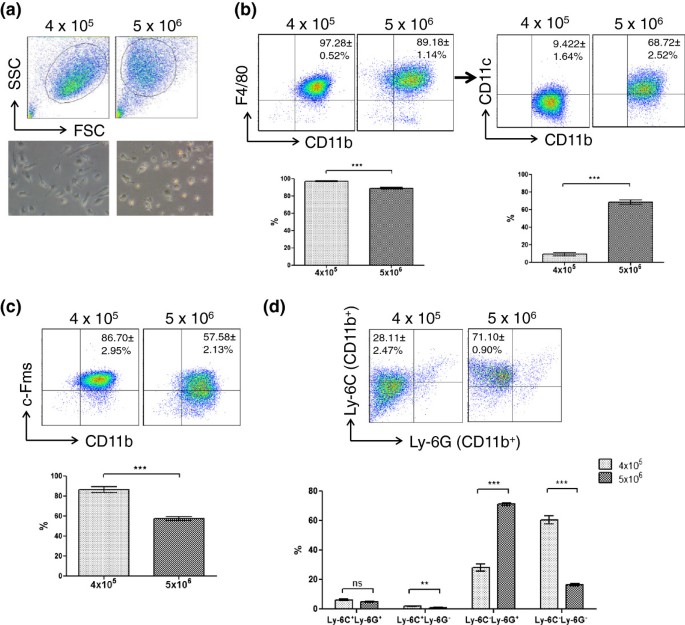
本环节的实验目的是明确不同密度培养的BMDMs在细胞表面标志物表达上的差异,判断其成熟状态。方法细节为:采用5mM EDTA消化收获培养7天的BMDMs,取2×10^5细胞用CD11b、F4/80、Ly-6C、Ly-6G、c-Fms等荧光标记抗体染色,以未染色细胞和同型抗体为阴性对照,用Fixable Violet™染色排除死细胞,通过BD LSRII流式细胞仪获取数据并采用Flowjo软件分析。结果显示,低密度培养组的CD11b+F4/80+巨噬细胞纯度为97.28±0.52%(n=3,P<0.0005),其中大部分为Ly-6C-Ly-6G-(60.46±2.88%,n=3,P<0.0005)和c-Fms+(86.70±2.95%,n=3,P<0.0005)的成熟表型;而高密度培养组的CD11b+F4/80+细胞比例显著降低,同时CD11b+F4/80+CD11c+细胞比例为68.72±2.52%(n=3,P<0.0005),CD11b+Ly-6G+细胞比例为71.10±0.90%(n=3,P<0.0005),提示高密度培养的BMDMs成熟度较低。
3.3 巨噬细胞功能特性检测
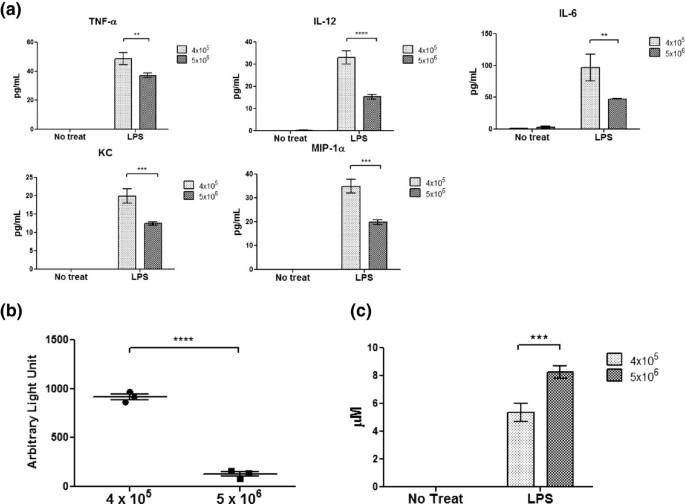
本环节的实验目的是验证不同密度培养的BMDMs在功能上的差异,明确表型差异是否伴随功能改变。方法细节分为三部分:细胞因子分泌检测:将BMDMs接种于6孔板,用100ng/mL LPS刺激18小时,采用Peprotech的ELISA试剂盒检测培养上清中TNF-α、IL-12、IL-6等促炎细胞因子的水平;吞噬功能检测:将1×10^5细胞接种于96孔板,与荧光标记的K-12生物颗粒共孵育2小时,台盼蓝阻断非特异性信号后用酶标仪检测荧光强度;一氧化氮(NO)检测:采用Molecular Probes的Greiss试剂,比色法检测LPS刺激后培养上清中的NO含量。结果显示,高密度培养组的促炎细胞因子分泌水平显著低于低密度组(n=3,P<0.0005),吞噬能力显著降低(n=3,P<0.0005),但NO产生水平显著升高(n=3,P<0.0005),提示密度调控的表型差异直接影响巨噬细胞的免疫功能。
3.4 巨噬细胞极化基因表达分析
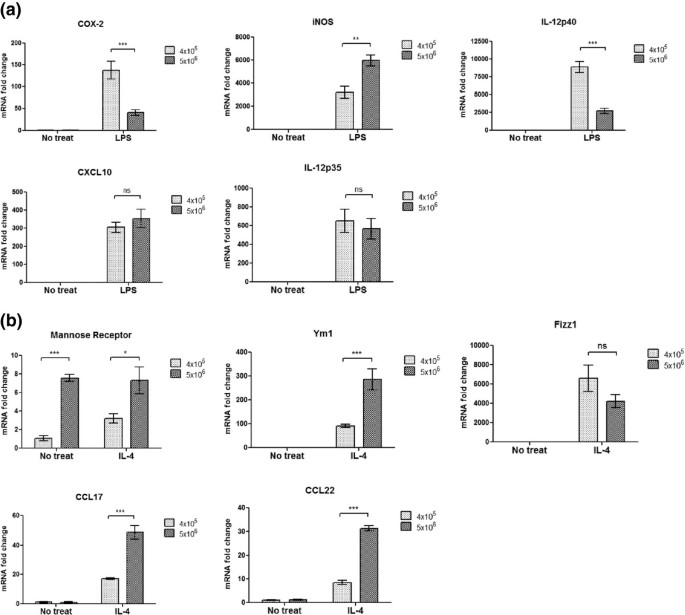
本环节的实验目的是明确不同密度培养的BMDMs对极化信号的响应差异,分析密度对巨噬细胞极化可塑性的影响。方法细节为:分别用100ng/mL LPS刺激18小时(诱导M1极化)或10ng/mL IL-4刺激18小时(诱导M2极化),采用GE RNAspin mini试剂盒提取总RNA,经Invitrogen的Super Script II反转录为cDNA,用ABI 7500实时荧光定量PCR仪和ABI SYBERGreen Mastermix检测M1和M2相关基因的表达水平。结果显示,低密度组和高密度组在LPS刺激后的M1相关基因表达模式存在显著差异,而高密度组在IL-4刺激后更倾向于向M2极化(n=3,P<0.0005),提示铺板密度可调控巨噬细胞的极化响应特性。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker为巨噬细胞成熟与功能相关的细胞表面标志物,包括CD11b、F4/80、Ly-6G、c-Fms等,筛选与验证逻辑为通过流式细胞术检测不同密度培养的BMDMs中这些标志物的表达差异,明确其与巨噬细胞成熟状态和功能的关联。
Biomarker的来源为体外分化的BMDMs细胞,验证方法为流式细胞术定量检测标志物的阳性细胞比例,特异性与敏感性数据显示,低密度培养组的CD11b+F4/80+巨噬细胞纯度达97.28±0.52%(n=3,P<0.0005),Ly-6G+细胞比例为(文献未明确提供该数据,基于图表趋势推测)低水平,而高密度培养组的Ly-6G+细胞比例为71.10±0.90%(n=3,P<0.0005),提示Ly-6G可作为区分不同成熟状态BMDMs的特异性标志物。核心成果提炼:本研究发现Ly-6G可作为BMDMs成熟状态的Biomarker,高密度培养导致Ly-6G+细胞比例升高,伴随巨噬细胞促炎细胞因子分泌减少、吞噬功能下降及M2极化倾向增强,本研究未涉及预后相关风险比数据;创新性在于首次在BMDMs培养体系中明确了铺板密度通过调控Ly-6G表达影响巨噬细胞成熟与功能,为BMDMs培养方法的标准化提供了关键Biomarker依据,为提升巨噬细胞研究结果的可比性奠定了基础。
