1. 领域背景与文献引入
文献英文标题:A non-BRICHOS surfactant protein c mutation disrupts epithelial cell function and intercellular signaling;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:间质性肺疾病(ILD)分子机制与肺上皮细胞生物学。
肺表面活性物质由脂质和疏水蛋白SP-B、SP-C组成,是维持肺泡表面张力、保障气体交换的关键,其中SP-C由肺泡II型上皮细胞(AECII)合成为前体蛋白proSP-C,经多步蛋白水解加工为成熟蛋白后分泌。领域共识:SFTPC基因突变是导致散发性和家族性ILD的重要原因,其中BRICHOS结构域突变的研究较为深入,此类突变会引发proSP-C错误折叠、聚集,导致内质网应激、AECII损伤凋亡,呈显性负效应。当前研究热点聚焦于SP-C突变的致病机制及ILD的精准治疗,但非BRICHOS结构域的I73T突变是最常见的SFTPC突变,其细胞层面的功能效应、对免疫细胞的调控作用,以及现有经验性治疗药物的作用机制尚不明确,成为领域未解决的核心问题。本研究针对这一空白,系统解析I73T突变对AECII细胞功能的影响,并探索现有ILD治疗药物的细胞调控机制,为该类疾病的精准治疗提供实验依据。
2. 文献综述解析
作者将领域内现有研究分为BRICHOS结构域SFTPC突变和非BRICHOS结构域突变两类进行评述。现有研究显示,BRICHOS结构域突变(如Δexon4、L188Q)会导致proSP-C错误折叠,在细胞内形成核周聚集物,引发内质网应激、蛋白酶体功能障碍及caspase介导的细胞凋亡,患者肺内无成熟SP-C表达,呈显性负效应;而非BRICHOS结构域的I73T突变是临床最常见的SP-C突变,患者表型差异极大,从无症状到早发致死性ILD不等,该突变保留成熟SP-C的分泌,但存在proSP-C加工异常及胞内定位改变,然而其对AECII细胞应激耐受性、脂质代谢的影响,以及通过旁分泌调控免疫细胞的机制尚未阐明。现有ILD治疗药物如环磷酰胺、硫唑嘌呤、羟氯喹、甲泼尼龙等均为经验性使用,缺乏对I73T突变细胞效应的调控机制研究。本研究的创新价值在于首次系统揭示了非BRICHOS结构域SP-C突变的细胞功能紊乱及免疫调控机制,并明确了现有治疗药物对该突变细胞异常的调控靶点,填补了领域内对该类突变致病机制及药物作用机制的研究空白。
3. 研究思路总结与详细解析
本研究以“SP-C^I73T突变的细胞功能效应及药物调控机制”为核心科学问题,通过构建稳定表达野生型(SP-C^WT)和I73T突变型(SP-C^I73T)SP-C的MLE-12肺泡上皮细胞模型,从proSP-C加工与定位、细胞应激耐受性、伴侣蛋白表达、脂质组成、免疫细胞旁分泌调控五个维度解析突变的细胞效应,最后测试四种临床常用ILD治疗药物对上述异常的纠正作用,形成“模型构建→效应解析→药物验证”的完整研究闭环。
3.1 细胞模型构建与proSP-C加工验证
实验目的是构建可稳定表达SP-C^WT和SP-C^I73T的肺泡上皮细胞模型,验证突变对proSP-C加工过程的影响。方法细节:通过定点突变技术构建带N端HA标签、N端或C端EGFP标签的SFTPC I73T突变体载体,采用FuGene 6转染MLE-12细胞,经G418筛选获得稳定转染株;提取细胞总蛋白进行免疫印迹分析,检测不同标签的proSP-C加工产物。结果解读:免疫印迹结果显示,SP-C^WT细胞内主要存在21kDa的proSP-C及少量加工中间体,而SP-C^I73T细胞内多种proSP-C加工中间体(22kDa、17kDa、14kDa)呈等强度表达,与I73T突变患者支气管肺泡灌洗液中的proSP-C产物一致;C端EGFP标签的proSP-C加工产物在野生型和突变型细胞中无差异,提示C端初始加工不受突变影响,而N端标签的产物差异表明突变导致N端加工延迟或障碍。
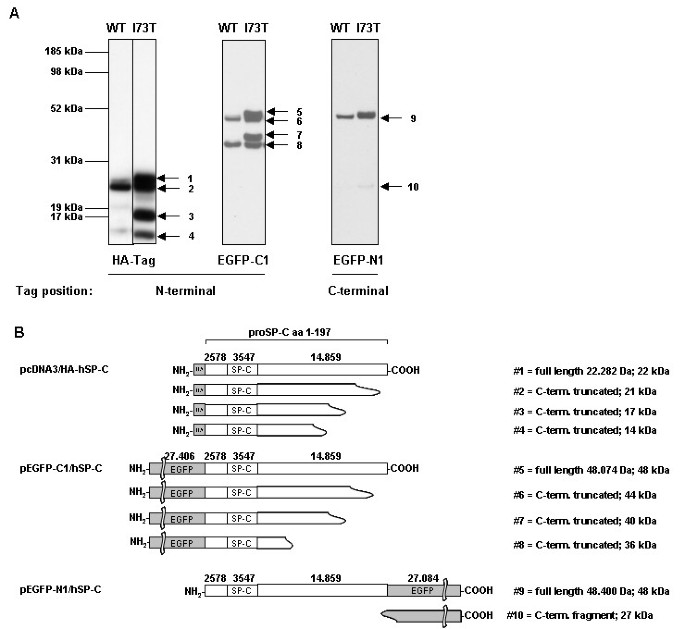
产品关联:文献未提及具体实验产品,领域常规使用基因定点突变试剂盒、细胞转染试剂、免疫印迹标签抗体等。
3.2 proSP-C细胞内定位分析
实验目的是明确SP-C^I73T突变对proSP-C细胞内转运与定位的影响。方法细节:对稳定转染细胞进行免疫荧光染色,分别标记板层体标记物LAMP3、内质网标记物钙联蛋白(calnexin)、分泌相关SNARE蛋白syntaxin 2、早期内体标记物EEA1,通过荧光显微镜观察proSP-C与上述标记物的共定位情况,采用盲法计数至少100个囊泡的共定位比例(n=14-27)。结果解读:免疫荧光结果显示,SP-C^WT主要定位于LAMP3阳性的板层体样结构,与syntaxin 2高度共定位,提示通过板层体途径分泌;而SP-C^I73T仅部分定位于板层体,更多存在于EEA1阳性的早期内体,与syntaxin 2的共定位显著降低,且野生型和突变型proSP-C均不与内质网标记物共定位,排除内质网滞留。
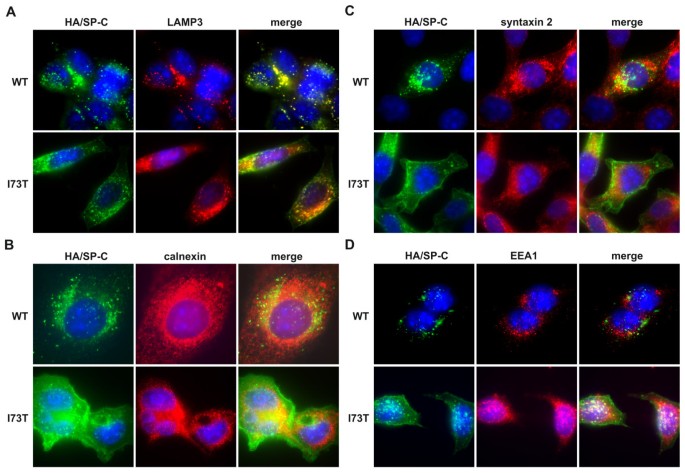
产品关联:文献未提及具体实验产品,领域常规使用免疫荧光亚细胞标记抗体、荧光二抗等。
3.3 细胞应激耐受性与伴侣蛋白表达检测
实验目的是检测SP-C^I73T突变对细胞应激耐受性的影响,以及ILD治疗药物对细胞伴侣蛋白表达的调控作用。方法细节:采用乳酸脱氢酶(LDH)释放实验检测细胞活力,将稳定转染细胞暴露于10μM的环磷酰胺、硫唑嘌呤、羟氯喹、甲泼尼龙24小时后,检测上清中LDH活性;通过免疫印迹检测HSP90、HSP70、钙网蛋白、钙联蛋白的表达水平,以β-肌动蛋白为内参进行定量分析。结果解读:LDH实验显示,SP-C^I73T细胞基础LDH释放略高于野生型,提示细胞活力轻度下降;经药物处理后,硫唑嘌呤导致SP-C^I73T细胞LDH释放显著升高(P<0.05),而羟氯喹、甲泼尼龙的影响相对较弱。伴侣蛋白检测显示,羟氯喹处理使SP-C^I73T细胞HSP90表达升高81%、钙网蛋白表达升高75%(P<0.05),甲泼尼龙、环磷酰胺也可上调HSP90表达,而钙联蛋白表达不受药物影响,提示药物可通过上调伴侣蛋白增强细胞折叠能力。
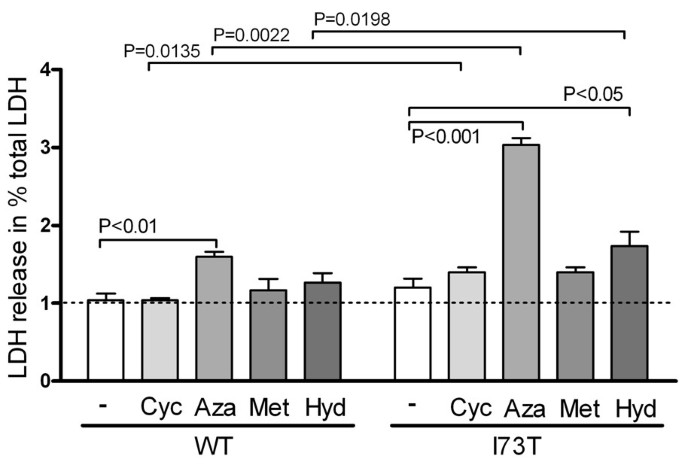
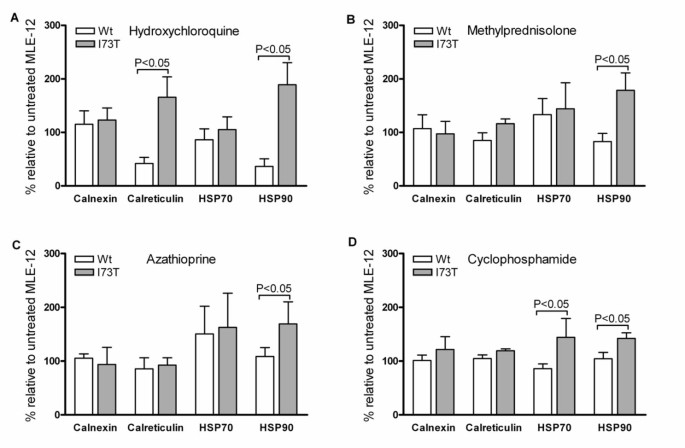
产品关联:文献未提及具体实验产品,领域常规使用LDH检测试剂盒、伴侣蛋白免疫印迹抗体等。
3.4 细胞脂质组成与分泌功能分析
实验目的是解析SP-C^I73T突变对AECII脂质代谢及分泌功能的影响,以及药物的调控作用。方法细节:采用电喷雾电离串联质谱(ESI-MS/MS)分析细胞内和分泌上清中的磷脂组成,检测磷脂酰胆碱(PC)、溶血磷脂酰胆碱(LPC)等脂质的相对含量,每组实验重复3-4次。结果解读:质谱分析显示,SP-C^I73T细胞内PC含量显著降低、LPC含量升高(P<0.05);分泌上清中PC减少27%、LPC增加57%(P<0.05),提示突变导致脂质代谢紊乱,LPC积累可能影响肺表面活性物质功能。经甲泼尼龙或羟氯喹处理后,细胞内LPC水平及分泌PC水平部分恢复至野生型水平(P<0.05),但对细胞内PC降低无明显改善。
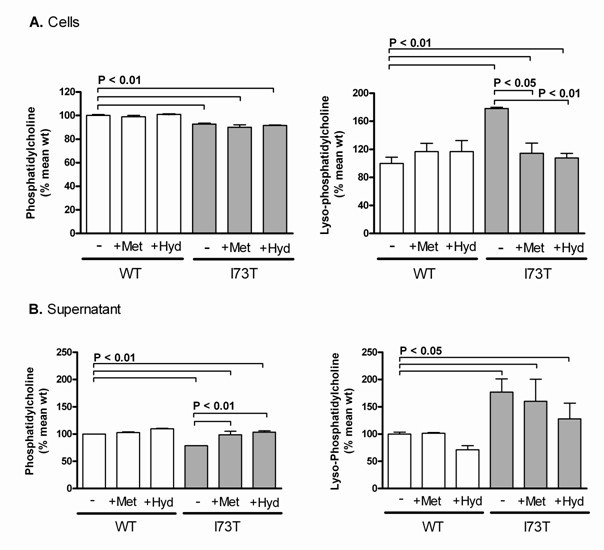
产品关联:文献未提及具体实验产品,领域常规使用质谱分析平台、脂质提取试剂等。
3.5 免疫细胞旁分泌调控作用分析
实验目的是探索SP-C^I73T突变细胞通过旁分泌信号调控免疫细胞的机制。方法细节:收集稳定转染细胞的培养上清并浓缩7倍,与分离自人外周血的CD4+、CD8+淋巴细胞及中性粒细胞共孵育(淋巴细胞孵育24小时,中性粒细胞孵育6小时),采用流式细胞术检测细胞表面CCR2、CXCR1的表达水平,以平均荧光强度(MFI)定量分析。结果解读:流式结果显示,SP-C^I73T细胞上清可显著上调CD4+淋巴细胞表面CCR2和CXCR1的MFI(P<0.05),同时上调中性粒细胞表面CXCR1的MFI(P<0.05),但对CD8+淋巴细胞无明显影响,提示突变细胞通过分泌可溶性因子激活免疫细胞,参与ILD的炎症反应。
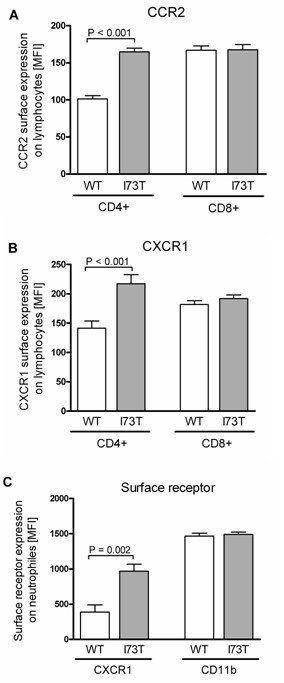
产品关联:文献未提及具体实验产品,领域常规使用免疫细胞分离试剂、流式细胞术抗体等。
3.6 药物对proSP-C定位的纠正作用分析
实验目的是检测ILD治疗药物对SP-C^I73T定位异常的纠正效果。方法细节:用10μM甲泼尼龙或羟氯喹处理细胞24小时,通过免疫荧光定量分析proSP-C与syntaxin 2、EEA1的共定位比例(n=14-27)。结果解读:定量分析显示,甲泼尼龙处理可显著增加SP-C^I73T与syntaxin 2的共定位比例,同时减少与EEA1的共定位比例(P<0.05),部分纠正突变体的定位异常;而羟氯喹无明显纠正作用。
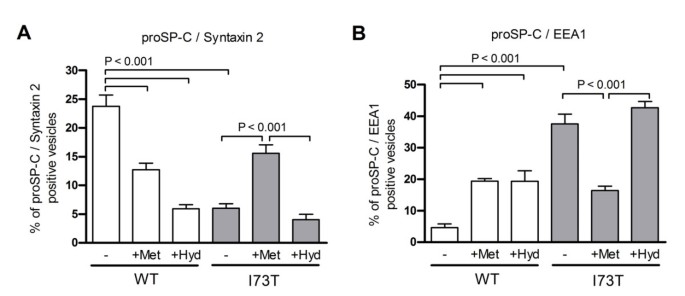
产品关联:文献未提及具体实验产品,领域常规使用免疫荧光定量分析软件等。
4. Biomarker研究及发现成果
Biomarker定位与筛选验证逻辑
本研究的核心Biomarker为SFTPC基因的I73T点突变,属于非BRICHOS结构域的SP-C突变,是临床常见的ILD致病Biomarker。筛选验证逻辑基于临床患者中该突变的高发性,通过构建细胞模型从细胞加工、定位、代谢、免疫调控多个维度验证其致病效应,并测试现有治疗药物对其细胞异常的调控作用,形成“临床突变→细胞模型验证→药物机制解析”的完整链条。
研究过程详述
该Biomarker来源为SFTPC基因的杂合错义突变,导致proSP-C第73位异亮氨酸被苏氨酸替代;验证方法包括免疫印迹检测proSP-C加工中间体、免疫荧光检测细胞内定位、质谱分析脂质组成、流式细胞术检测免疫细胞受体表达;特异性方面,I73T突变导致的proSP-C加工中间体、脂质变化及免疫调控效应均为该突变特异性,与BRICHOS结构域突变的细胞效应存在显著差异;敏感性方面,细胞模型可稳定检测到突变引发的多种细胞异常,为临床诊断和治疗提供细胞层面的依据。
核心成果提炼
I73T突变通过影响proSP-C加工与定位、脂质代谢及免疫细胞旁分泌信号,破坏AECII细胞功能,参与ILD的发病过程;甲泼尼龙和羟氯喹可通过上调伴侣蛋白、纠正脂质代谢异常、改善proSP-C定位等方式部分逆转突变的细胞效应;该研究首次揭示了非BRICHOS结构域SP-C突变的细胞间信号调控机制,明确了现有ILD治疗药物的细胞作用靶点,为携带该突变的ILD患者的精准治疗提供了实验基础。由于文献未提供临床样本的ROC曲线、HR值等数据,相关临床诊断与预后价值需进一步临床验证。
