1. 领域背景与文献引入
文献英文标题:C-reactive protein exerts angiogenic effects on vascular endothelial cells and modulates associated signalling pathways and gene expression;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:心血管病学(动脉粥样硬化与血管生物学)。
动脉粥样硬化是缺血性心脑血管疾病的病理基础,不稳定颈动脉粥样硬化斑块的血栓并发症是急性心肌梗死、脑卒中等临床事件的主要诱因。领域共识:斑块内新生血管形成是导致斑块不稳定的关键机制之一,新生血管为斑块内细胞提供氧和营养,但同时因其结构脆弱易发生破裂出血,引发斑块内血肿和破裂。C反应蛋白(CRP)是经典的急性时相反应蛋白,其循环水平升高是心血管事件的强独立预测因子,且研究显示CRP在血管壁尤其是动脉粥样硬化斑块的活性区域(如溃疡、出血区域)局部表达。然而,CRP对血管生成的直接作用存在争议,部分研究认为商业CRP制剂中的脂多糖(LPS)或叠氮钠污染导致了实验结果的假阳性,因此明确CRP本身对血管生成的作用及其机制是领域内未解决的核心问题。本研究旨在排除污染干扰,直接验证CRP的促血管生成作用,解析其下游信号通路和基因表达变化,为CRP在斑块不稳定中的作用提供实验依据。
2. 文献综述解析
作者对领域内现有研究的分类维度包括CRP作为心血管疾病生物标志物的研究、CRP对血管内皮细胞的功能影响研究,以及关于CRP制剂污染的争议性研究。
现有研究的关键结论显示,CRP是心血管事件的独立预测因子,循环CRP水平与动脉粥样硬化的进展和斑块不稳定密切相关;同时,CRP可诱导内皮细胞的促炎表型,包括吸引单核细胞、上调黏附分子、抑制一氧化氮释放等,这些效应被认为促进了动脉粥样硬化的发展。然而,关于CRP对血管生成的作用存在矛盾结论:部分研究显示CRP可上调内皮细胞中促血管生成分子如内皮素-1的表达,而另一些研究则报道CRP抑制内皮细胞增殖和管样结构形成,这些矛盾结论的核心争议点在于商业CRP制剂中的LPS或叠氮钠污染,有研究认为这些污染是导致实验结果差异的主要原因。现有研究的局限性在于未有效排除污染的影响,无法明确CRP本身的生物学效应。本研究的创新价值在于采用去污染的CRP(CRPdt),通过设置严格的污染对照(LPS、叠氮钠)和抗体阻断实验,直接证明CRP本身的促血管生成作用,同时系统解析其下游信号通路和基因表达变化,填补了领域内关于CRP直接调控血管生成机制的空白。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确CRP对血管内皮细胞的直接促血管生成作用,核心科学问题是CRP是否通过激活特定细胞信号通路和上调促血管生成基因来介导血管生成过程,技术路线遵循“体外细胞功能验证→体内模型验证→信号通路解析→基因表达筛选”的闭环逻辑,从细胞水平到整体动物水平,逐步解析CRP的促血管生成效应及其分子机制。
3.1 内皮细胞趋化性检测
实验目的是验证CRP对血管内皮细胞迁移能力的直接影响,迁移是血管生成的关键步骤之一。方法细节:采用人冠状动脉内皮细胞(HCAEC)和牛主动脉内皮细胞(BAEC)两种原代内皮细胞模型,使用改良Boyden小室法检测细胞趋化性,设置1-5μg/ml的天然CRP和经Detoxi-Gel柱处理的去污染CRP(CRPdt),以碱性成纤维细胞生长因子(FGF-2)为阳性对照,同时设置LPS(1ng/ml)作为污染对照,此外用抗CRP抗体(1:5)进行阻断实验以验证效应的特异性。结果解读:CRPdt在5μg/ml浓度时使HCAEC的迁移率达到对照组的290%(P<0.01),天然CRP在5μg/ml时使BAEC的迁移率达到对照组的175%(P<0.001),LPS处理组无显著迁移变化,抗CRP抗体可显著抑制CRPdt诱导的HCAEC迁移,说明CRP本身而非污染成分介导了内皮细胞的趋化效应。
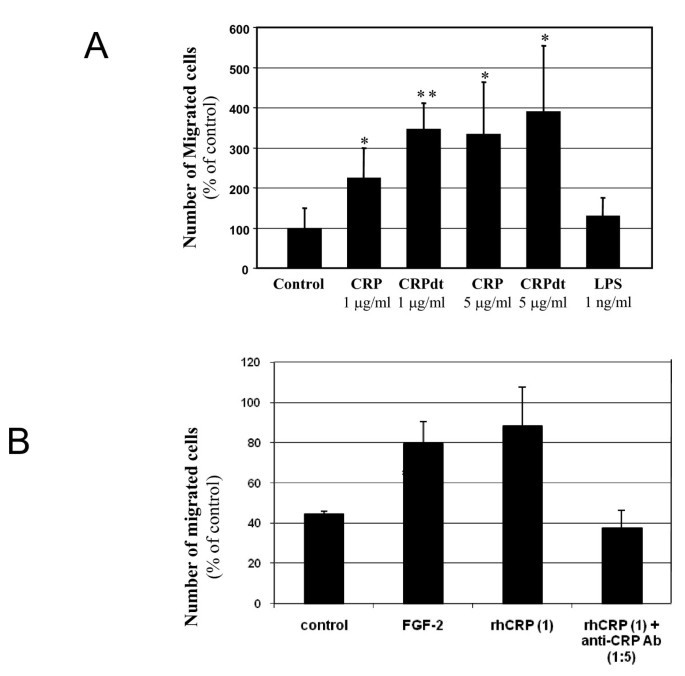
实验所用关键产品:人重组CRP购自Calbiochem,抗CRP抗体购自Sigma-Aldrich。
3.2 内皮细胞增殖检测
实验目的是检测CRP对不同来源血管内皮细胞增殖能力的影响,增殖是血管生成的核心环节。方法细节:将HCAEC接种于24孔板、BAEC接种于6孔板,待细胞贴壁后换用血清贫乏培养基(SPM)使细胞生长速率降低,随后加入1-5μg/ml的天然CRP或CRPdt,培养72小时后用胰酶消化细胞,使用Coulter计数器进行细胞计数。结果解读:1μg/ml天然CRP使BAEC的增殖率较对照组增加40%(P<0.05),CRPdt处理使BAEC增殖率进一步增加至对照组的180%(P<0.01),而在1-5μg/ml的浓度范围内,CRP对HCAEC的增殖无显著影响,说明CRP对不同来源内皮细胞的增殖调控存在细胞特异性。
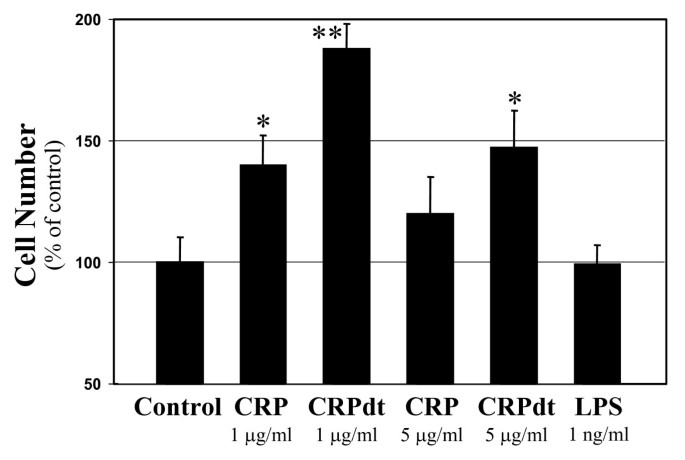
实验所用关键产品:细胞计数采用Coulter计数器。
3.3 管样结构形成检测
实验目的是验证CRP对内皮细胞体外血管形成能力的影响,管样结构形成是体外模拟血管生成的关键指标。方法细节:将HCAEC和BAEC与生长因子减少的Matrigel按1:1混合,加入1-5μg/ml的天然CRP或CRPdt,将混合物滴加至48孔板中形成3D凝胶滴,培养24-48小时后固定细胞,采用双盲法测量管样结构的总长度,同时设置抗CRP抗体阻断组和LPS对照组。结果解读:CRP处理使HCAEC的管样结构长度较对照组增加约4倍(P<0.01),CRPdt处理使BAEC的管样结构长度增加约3倍(P≤0.01),抗CRP抗体可显著抑制CRP诱导的管样结构形成,LPS处理组无显著变化,说明CRP可直接诱导内皮细胞形成功能性的管样结构。
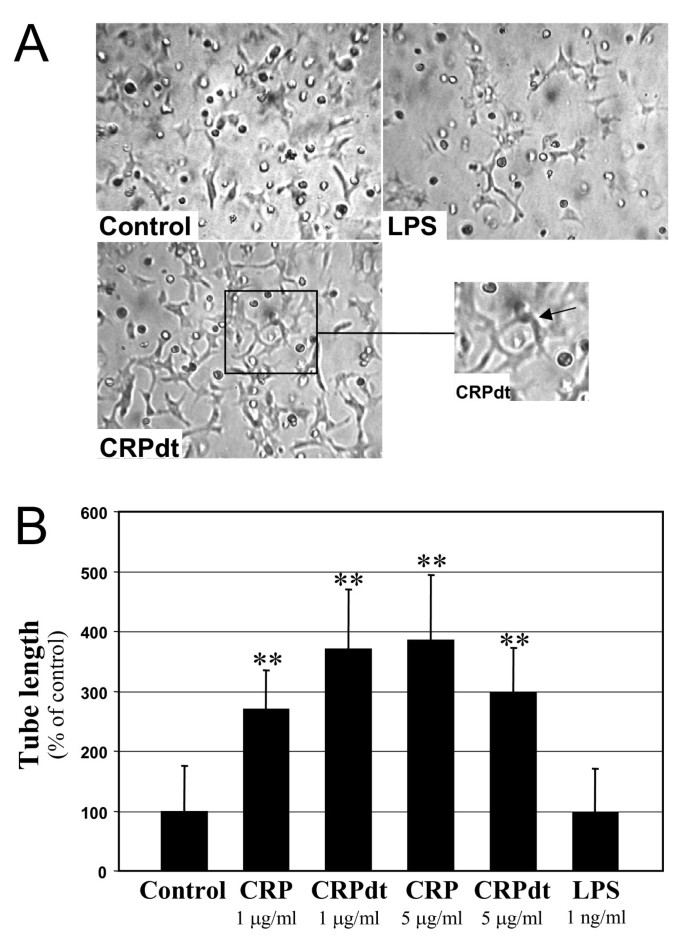
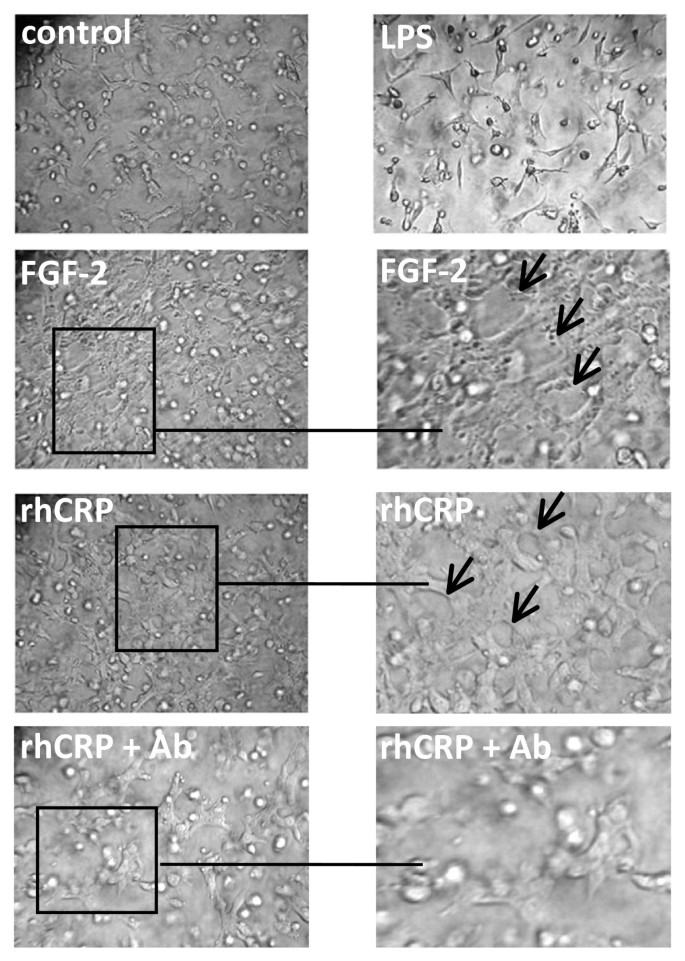
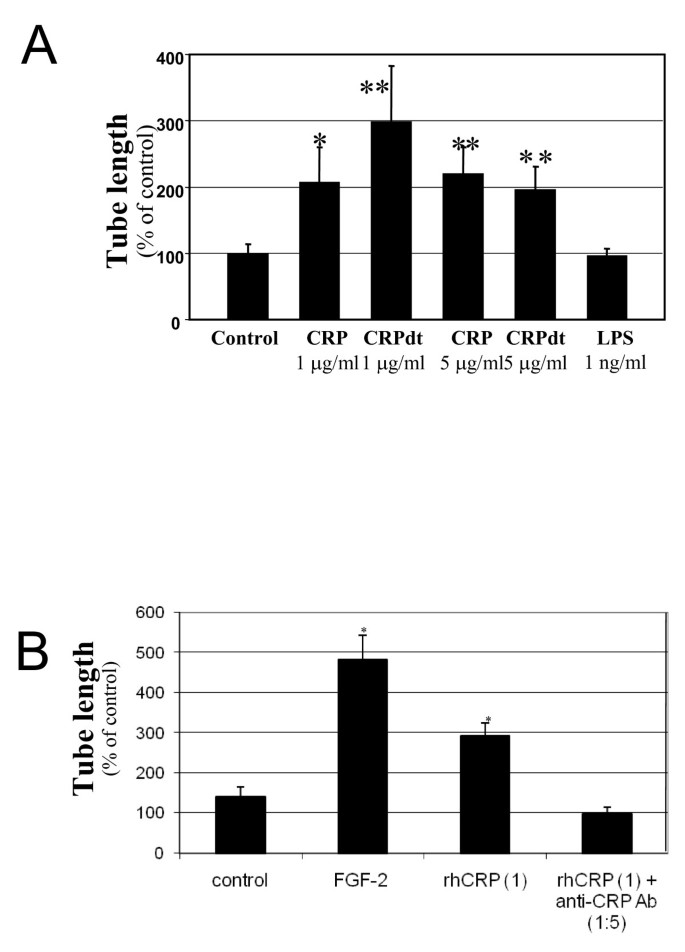
实验所用关键产品:生长因子减少的Matrigel购自BD Biosciences。
3.4 体内血管生成模型验证
实验目的是在整体动物水平验证CRP的促血管生成作用,体内模型更接近生理病理状态。方法细节:采用鸡胚绒毛尿囊膜(CAM)实验,将5μg CRPdt应用于第7天鸡胚的CAM,培养7天后按0-3分的标准评分血管生成情况;同时采用大鼠主动脉环实验,将成年Wistar大鼠的主动脉切成1mm厚的环,接种于Matrigel上,加入1μg/ml CRPdt培养6天,测量微管出芽的面积。结果解读:CRPdt处理的CAM血管生成评分为2.0(对照组为0.5,P<0.001),形成典型的轮辐状血管结构;CRPdt处理使大鼠主动脉环的微管出芽面积从对照组的2.3±0.3增加到10.5±0.8(P<0.01),与FGF-2的效应相当,说明CRP在体内具有显著的促血管生成活性。
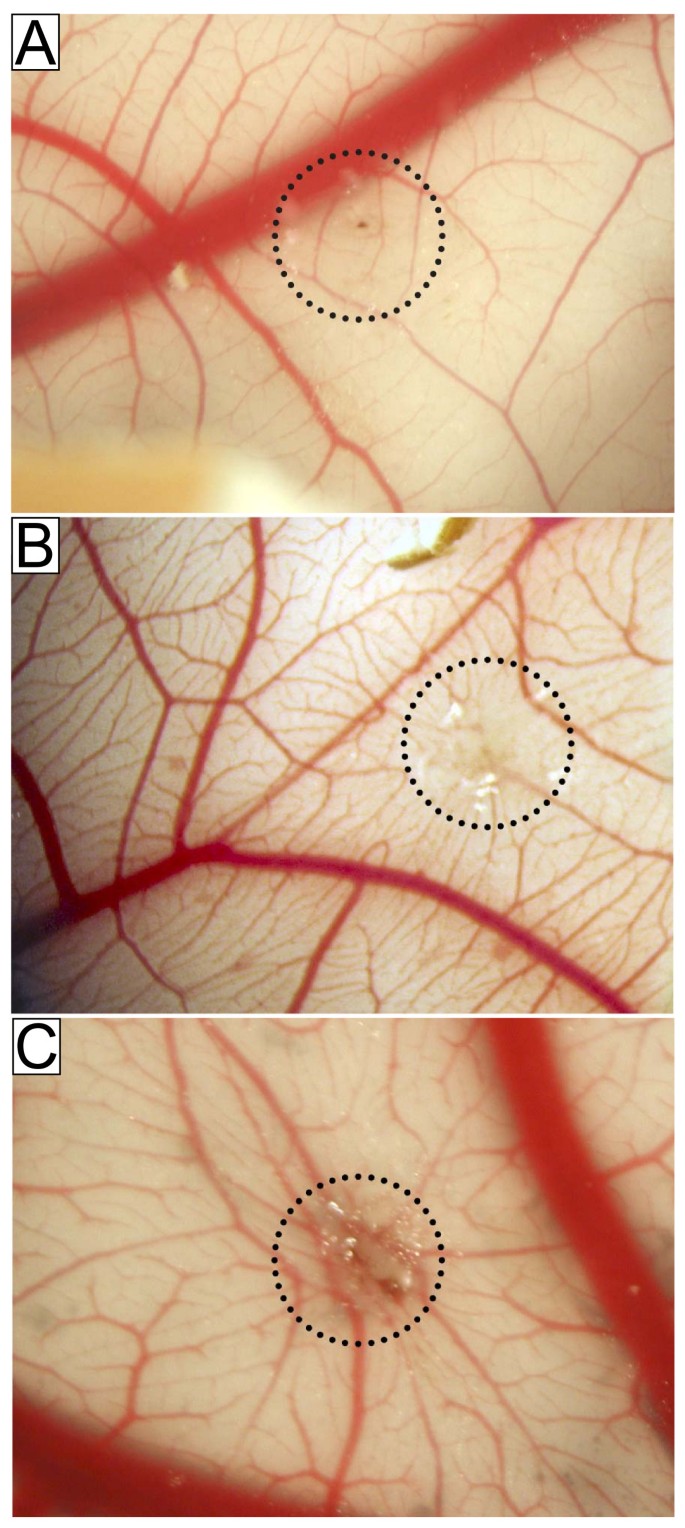
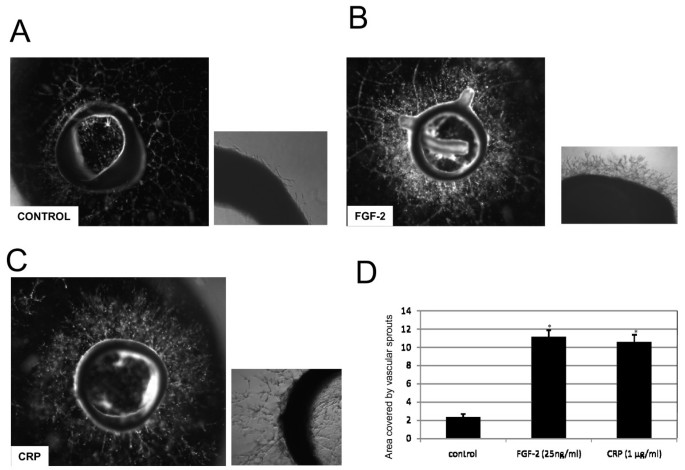
3.5 3D Matrigel侵袭实验
实验目的是检测CRP对内皮细胞侵袭能力的影响,侵袭是内皮细胞形成新生血管的关键步骤之一。方法细节:先让HCAEC在FGF-2存在下于Matrigel中形成管样结构,然后在其周围加入第二层Matrigel并加入1μg/ml CRPdt,培养24小时后观察细胞向第二层Matrigel的侵袭情况。结果解读:对照组HCAEC的侵袭水平较低,而CRPdt处理组可见明显的细胞侵袭进入第二层Matrigel,说明CRP可促进内皮细胞的侵袭能力,进一步支持其促血管生成作用。
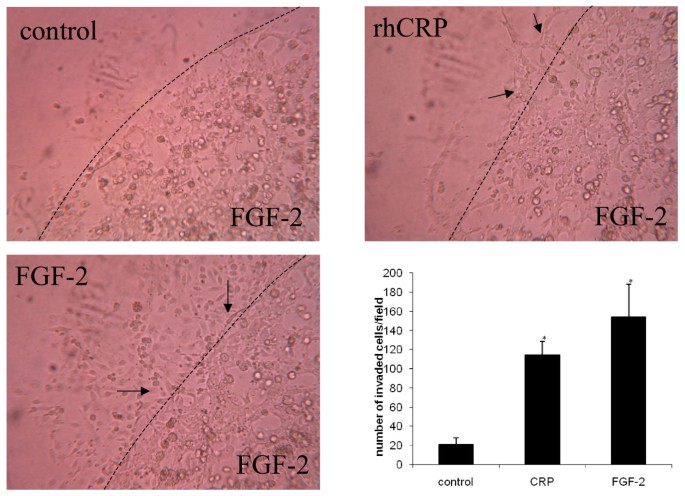
3.6 ERK1/2信号通路检测
实验目的是解析CRP促血管生成的下游细胞信号通路,ERK1/2是调控内皮细胞增殖和迁移的关键信号分子。方法细节:HCAEC和BAEC经血清饥饿48小时后,用1-5μg/ml的天然CRP或CRPdt处理8分钟,采用免疫印迹法检测ERK1/2的磷酸化水平,以总ERK1/2作为内参。结果解读:CRP和CRPdt均显著增加ERK1/2的磷酸化水平,与FGF-2的效应相似,LPS和叠氮钠处理组无显著变化,说明CRP通过激活ERK1/2信号通路介导其促血管生成效应。
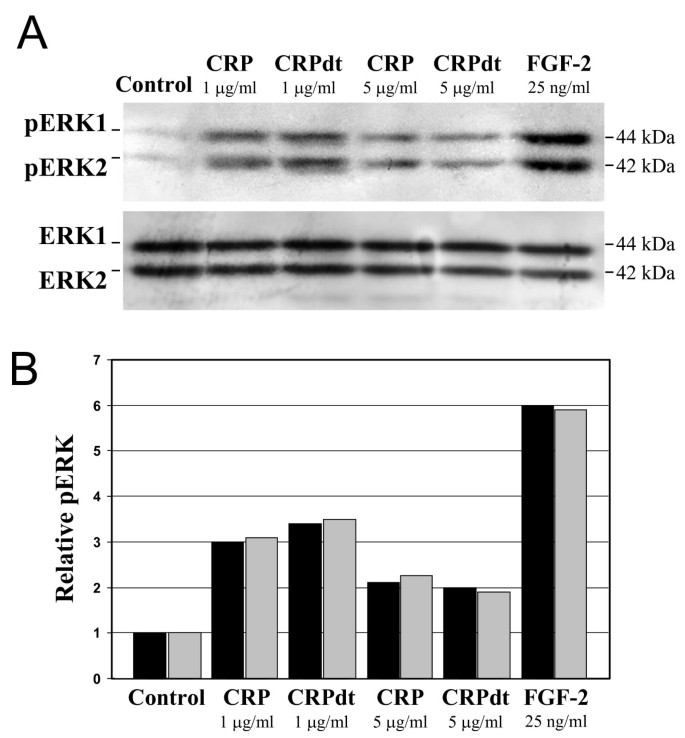
实验所用关键产品:ERK1/2和磷酸化ERK1/2抗体购自Santa Cruz Biotechnology。
3.7 促血管生成基因表达分析
实验目的是筛选CRP上调的促血管生成相关基因,从转录水平解析CRP的促血管生成机制。方法细节:HCAEC经5μg/ml CRP处理4-72小时后提取总RNA,采用TaqMan低密度芯片检测血管生成相关基因的表达水平,筛选在两次独立实验中均上调超过1.5倍的基因。结果解读:共筛选出6个显著上调的促血管生成基因,包括血管内皮生长因子受体2(VEGFR2/KDR)、血小板衍生生长因子BB(PDGF-BB)、Notch1、Notch3、富含半胱氨酸的血管生成诱导因子61(CYR61/CCN1)和DNA结合/分化抑制因子1(ID1),这些基因分别参与血管生成的信号传导、细胞增殖、血管发育调控等过程,说明CRP通过上调多个关键促血管生成基因的表达来促进血管生成。
4. Biomarker研究及发现成果
本研究中CRP既是心血管疾病的经典生物标志物,也是直接的促血管生成功能介质,其筛选与验证逻辑基于CRP在不稳定动脉粥样硬化斑块中的高表达,通过去污染实验排除干扰,从细胞到整体水平验证其促血管生成作用,再解析其分子机制。
Biomarker定位:CRP属于循环蛋白类Biomarker,本研究的验证逻辑为“临床样本关联→体外细胞功能验证→体内模型验证→分子机制解析”,首先基于前期研究中CRP在不稳定斑块中的高表达,提出CRP可能参与血管生成的假设,然后通过去污染的CRP排除干扰,验证其直接的促血管生成效应,最后解析其下游信号通路和基因表达变化。研究过程详述:CRP的来源为商业重组人CRP,经Detoxi-Gel柱处理去除LPS和叠氮钠污染;验证方法包括体外内皮细胞迁移、增殖、管形成实验,体内CAM和主动脉环实验,信号通路检测和基因表达分析;特异性方面,抗CRP抗体可完全阻断CRP的促血管生成效应,LPS和叠氮钠无类似效应,说明效应由CRP本身介导;敏感性方面,在1-5μg/ml的浓度范围(对应心血管事件中危/高危患者的循环CRP水平)即可产生显著的促血管生成效应。核心成果提炼:CRP不仅是心血管疾病的预测生物标志物,更是直接的促血管生成介质,可通过激活ERK1/2信号通路,上调VEGFR2、Notch家族等关键促血管生成基因的表达,诱导内皮细胞的迁移、增殖、管形成和体内血管生成;其创新性在于首次在严格排除污染的情况下明确了CRP本身的促血管生成作用,为CRP在动脉粥样硬化斑块不稳定中的病理作用提供了直接实验证据;各实验结果均具有显著的统计学意义(如P<0.01、P<0.001),样本量为至少3次独立重复实验,数据可靠性高。
