1. 领域背景与文献引入
文献英文标题:cAMP-dependent and cholinergic regulation of the electrogenic intestinal/pancreatic Na⁺/HCO₃⁻ cotransporter pNBC1 in human embryonic kidney (HEK293) cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(离子转运蛋白调控)
领域共识:Na⁺/HCO₃⁻共转运蛋白1(NBC1)是介导细胞内外HCO₃⁻转运的关键离子转运蛋白,分为肾型(kNBC1)和肠胰型(pNBC1)两个亚型,二者在结构、转运方向及对分泌素的响应上存在显著差异。早期研究认为,pNBC1独特的N端磷酸化位点是其与kNBC1调控差异的核心原因,例如环腺苷酸(cAMP)对kNBC1具有抑制作用,而对天然肠组织中的pNBC1具有激活作用。但近年来的研究显示,细胞类型对离子转运蛋白的调控具有重要影响,这一现象已在Na⁺/H⁺交换蛋白、阴离子交换蛋白等多种转运蛋白中被证实,但pNBC1在异源表达体系中的分泌素调控是否依赖细胞类型,以及结构与细胞类型的相对调控作用尚未明确,这一研究空白限制了对NBC1亚型调控机制的全面理解。本研究旨在通过在人胚肾(HEK293)细胞中异源表达pNBC1,模拟其生理功能(酸负荷下的HCO₃⁻摄取),研究cAMP和胆碱能通路对其的调控作用,明确细胞类型在pNBC1调控中的作用。
2. 文献综述解析
作者将现有研究分为两类核心方向,一类是基于NBC1亚型结构差异的调控机制研究,另一类是细胞类型对离子转运调控的影响研究。基于结构差异的研究表明,pNBC1的N端存在独特的蛋白激酶A(PKA)、蛋白激酶C(PKC)和酪蛋白激酶II磷酸化位点,而kNBC1缺乏这些位点,这一结构差异被认为是cAMP对二者调控差异的原因;同时,cAMP可通过调控C端共同磷酸化位点改变转运化学计量比,进而影响转运方向。基于细胞类型的研究则显示,多种离子转运蛋白的调控模式具有细胞特异性,这与细胞内的信号转导机制、辅助蛋白表达等因素相关,但针对pNBC1的相关研究较为匮乏,仅有的研究未模拟其生理功能状态下的调控。现有研究的局限性在于,缺乏pNBC1在异源表达体系中模拟生理HCO₃⁻摄取功能时的分泌素调控研究,无法明确结构与细胞类型在pNBC1调控中的相对作用。本研究的创新价值在于,首次在非肠上皮细胞系中异源表达pNBC1,研究其在酸负荷下的功能及分泌素调控,直接对比天然肠组织中的调控模式,明确细胞类型对pNBC1调控的关键影响,弥补了现有研究的空白。
3. 研究思路总结与详细解析
本研究的核心目标是明确pNBC1的分泌素调控是否依赖细胞类型,核心科学问题是异源表达的pNBC1在酸负荷下的HCO₃⁻摄取功能及分泌素调控模式与天然肠组织是否一致,技术路线遵循“载体构建→异源表达→功能验证→调控机制研究→结论”的闭环逻辑。
3.1 表达载体构建与细胞转染
实验目的是构建可可视化追踪的pNBC1表达载体,并在HEK293细胞中实现功能性异源表达。方法细节为通过聚合酶链反应(PCR)扩增人pNBC1全长cDNA,将其克隆至N端融合绿色荧光蛋白(GFP)的表达载体pcDNA3.1/NT-GFP-TOPO中,采用磷酸钙法或Lipofectamine 2000转染试剂将重组载体转染至HEK293细胞,转染后48-72小时进行后续实验。结果解读为成功构建GFP标记的pNBC1重组载体,共聚焦显微镜观察显示转染效率为10%-15%,GFP信号定位于细胞膜,符合pNBC1的亚细胞定位特征。实验所用关键产品:Invitrogen的pcDNA3.1/NT-GFP-TOPO载体、Lipofectamine 2000转染试剂,Sigma-Aldrich的福斯高林、卡巴胆碱等。
3.2 亚型表达验证
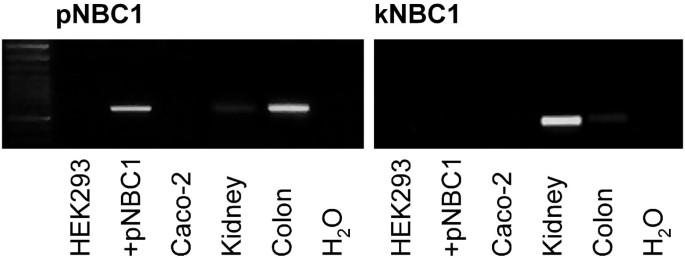
实验目的是确认HEK293细胞内源性NBC1亚型的表达情况,以及转染后pNBC1的特异性表达。方法细节为提取未转染HEK293细胞、转染pNBC1的HEK293细胞、人肾组织和人结肠组织的RNA,采用kNBC1和pNBC1特异性引物进行聚合酶链反应(PCR),检测各样本中NBC1亚型的表达。结果解读为未转染HEK293细胞中未检测到kNBC1和pNBC1的表达,转染pNBC1的HEK293细胞和人结肠组织中可检测到pNBC1的特异性条带,人肾组织中可检测到kNBC1的条带,说明HEK293细胞无内源性NBC1表达,适合作为异源表达体系。
3.3 细胞定位与pH校准体系建立
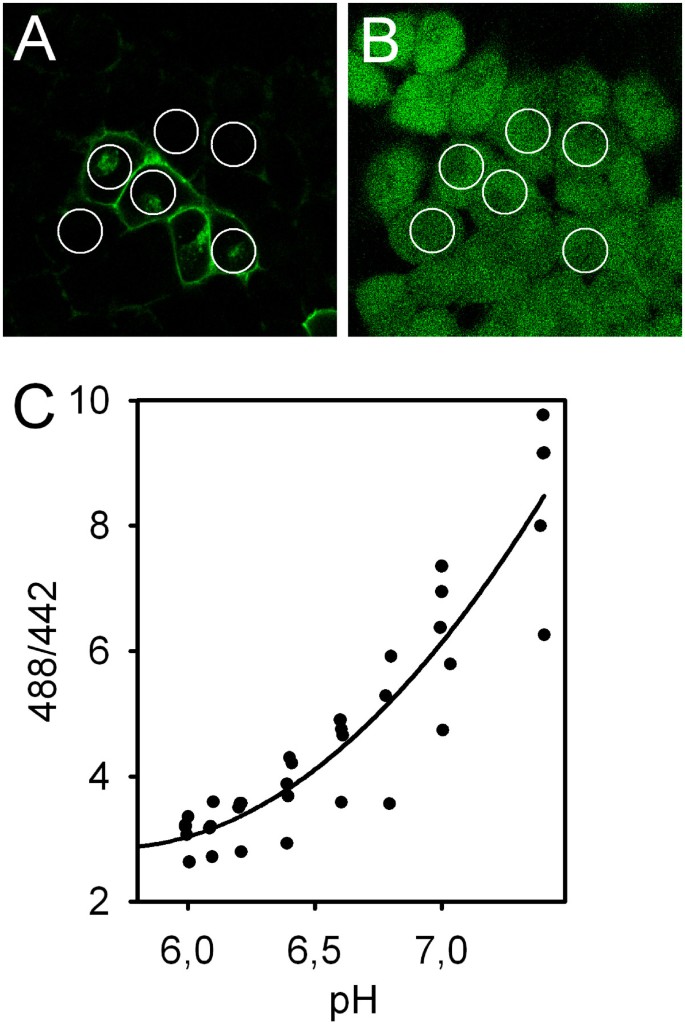
实验目的是明确pNBC1在HEK293细胞中的亚细胞定位,并建立适合检测酸负荷后细胞内pH(pHᵢ)恢复的校准体系。方法细节为采用共聚焦显微镜观察转染细胞的GFP荧光信号,定位pNBC1的表达位置;使用pH敏感染料BCECF负载细胞,通过高K⁺/尼日利亚菌素溶液将细胞内pH钳制在不同水平,构建pH校准曲线。结果解读为pNBC1定位于HEK293细胞的细胞膜上,pH校准曲线在pH6.2-7.0区间斜率稳定,适合检测酸负荷后的pHᵢ恢复率,该区间与pNBC1发挥HCO₃⁻摄取功能的生理pH范围一致。
3.4 酸负荷下pNBC1的功能验证
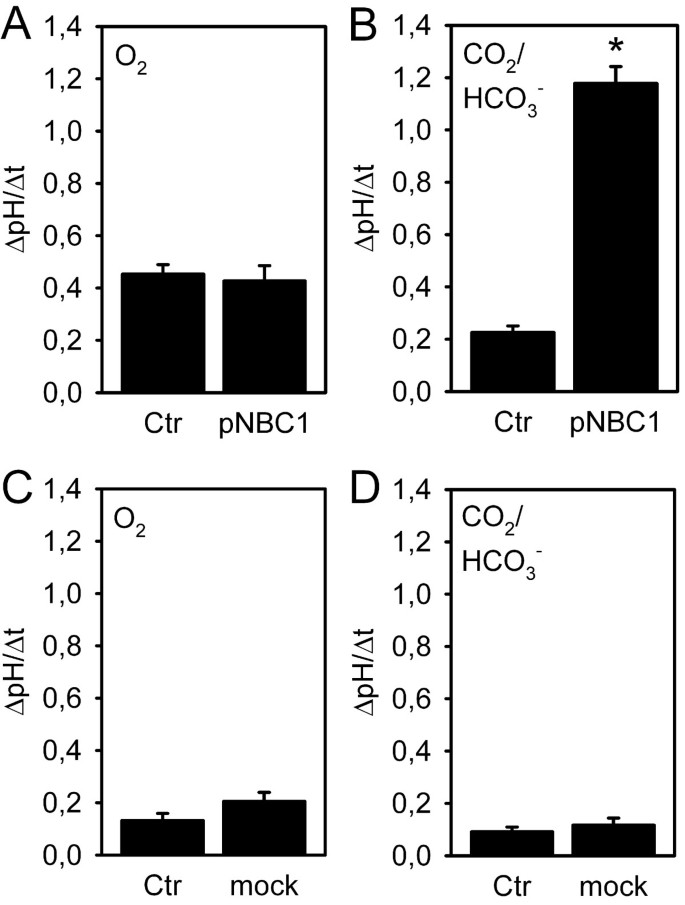
实验目的是确认转染pNBC1的HEK293细胞是否具有功能性的HCO₃⁻摄取能力。方法细节为采用NH₄⁺预脉冲法对细胞施加酸负荷,在有无CO₂/HCO₃⁻的条件下,检测重新加入Na⁺后的pHᵢ恢复率,对比转染细胞与未转染细胞的差异。结果解读为在无CO₂/HCO₃⁻的HEPES缓冲液中,转染细胞与未转染细胞的pHᵢ恢复率无显著差异;而在存在CO₂/HCO₃⁻的条件下,转染细胞的pHᵢ恢复率是未转染细胞的5倍(n=7,P<0.05),且稳态pHᵢ显著偏碱性(n=7,P<0.001),说明pNBC1在HEK293细胞中具有功能性的HCO₃⁻摄取能力。

3.5 分泌素对pNBC1的调控作用研究
实验目的是研究cAMP和胆碱能通路对异源表达pNBC1的调控作用,对比天然肠组织中的调控模式。方法细节为分别用10⁻⁵M福斯高林(cAMP激活剂)和10⁻⁴M卡巴胆碱(胆碱能激动剂)处理细胞,采用NH₄⁺预脉冲法检测酸负荷后的pHᵢ恢复率,对比处理组与对照组的差异。结果解读为福斯高林对未转染HEK293细胞的pHᵢ恢复率无显著影响,但可使转染细胞的pHᵢ恢复率降低62%以上(n=7,P<0.01),这与天然肠组织中cAMP激活pNBC1的结果相反;卡巴胆碱可使未转染细胞的pHᵢ恢复率显著升高(n=6,P<0.05),但对转染细胞的pHᵢ恢复率无显著影响,同样与天然肠组织中卡巴胆碱激活pNBC1的结果不同。

4. Biomarker研究及发现成果解析
Biomarker定位:本研究中pNBC1作为离子转运功能的调控靶点,其筛选/验证逻辑为通过异源表达体系验证其功能及调控模式的细胞依赖性,明确细胞类型在pNBC1调控中的作用。研究过程详述:pNBC1的来源为克隆的人胰腺NBC1 cDNA,验证方法包括聚合酶链反应(PCR)表达验证、共聚焦显微镜亚细胞定位、酸负荷pHᵢ恢复实验、分泌素处理后的功能检测;特异性方面,转染pNBC1的HEK293细胞在CO₂/HCO₃⁻存在下的pHᵢ恢复率显著高于未转染细胞(n=7,P<0.05),具有明确的功能特异性;敏感性方面,福斯高林处理可显著抑制转染细胞的pHᵢ恢复率(n=7,P<0.01),显示出对cAMP调控的敏感性。核心成果提炼:本研究首次证实pNBC1的分泌素调控不仅依赖自身的结构特征,还显著依赖其所在的细胞类型,打破了之前仅基于结构差异解释NBC1亚型调控差异的认知;统计学结果显示,稳态pHᵢ在转染细胞与未转染细胞间的差异具有高度显著性(n=7,P<0.001),福斯高林对转染细胞的抑制作用也具有统计学意义(n=7,P<0.01)。该成果为离子转运蛋白的调控机制研究提供了新的视角,提示细胞内的信号转导网络、辅助蛋白等因素在pNBC1调控中具有重要作用,为进一步研究pNBC1的调控机制奠定了基础。
