1. 领域背景与文献引入
文献英文标题:A novel class of copper(II)- and zinc(II)-bound non-steroidal anti-inflammatory drugs that inhibits acute inflammation in vivo;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:炎症药理学与心血管炎症治疗
非甾体抗炎药(NSAIDs)是全球临床应用最广泛的抗炎药物之一,可用于多种炎症性疾病的治疗,但传统非选择性NSAIDs常引发胃肠道溃疡、出血等严重不良反应。20世纪90年代选择性环氧合酶-2(COX-2)抑制剂的出现曾被认为能降低胃肠道毒性,但后续研究证实这类药物会显著增加心血管事件风险,如心肌梗死、中风等,临床应用受到严格限制。为解决这一困境,研究人员尝试通过药物结构修饰或金属络合等方式开发更安全的抗炎药物,其中金属(尤其是铜、锌)与NSAIDs的络合物在兽医领域已显示出胃肠道保护优势,阿西美辛作为吲哚美辛的前体药物,本身也具有更好的胃肠道耐受性,但这类金属结合NSAIDs在心血管炎症中的治疗效果尚未在体内模型中得到验证。基于这一研究空白,本文旨在探讨铜(II)-吲哚美辛、铜(II)-阿西美辛、锌(II)-阿西美辛在体内急性血管炎症模型中的抗炎活性及安全性,为开发新型安全抗炎药物提供实验依据。
2. 文献综述解析
作者对领域内现有研究按药物类型及局限性进行分类评述,首先梳理了传统NSAIDs的临床应用现状与胃肠道毒性问题,指出其通过抑制COX-1导致胃肠道黏膜保护机制受损;随后分析选择性COX-2抑制剂的研发背景与心血管风险,说明这类药物因抑制血管内皮前列腺素合成,破坏了心血管系统的稳态平衡;接着介绍了金属结合NSAIDs的前期研究进展,提到20世纪中期已有铜-水杨酸盐复合物用于风湿性疾病治疗,后续研究证实铜结合NSAIDs具有超氧化物歧化酶(SOD)样活性,可减少氧化应激损伤,且在动物模型中显示出更低的胃肠道毒性;最后阐述了阿西美辛的药理学优势,其作为吲哚美辛的前体药物,体内代谢后释放活性成分,同时具有更好的老年患者药代动力学特性。
现有研究已证实传统NSAIDs和选择性COX-2抑制剂均存在严重的器官毒性,金属结合NSAIDs虽在胃肠道保护方面显示出潜力,但相关研究多集中于基础抗炎活性或胃肠道毒性评估,缺乏在心血管炎症模型中的验证数据,且不同金属结合NSAIDs的作用靶点差异尚未明确。本文的创新价值在于首次在体内急性血管炎症模型中系统比较了铜、锌结合NSAIDs的抗炎效果,明确了不同金属络合物对血管内皮黏附分子的特异性抑制作用,同时证实这类药物无明显胃肠道、肝、肾毒性,为其临床转化应用提供了关键的“概念验证”数据。
3. 研究思路总结与详细解析
本研究的核心目标是验证铜、锌结合NSAIDs在体内急性血管炎症模型中的抗炎活性与安全性,核心科学问题为这类金属络合物是否能有效抑制血管内皮炎症相关黏附分子表达,且避免传统NSAIDs的器官毒性,技术路线遵循“模型构建→药物干预→指标检测→结果分析”的闭环逻辑,通过体内动物实验完成验证。
3.1 急性血管炎症动物模型构建与实验分组
实验目的是构建稳定的体内急性血管炎症模型,并设置不同药物处理组以对比抗炎效果。方法细节为选用血脂正常的新西兰白兔,通过手术在左侧颈总动脉周围放置非闭塞性硅胶环诱导急性血管炎症,每组纳入4只动物,分别经剖腹手术给予生理盐水(阳性对照)、吲哚美辛(3mg/kg)、铜(II)-吲哚美辛(3mg/kg)、铜(II)-阿西美辛(3mg/kg)、锌(II)-阿西美辛(3mg/kg)单次口服给药,右侧未套环颈总动脉作为自身对照,24小时后处死动物并采集血管组织。结果解读显示,硅胶环植入成功诱导血管内皮血管细胞黏附分子-1(VCAM-1)和细胞间黏附分子-1(ICAM-1)表达显著上调(P<0.01),模型构建成功。实验所用关键产品:Sigma的阿西美辛、吲哚美辛、乙酸锌二水合物,Ajax的乙酸铜一水合物。
3.2 血管内皮黏附分子表达的定量检测
实验目的是评估不同药物处理对血管内皮炎症标志物表达的影响。方法细节为将采集的颈动脉组织制作石蜡切片,采用免疫组化染色法检测VCAM-1和ICAM-1的表达,使用ImagePro Plus 4.5软件对染色结果进行定量分析,以图像单位表示阳性染色强度,每组样本分析8-10个连续切片,每个切片选取20个随机视野,由盲法病理学家设定染色阈值。结果解读显示,铜(II)-吲哚美辛处理使VCAM-1表达降低67%(8.2±1.7 vs 2.7±0.4图像单位,n=4,P<0.05),铜(II)-阿西美辛处理使VCAM-1表达降低88%(8.2±1.7 vs 1.0±0.5图像单位,n=4,P<0.01),锌(II)-阿西美辛处理使ICAM-1表达降低84%(19.3±1.0 vs 3.1±1.2图像单位,n=4,P<0.01),而吲哚美辛对两种黏附分子均有显著抑制作用。
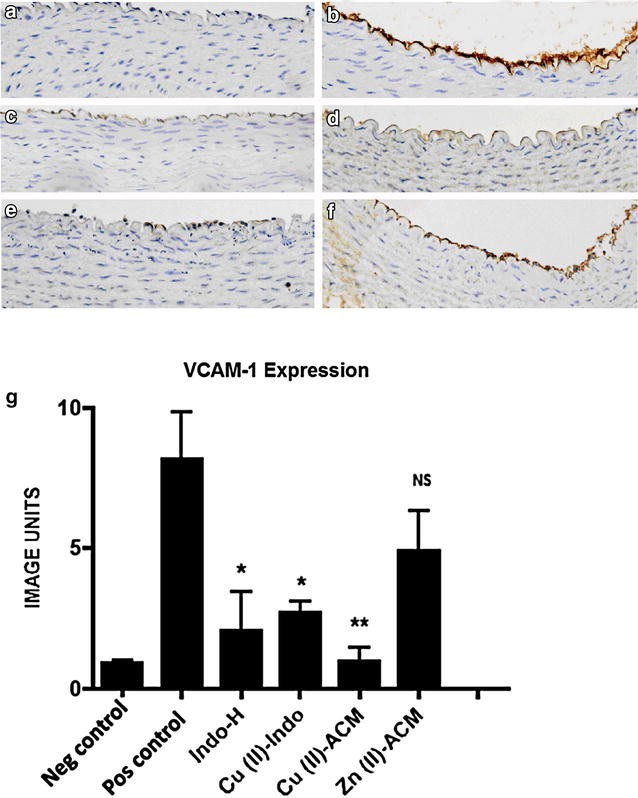
图1 不同处理对血管内皮VCAM-1表达的影响
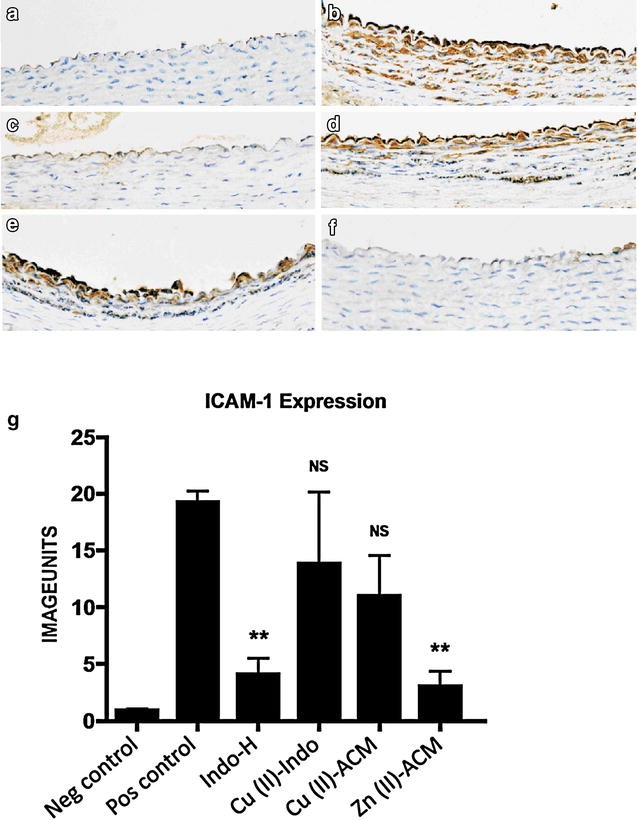
图2 不同处理对血管内皮ICAM-1表达的影响
实验所用关键产品:多伦多大学Dr M. Cybulsky捐赠的抗兔VCAM-1和ICAM-1抗体,ImagePro Plus 4.5软件(Media Cybernetics)。
3.3 药物急性毒性与血脂参数评估
实验目的是检测不同药物处理对动物器官毒性及血脂代谢的影响。方法细节为处死动物前采集血浆样本,采用Roche诊断试剂盒检测总胆固醇、高密度脂蛋白(HDL)胆固醇水平,通过免疫比浊法检测载脂蛋白A-I(apoA-I)浓度;同时对胃、肝、肾进行宏观和微观组织学检查,评估是否存在炎症、溃疡或坏死等毒性表现。结果解读显示,所有药物处理组的血浆总胆固醇、HDL胆固醇、apoA-I浓度与对照组相比无显著差异,宏观和组织学检查未发现胃肠道溃疡、肝炎或肾炎等毒性迹象,证实3mg/kg剂量下的金属结合NSAIDs无急性器官毒性。
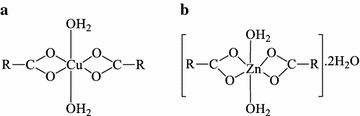
图3 阿西美辛及金属络合物的化学结构
实验所用关键产品:Roche的胆固醇检测试剂盒,免疫比浊法检测载脂蛋白A-I的相关试剂。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker为血管内皮表面的黏附分子VCAM-1和ICAM-1,属于炎症状态下的功能型Biomarker,其筛选与验证逻辑为:首先通过体内急性炎症模型诱导Biomarker表达上调,然后检测不同药物处理对其表达的抑制效果,最后结合毒性数据评估Biomarker抑制与药物安全性的关联。
Biomarker的来源为新西兰白兔颈总动脉内皮细胞,验证方法采用免疫组化染色结合图像定量分析,其中VCAM-1的特异性抑制数据显示,铜(II)-阿西美辛处理组的表达水平较对照组降低88%(n=4,P<0.01),铜(II)-吲哚美辛处理组降低67%(n=4,P<0.05);ICAM-1的特异性抑制数据显示,锌(II)-阿西美辛处理组的表达水平较对照组降低84%(n=4,P<0.01),而铜结合药物对ICAM-1的抑制作用无统计学意义。
核心成果方面,本研究首次证实铜结合NSAIDs主要通过抑制VCAM-1表达发挥抗炎作用,而锌结合阿西美辛可特异性抑制ICAM-1表达,提示其可能通过非经典核因子-κB(NF-κB)通路发挥抗炎活性;同时,这类金属结合NSAIDs在有效抑制炎症Biomarker表达的同时,无明显胃肠道、肝、肾毒性,其抗炎活性与等效剂量的吲哚美辛相当,但安全性显著提升。研究还指出,VCAM-1和ICAM-1作为心血管炎症的早期标志物,其表达水平与动脉粥样硬化进展密切相关,因此这类金属结合NSAIDs有望成为急性和慢性心血管炎症的潜在治疗药物,后续需扩大样本量并开展机制研究以明确其作用通路。
