1. 领域背景与文献引入
文献英文标题:The roles of lncRNA in hepatic fibrosis;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:肝脏纤维化的长链非编码RNA(lncRNA)调控机制。
领域共识:肝纤维化是慢性肝病进展至肝硬化、肝癌的关键中间阶段,全球每年因肝癌死亡的病例中约半数由肝纤维化进展而来。2000年左右的研究明确,肝星状细胞(HSC)从静息态向肌成纤维细胞样细胞的活化是肝纤维化进程中细胞外基质(ECM)过度沉积的核心节点。2010年后,表观遗传调控成为肝纤维化研究的热点方向,尤其是长链非编码RNA(lncRNA)的调控作用逐渐受到关注,但截至2018年,领域内对lncRNA在肝纤维化中的具体调控机制、功能方向尚未形成系统总结,不同研究结果分散且缺乏机制分类整合,导致临床转化应用的理论框架不清晰。本综述旨在系统梳理lncRNA在肝纤维化中的三类核心调控机制(TGF-β信号通路调控、DNA甲基化关联调控、竞争性内源性RNA(ceRNA)作用模式),为后续的分子靶向治疗研究提供系统性理论基础。
2. 文献综述解析
本综述以lncRNA的调控机制为核心分类维度,将现有研究分为TGF-β信号通路调控、DNA甲基化关联调控、ceRNA作用模式三类,系统总结了不同lncRNA在肝星状细胞(HSC)活化中的功能。
现有研究已证实,TGF-β信号通路是促进HSC活化的核心通路,部分lncRNA可通过直接或间接调控该通路的关键分子(如Smad3)影响纤维化进程;DNA甲基化作为经典的表观遗传修饰,可通过沉默抑纤维化lncRNA的表达促进HSC活化;ceRNA模式则通过lncRNA吸附微小RNA(miRNA),解除miRNA对靶基因的抑制作用,从而调控HSC活化。现有研究的优势在于明确了单个lncRNA的具体功能机制,为纤维化调控提供了潜在靶点,但局限性在于缺乏对不同调控机制之间交叉作用的研究,且多数研究停留在细胞或动物模型层面,临床转化证据不足。本综述的创新价值在于首次系统整合了三类调控机制下的lncRNA功能图谱,明确了不同lncRNA对HSC活化的双向调控作用(促进或抑制),填补了领域内对lncRNA调控肝纤维化的系统性总结空白,为后续的机制交叉研究和临床转化提供了清晰的方向。
3. 研究思路总结与详细解析
本综述的研究目标是系统总结长链非编码RNA(lncRNA)在肝纤维化中的调控机制,核心科学问题是明确不同lncRNA通过何种分子通路影响肝星状细胞(HSC)的活化,技术路线为“分类整合已发表研究→解析每类机制下lncRNA的具体功能→总结双向调控模式及临床应用潜力”。
3.1 TGF-β信号通路相关lncRNA调控
实验目的:总结通过转化生长因子-β(TGF-β)信号通路调控肝星状细胞(HSC)活化的lncRNA功能及具体机制。
方法细节:整合已发表的细胞实验、动物模型及临床样本研究结果,分析lncRNA与TGF-β通路关键分子的相互作用。
结果解读:研究发现,转移相关肺腺癌转录本1(MALAT1)可通过沉默沉默信息调节因子1(SIRT1)的表达,抑制SIRT1对Smad3的去乙酰化作用,增强Smad3与纤维化基因启动子的结合能力,从而促进HSC活化;肝纤维化相关lncRNA1(lnc-LFAR1)则通过与Smad2/3形成正反馈回路,上调Smad2/3的表达及磷酸化水平,进一步增强TGF-β通路的活化,促进ECM沉积。对应文献机制图清晰展示了两类lncRNA的调控逻辑:
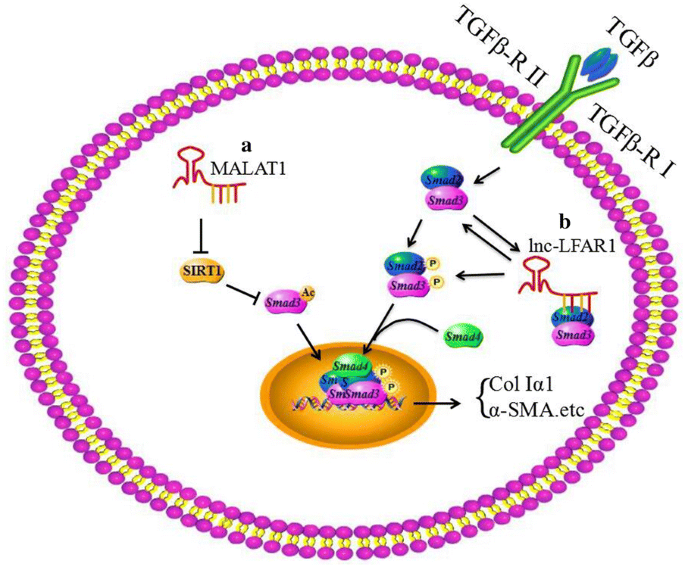
产品关联:文献未提及具体实验产品,领域常规使用RNA测序、荧光定量PCR、免疫印迹(WB)、免疫组化(IHC)等试剂/仪器。
3.2 DNA甲基化关联lncRNA调控
实验目的:总结与DNA甲基化修饰相关的lncRNA在肝星状细胞(HSC)活化中的抑制作用及机制。
方法细节:整合已发表的表观遗传修饰研究,分析DNA甲基转移酶(DNMT)、Ten-eleven易位甲基胞嘧啶双加氧酶(TET)与lncRNA的相互作用对HSC活化的影响。
结果解读:母系表达基因3(MEG3)的表达受DNMT1介导的启动子高甲基化抑制,而MEG3可通过激活p53通路诱导活化HSC的凋亡,降低Ⅰ型胶原(colIα1)和α-平滑肌肌动蛋白(α-SMA)的表达;HIF1α反义RNA1(HIF1A-AS1)则与TET3相互作用,TET3可通过下调HIF1A-AS1的表达促进HSC活化,反之HIF1A-AS1的上调可抑制HSC活化。对应文献机制图展示了DNA甲基化循环与lncRNA的调控关系:
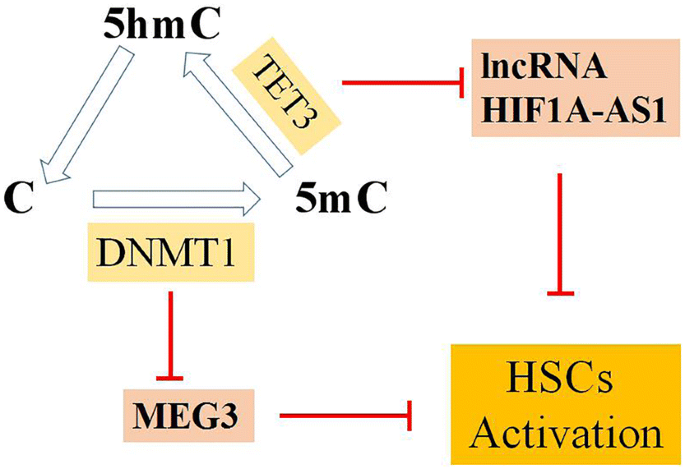
产品关联:文献未提及具体实验产品,领域常规使用甲基化特异性PCR(MSP)、染色质免疫共沉淀(ChIP)等试剂/仪器。
3.3 ceRNA模式下lncRNA调控
实验目的:总结以竞争性内源性RNA(ceRNA)模式调控肝星状细胞(HSC)活化的lncRNA功能及作用机制。
方法细节:整合已发表的miRNA靶标验证研究,分析lncRNA作为miRNA海绵对靶基因表达的调控作用。
结果解读:长基因间非编码RNA-p21(lncRNA-p21)可通过吸附miR-181b和miR-17-5p,分别上调PTEN和WIF1的表达,抑制PI3K/Akt和Wnt/β-catenin通路,从而抑制HSC活化;生长停滞特异性转录本5(GAS5)则通过吸附miR-222上调p27的表达,抑制HSC增殖;而MALAT1、浆细胞瘤变体易位1(PVT1)、同源盒转录反义RNA(HOTAIR)则通过吸附miR-101b、miR-152、miR-29b,分别上调Rac1、PTCH1、PTEN甲基化水平,促进HSC活化。对应文献机制图展示了ceRNA模式下的双向调控:
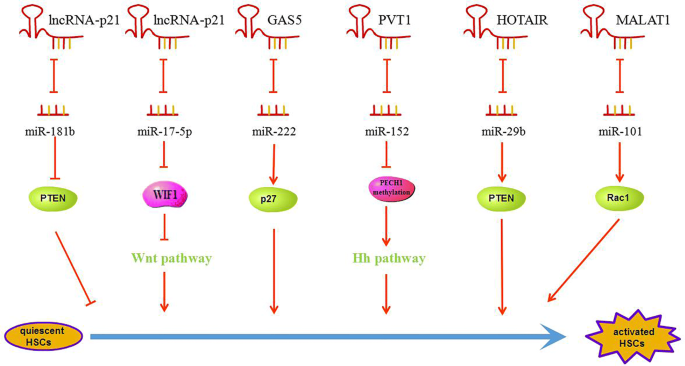
ceRNA核心作用模型图如下:
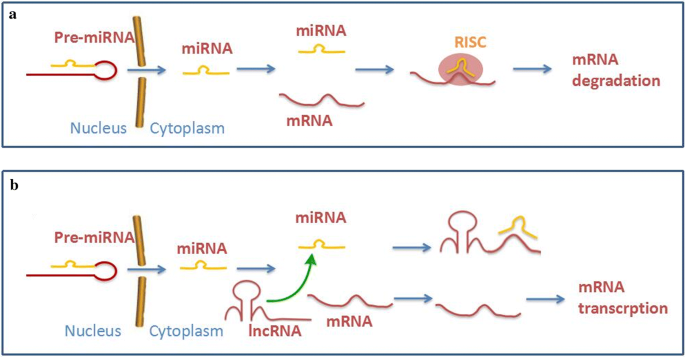
产品关联:文献未提及具体实验产品,领域常规使用双荧光素酶报告基因实验、RNA免疫共沉淀(RIP)等试剂/仪器。
4. Biomarker研究及发现成果
本综述指出,长链非编码RNA(lncRNA)在正常肝组织与纤维化肝组织中的表达差异,使其具备作为肝纤维化诊断生物标志物及治疗靶点的潜力,涉及的核心lncRNA包括MALAT1、lnc-LFAR1、MEG3、lncRNA-p21等。
Biomarker定位:这些lncRNA属于转录组学生物标志物,筛选逻辑基于临床样本的表达谱分析结合细胞/动物模型的功能验证,分为促进纤维化型(如MALAT1、lnc-LFAR1)和抑制纤维化型(如MEG3、lncRNA-p21)两类。研究过程详述:这些lncRNA的来源为临床肝组织样本或血清样本,验证方法主要包括荧光定量PCR(qRT-PCR)检测表达水平、细胞实验验证功能,文献未提供具体的特异性、敏感性数据及ROC曲线分析结果。核心成果提炼:核心成果在于明确了不同lncRNA对肝星状细胞(HSC)活化的双向调控作用,其中促进纤维化型lncRNA在纤维化组织中表达上调,抑制纤维化型lncRNA表达下调,提示其可作为肝纤维化的诊断生物标志物;同时,这些lncRNA及其调控的靶分子可作为潜在的治疗靶点,为肝纤维化的分子靶向治疗提供新方向。文献未提供具体的统计学结果(如HR值、P值),但明确指出lncRNA的表达差异与肝纤维化进程相关。
