1. 领域背景与文献引入
文献英文标题:Hyperoxia exposure upregulates Dvl-1 and activates Wnt/β-catenin signaling pathway in newborn rat lung;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:新生儿支气管肺发育不良(BPD)与高氧性肺损伤机制
支气管肺发育不良(BPD)是早产儿最常见的慢性肺部疾病,全球发病率约25%,严重影响早产儿的远期生存质量,甚至导致终身呼吸功能障碍。领域共识:氧疗是早产儿呼吸支持的核心手段,但高氧暴露会诱导肺组织氧化应激损伤,破坏肺泡发育进程,是BPD的关键致病因素之一。当前研究热点聚焦于肺发育相关信号通路的调控机制,其中Wnt/β-连环蛋白信号通路被证实参与肺上皮细胞分化、肺泡形成及肺纤维化过程,但其在高氧诱导BPD中的具体调控节点尚未明确。现有治疗手段以支持性护理为主,缺乏针对高氧性肺损伤的特异性干预靶点,因此明确高氧诱导BPD的分子调控机制,寻找潜在治疗靶点成为领域亟待解决的核心问题。本研究针对Dvl-1(散乱蛋白-1)这一Wnt通路关键调控因子,系统探讨其在高氧诱导新生大鼠肺损伤中的作用及机制,为BPD的精准治疗提供新的理论依据。
2. 文献综述解析
本文综述部分以“BPD发病机制-高氧损伤诱因-Wnt通路调控作用-Dvl-1研究空白”为核心逻辑,对领域内现有研究进行分层评述。现有研究已明确BPD的发病涉及遗传易感性与环境刺激的复杂交互作用,高氧通过诱导氧化应激、炎症反应及上皮细胞损伤推动疾病进展;Wnt/β-连环蛋白信号通路在肺胚胎发育、肺泡稳态维持中发挥关键作用,异常激活会导致肺纤维化、肺泡发育停滞等病理改变,是肺疾病领域的重要研究靶点;Dvl家族蛋白作为Wnt通路的上游调控因子,在肿瘤发生、组织纤维化中的功能已被证实,但在高氧诱导的BPD中未见相关报道。现有研究的优势在于确立了Wnt通路在肺疾病中的核心地位,为机制研究提供了方向,但局限性在于缺乏对Dvl-1这一关键节点的针对性研究,且未阐明其在高氧性肺损伤中的具体调控模式,也未提出基于该靶点的干预策略。通过对比现有研究的未解决问题,本文的创新价值凸显为首次揭示Dvl-1通过激活Wnt/β-连环蛋白通路促进高氧诱导的BPD发生,填补了Dvl-1在新生儿肺部疾病领域的研究空白,为BPD的靶向治疗提供了新的潜在靶点。
3. 研究思路总结与详细解析
本研究以“高氧诱导BPD的分子机制-Dvl-1的调控作用-干预策略验证”为核心逻辑,形成“动物模型构建→组织与细胞水平检测→机制验证→结论”的完整研究闭环。研究目标明确为阐明Dvl-1和Wnt/β-连环蛋白通路在高氧诱导新生大鼠肺损伤中的作用及调控机制,核心科学问题是Dvl-1如何通过调控Wnt通路影响肺泡Ⅱ型上皮细胞(AECII)的增殖、凋亡及迁移能力,最终为BPD寻找潜在治疗靶点。
3.1 高氧诱导新生大鼠BPD模型构建与肺组织病理检测
实验目的:建立高氧诱导的新生大鼠BPD模型,观察肺组织病理形态学变化及氧化应激水平,明确高氧对肺发育的损伤作用。
方法细节:将36只新生SD大鼠随机分为高氧组(85% O₂持续暴露)和常氧组(21% O₂),分别在出生后第3、7、14天处死大鼠,取肺组织进行苏木精-伊红(HE)染色观察肺泡结构,采用试剂盒检测肺组织中超氧化物歧化酶(SOD)活性和丙二醛(MDA)含量,评估氧化应激程度。
结果解读:HE染色结果显示,与常氧组相比,高氧组大鼠肺泡数量显著减少、体积增大、肺泡间隔增厚(n=9,P<0.01),呈现典型的BPD病理特征;氧化应激指标检测显示,高氧组SOD活性在第7天(P<0.05)和第14天(P<0.01)显著降低,MDA含量在第7天(P<0.05)和第14天(P<0.01)显著升高,提示高氧暴露诱导肺组织氧化损伤,抑制肺泡正常发育。
产品关联:实验所用关键产品:SOD和MDA检测试剂盒(Solarbio Life Sciences, Beijing, China),免疫组化试剂盒(MXB, Fujian, China)。
3.2 高氧对肺组织中Dvl-1及Wnt/β-连环蛋白通路分子表达的影响
实验目的:检测高氧暴露后新生大鼠肺组织中Dvl-1及Wnt/β-连环蛋白通路关键分子的表达变化,明确高氧对该通路的激活作用。
方法细节:采用蛋白质免疫印迹(Western blot)和实时荧光定量PCR(qRT-PCR)技术,检测不同时间点肺组织中Dvl-1、β-连环蛋白、CTNNBL1、细胞周期蛋白D1(cyclin D1)的蛋白和mRNA表达水平;通过免疫组化染色并半定量评分,观察上述分子在肺组织中的定位及表达强度。
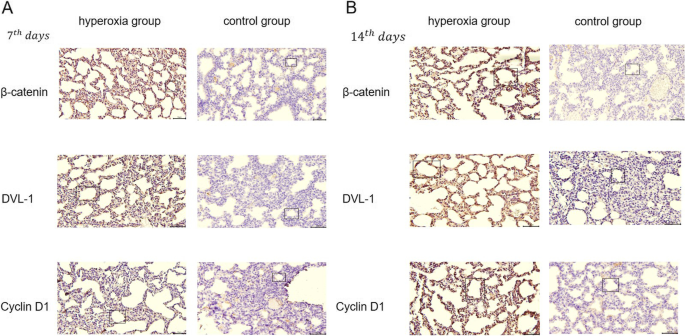
结果解读:Western blot结果显示,Dvl-1蛋白表达在高氧暴露第7、14天显著上调(P<0.01),β-连环蛋白、CTNNBL1、cyclin D1蛋白在第3、7、14天均显著上调(P<0.01);qRT-PCR结果与蛋白表达趋势一致;免疫组化评分显示,高氧组β-连环蛋白、Dvl-1、cyclin D1的表达强度显著高于常氧组(第7天P<0.01,第14天P<0.01),提示高氧暴露可激活Wnt/β-连环蛋白信号通路,且Dvl-1表达上调与通路激活密切相关。
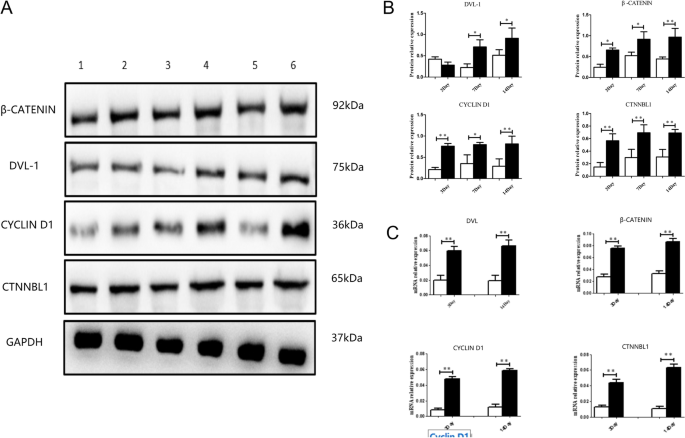
产品关联:实验所用关键产品:Dvl-1、β-连环蛋白等一抗(ZENBIO Biotech, Chengdu, China),Western blot相关试剂盒(Vazyme, Nanjing, China;Cell Signaling Technology, MA, USA)。
3.3 Dvl-1下调对高氧诱导AECII细胞功能的影响
实验目的:探讨Dvl-1下调对高氧环境下AECII细胞增殖、凋亡及迁移能力的影响,明确Dvl-1的功能作用。
方法细节:培养大鼠AECII细胞,分为对照组、高氧组、si-Dvl-1组、si-Dvl-1+高氧组、si-Dvl-1+高氧+MSAB(Wnt通路特异性抑制剂)组;采用细胞计数试剂盒-8(CCK-8)检测细胞增殖能力,Annexin V-FITC/PI双染色流式细胞术检测细胞凋亡率,划痕实验检测细胞迁移能力。
结果解读:CCK-8实验显示,高氧组细胞增殖率显著降低,si-Dvl-1处理可逆转该抑制作用,联合MSAB处理后增殖率进一步升高(P<0.01);流式细胞术结果显示,高氧组细胞凋亡率显著升高(P<0.01),si-Dvl-1处理可显著降低凋亡率(P<0.01);划痕实验显示,高氧组细胞迁移能力下降,si-Dvl-1处理可改善细胞迁移能力(P<0.05),提示Dvl-1下调对高氧诱导的AECII细胞损伤具有显著保护作用,且该作用可能通过抑制Wnt通路实现。
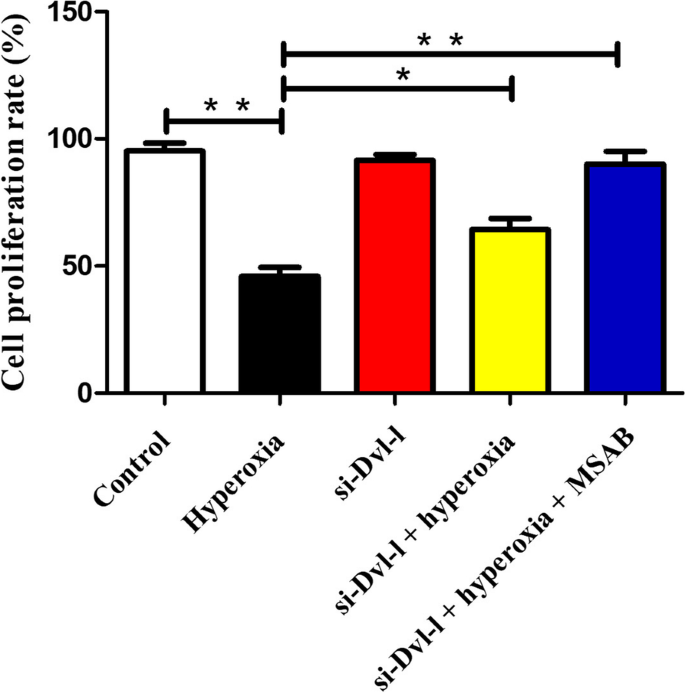
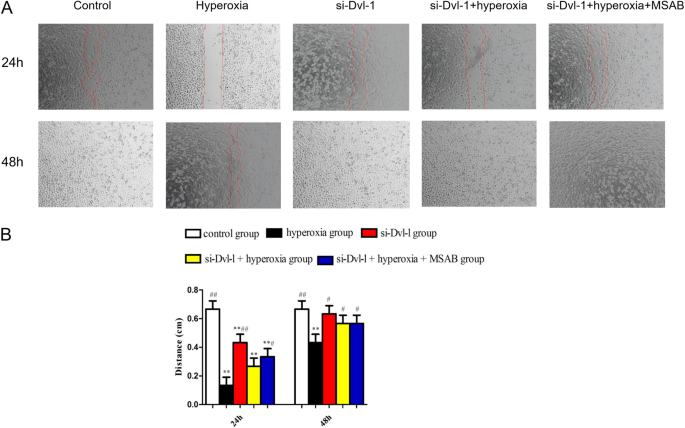
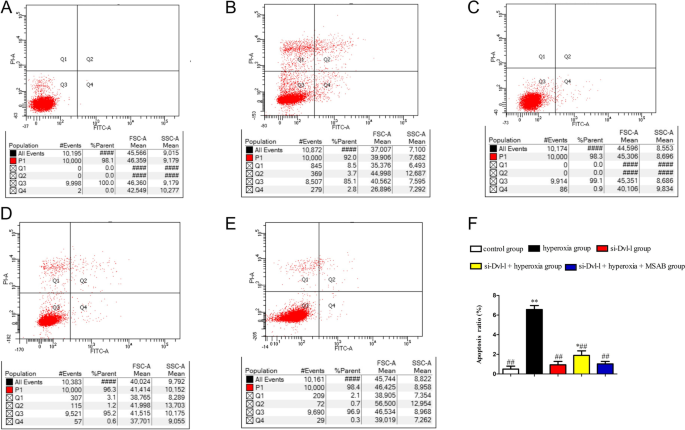
产品关联:实验所用关键产品:CCK-8试剂盒、Annexin V-FITC/PI凋亡检测试剂盒(Vazyme, Nanjing, China),MSAB(Selleck, Shanghai, China)。
3.4 Dvl-1下调对Wnt/β-连环蛋白通路分子表达的调控机制
实验目的:明确Dvl-1下调对高氧诱导的Wnt/β-连环蛋白通路激活的抑制作用,阐明其分子调控机制。
方法细节:采用qRT-PCR和Western blot技术,检测各组AECII细胞中GSK3β、p-GSK3β、β-连环蛋白、CTNNBL1、cyclin D1的mRNA和蛋白表达水平,分析Dvl-1下调对通路上下游分子的影响。
结果解读:qRT-PCR结果显示,高氧组上述分子的mRNA表达显著上调(P<0.01),si-Dvl-1处理可显著降低其表达水平(P<0.01);Western blot结果显示,高氧组GSK3β、p-GSK3β、β-连环蛋白等蛋白表达显著上调(P<0.01),si-Dvl-1处理可显著抑制其表达,联合MSAB处理后抑制效果进一步增强,提示Dvl-1通过调控Wnt/β-连环蛋白通路的关键分子表达,参与高氧诱导的AECII细胞损伤,下调Dvl-1可有效抑制通路激活。
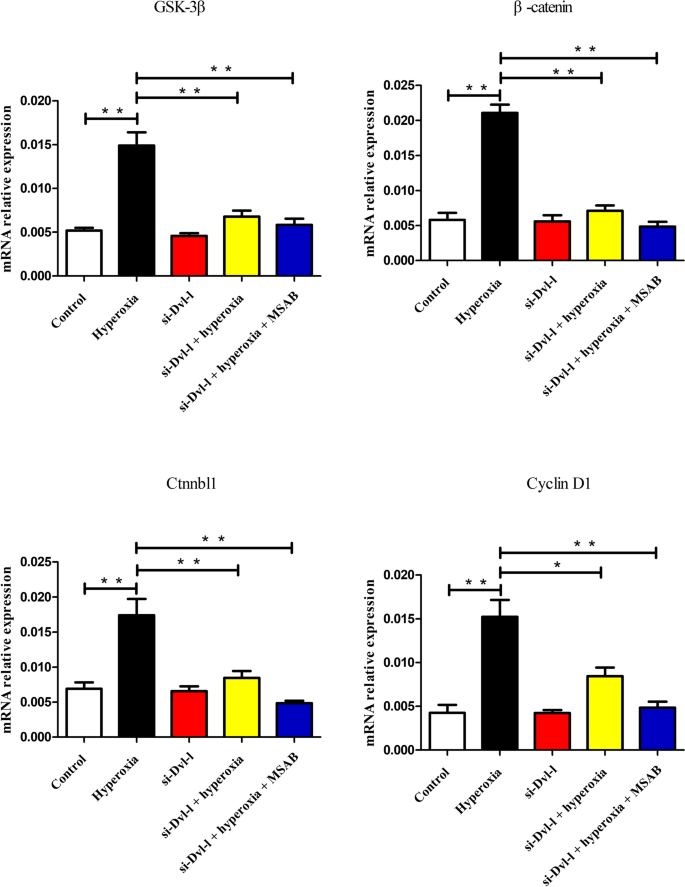
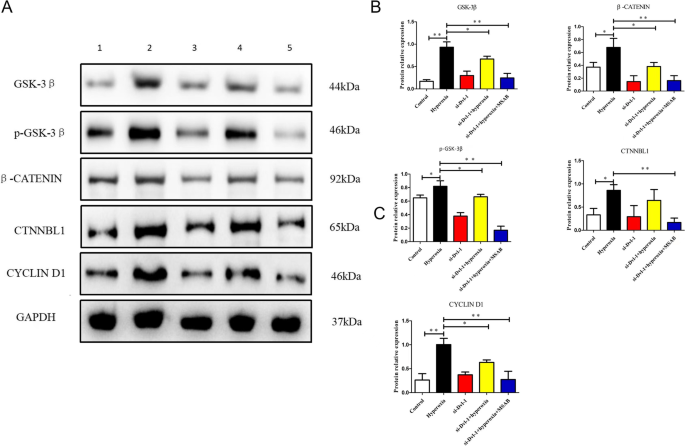
产品关联:实验所用关键产品:qRT-PCR试剂盒(TaKaRa, Dalian, China),Western blot相关试剂同前。
4. Biomarker研究及发现成果
Biomarker定位
本文涉及的Biomarker为Dvl-1,属于蛋白类功能型生物标志物,其筛选与验证逻辑为“临床病理关联-细胞功能验证-通路机制解析”:首先通过动物模型发现高氧诱导的肺组织中Dvl-1表达显著上调,与BPD病理严重程度相关;随后通过细胞实验验证Dvl-1对AECII细胞功能的调控作用;最后明确其通过激活Wnt/β-连环蛋白通路参与疾病进程,形成完整的验证链条。
研究过程详述
Dvl-1的来源为新生大鼠肺组织及体外培养的AECII细胞,验证方法包括免疫组化、Western blot、qRT-PCR等。特异性方面,高氧暴露后肺组织中Dvl-1的表达水平显著高于常氧组(第7天P<0.01,第14天P<0.01),且与Wnt通路下游分子的表达呈正相关;敏感性方面,高氧暴露第7天即可检测到Dvl-1的显著上调,可作为早期损伤的检测指标。
核心成果提炼
本研究核心成果为证实Dvl-1是高氧诱导BPD的关键调控因子,其功能关联表现为Dvl-1高表达可激活Wnt/β-连环蛋白通路,抑制AECII细胞增殖、促进凋亡并降低迁移能力,推动BPD的病理进程;创新性在于首次在新生儿肺部疾病领域揭示Dvl-1的调控作用,明确其作为BPD潜在治疗靶点的价值;统计学结果显示,Dvl-1表达上调及通路分子激活均具有显著统计学意义(P<0.01),样本量覆盖动物实验n=9、细胞实验重复3次以上,数据可靠性较高。研究结论为靶向下调Dvl-1可通过抑制Wnt/β-连环蛋白通路激活,减轻高氧诱导的肺损伤,为BPD的精准治疗提供了新的方向。