1. 领域背景与文献引入
文献英文标题:Sorting of cells of the same size, shape, and cell cycle stage for a single cell level assay without staining;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学-单细胞分析技术
2006年前后,生命科学领域的单细胞水平研究进入快速发展阶段,RT-PCR扩增技术的优化实现了单细胞基因表达的精准检测,微加工技术的进步提升了细胞定位、形态分析及细胞间接触研究的精度,高通量膜片钳技术也突破了传统操作的技术壁垒。然而,单细胞分析的样本纯化技术并未同步发展,群体水平研究中可忽略的细胞异质性,在单细胞分析中会成为干扰实验结果的核心因素。克隆细胞系虽遗传背景一致,但因细胞周期差异、机械分散导致的细胞聚集、表型自然变异等问题,仍存在显著的形态异质性;传统细胞分选依赖特异性荧光标记,存在标记过程复杂、标记效率不均一、易造成细胞损伤等局限,缺乏一种无标记、快速、可定量的均一细胞分选方法,制约了单细胞分析技术的进一步应用。本文正是针对这一研究空白,旨在开发基于光散射参数的无标记活单细胞分选技术,为单细胞分析提供标准化的样本前处理方案。
2. 文献综述解析
作者将现有研究分为两大类别,一是单细胞分析技术的发展现状,二是细胞分选技术的应用局限,通过对比两类技术的进展与不足,凸显样本前处理技术对单细胞分析的制约作用。
现有单细胞分析技术的关键结论显示,RT-PCR、微加工、高通量膜片钳等技术已能检测群体水平无法观察到的细胞个体特性,但样本中的死细胞、细胞聚集体及形态异质性细胞会严重干扰实验数据的准确性;细胞分选技术方面,荧光标记分选可通过特异性标记实现目标细胞的精准富集,但其标记过程需针对不同样本优化,且标记试剂可能损伤细胞、导致标记异质性,限制了其在单细胞分析中的应用;光散射分选技术可反映细胞大小、形态等通用物理特性,无需标记,但其传统应用仅采用单一光散射参数,无法有效区分大体积单细胞与小型细胞聚集体,难以获得均一的活单细胞群体。现有研究的局限性在于,单细胞分析缺乏标准化的样本前处理方法,光散射分选的参数应用不充分,无法满足单细胞分析对均一样本的需求。本文的创新价值在于,首次同时整合前向散射与侧向散射的峰高及面积四个参数,建立无标记的活单细胞分选方法,解决了传统光散射分选无法区分单细胞与聚集体的难题,且分选后的细胞保持完整的生物学功能,为单细胞分析提供了可靠的样本前处理技术。
3. 研究思路总结与详细解析
本研究的整体目标是建立一种无标记、快速、可定量的活单细胞分选方法,用于单细胞水平分析的样本前处理;核心科学问题是如何利用光散射参数有效区分活细胞与死细胞、单细胞与细胞聚集体,并关联光散射参数与细胞大小、形态、细胞周期等生物学特性;技术路线遵循“参数筛选→分群验证→亚分群分析→功能验证”的闭环逻辑,从光散射参数的优化应用到分选细胞的功能完整性验证,逐步完善方法体系。
3.1 活细胞与死细胞的光散射分群验证
本环节的实验目的是确定可有效区分活细胞与死细胞的光散射参数组合。实验采用大鼠嗜铬细胞瘤PC12细胞系,通过钙黄绿素AM(活细胞特异性标记,可透过完整细胞膜并被酯酶水解为绿色荧光产物)和碘化丙啶(PI,死细胞标记,仅能透过破损细胞膜染色核酸)对细胞进行染色,同时检测前向散射峰高(FSheight)、前向散射面积(FSarea)、侧向散射峰高(SSheight)、侧向散射面积(SSarea)四个光散射参数的散点图分布。结果显示,活细胞(钙黄绿素阳性、PI阴性)集中分布在高FSarea、中SSheight/SSarea分群,而死细胞或细胞碎片则集中在低FSarea、低至中SSarea分群,且死细胞在FSarea-FSheight和SSarea-SSheight散点图的上部区域(峰高/面积比值较高),这一分布差异说明四个光散射参数的组合可有效区分活细胞与死细胞,避免死细胞对后续单细胞分析的干扰。
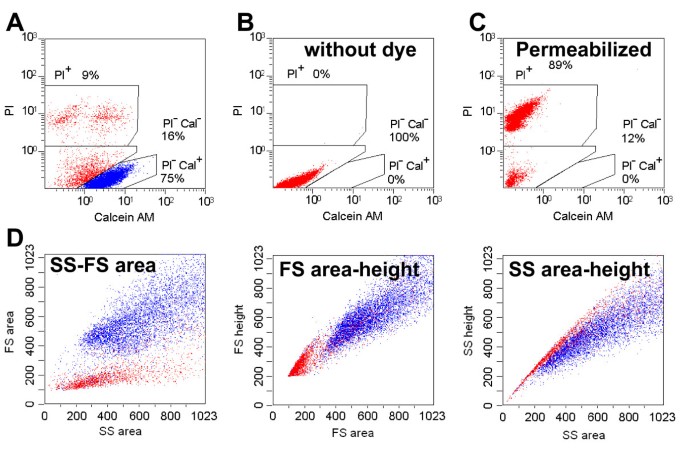
实验所用关键产品:钙黄绿素AM(Molecular Probes, 货号c3100)、碘化丙啶(Sigma-Aldrich, 货号A4378)、EPICS ALTRA流式细胞仪(Beckman Coulter)。
3.2 单细胞与细胞聚集体的光散射区分验证
本环节的实验目的是建立无标记区分单细胞与细胞聚集体的方法,解决传统分选无法区分大体积单细胞与小型聚集体的难题。实验基于“细胞聚集体的峰高/面积比值低于同体积单细胞”的假设,对FSarea-FSheight和SSarea-SSheight散点图中的不同分群细胞进行分选,采用SYTO24(细胞通透性核酸染料)染色后计数细胞核数量,验证单细胞比例;同时采用乙醇固定细胞后PI染色,通过DNA含量分析进一步验证分群的准确性。结果显示,低SS、中FS分群,以及高FSheight/FSarea、SSheight/SSarea分群中的单细胞比例显著更高,细胞聚集体集中在低峰高/面积比值的分群中;乙醇固定细胞的PI染色结果显示,高峰高/面积比值分群中细胞聚集体的比例低于2%,而低比值分群中这一比例达17%,证明该方法可有效区分单细胞与细胞聚集体,且适用于活细胞与固定细胞。
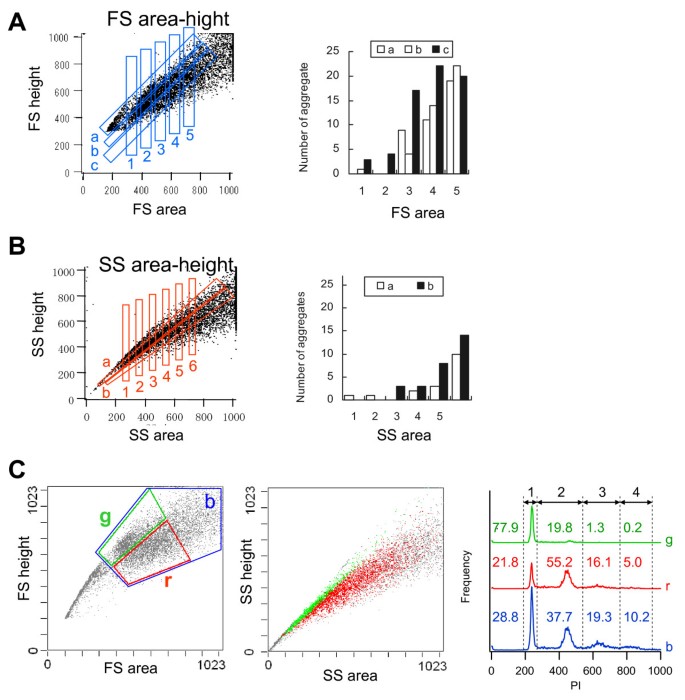
实验所用关键产品:SYTO24(Molecular Probes, 货号S7559)、EPICS ALTRA流式细胞仪(Beckman Coulter)。
3.3 12个活单细胞亚分群的划分与形态关联分析
本环节的实验目的是在活单细胞分群内划分均一的亚分群,并建立光散射参数与细胞形态特征的关联。实验基于FSarea和SSarea两个参数,在活单细胞分群内设置12个亚分群,采用相差显微镜观察各亚分群细胞的形态,通过图像分析软件测量细胞直径、伸长率、表面粗糙度等指标。结果显示,SSarea与细胞体积成正比,当SSn(标准化SSarea)为2.00时,细胞相对体积约为2(n=各亚分群测量细胞数,P<0.05);FSarea与细胞圆形度、伸长率及DNA含量相关,细胞伸长率随FSn(标准化FSarea)升高而显著增加(P<0.0005);细胞表面粗糙度随SSn升高而升高、随FSn升高而降低,且与细胞活力呈显著负相关(Pearson相关系数<0,P<0.05),表面粗糙度高的细胞活力较低。
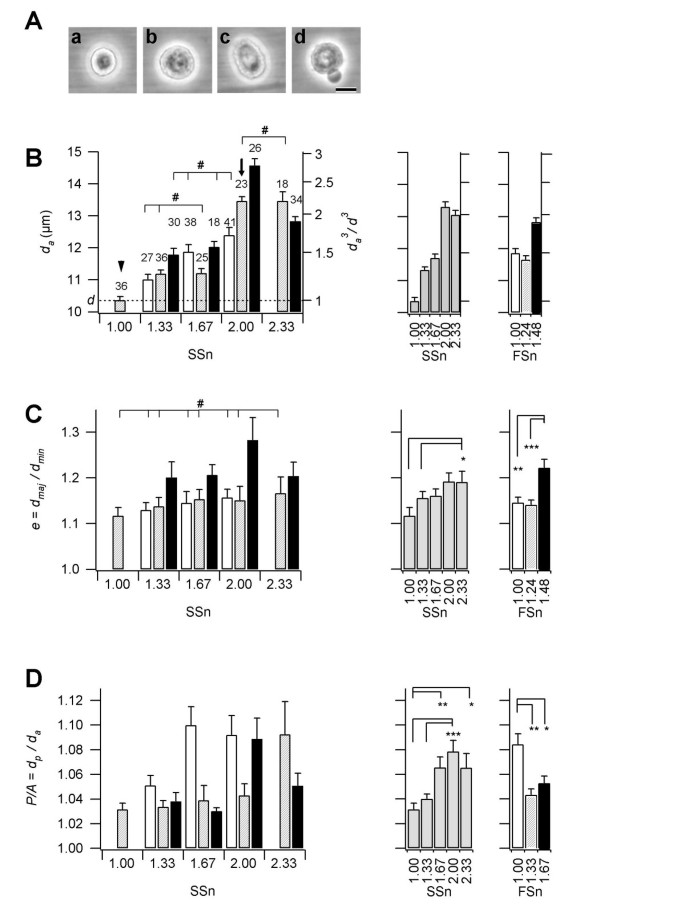
实验所用关键产品:Nikon TS100倒置显微镜、Coolpix 995数码相机、Scion Image图像分析软件。
3.4 亚分群细胞周期与功能特性验证
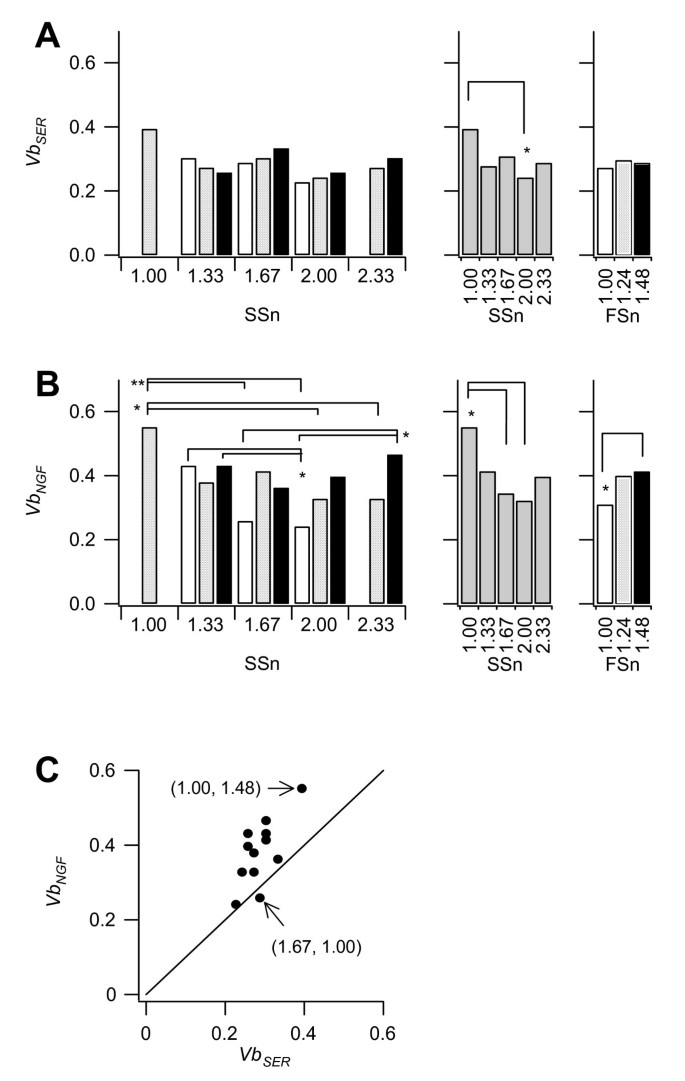
本环节的实验目的是关联光散射参数与细胞周期,并验证分选后细胞的生物学功能完整性。实验对12个亚分群的细胞进行分选,固定后采用PI染色检测DNA含量,分析细胞周期分布;同时将分选后的单细胞接种于胶原包被的96孔板,分为添加神经生长因子(NGF)与不添加NGF两组,培养后检测细胞活力、增殖能力与分化潜能。结果显示,低FSn、SSn的亚分群以G1期细胞为主,高FSn、SSn的亚分群中S/G2/M期细胞比例显著升高,且细胞伸长率与S/G2/M期细胞比例呈显著正相关(Pearson相关系数=0.9,P<0.0025);所有亚分群的细胞活力均高于20%,添加NGF后细胞活力最高可达60%(n=各亚分群,P<0.05),分化率超过70%,且NGF可显著提高细胞活力但降低增殖能力,证明分选后的细胞保持正常的存活、增殖与分化功能。
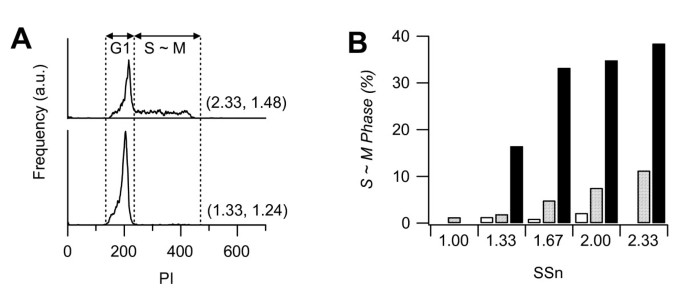
实验所用关键产品:神经生长因子(NGF)、96孔胶原包被板(Iwaki)、EPICS ALTRA流式细胞仪(Beckman Coulter)。
4. Biomarker研究及发现成果
本文中的Biomarker为基于光散射参数的细胞特性标记物,包括标准化前向散射面积(FSn)和标准化侧向散射面积(SSn),其筛选与验证逻辑为“活单细胞分群筛选→12亚分群划分→形态与细胞周期关联→功能验证”的完整链条。
该Biomarker的来源为PC12细胞系的活单细胞群体,验证方法包括相差显微镜形态测量、PI染色细胞周期分析、单细胞培养功能检测。特异性与敏感性数据显示,SSn与细胞体积呈线性正相关(相对体积随SSn从1.00升至2.00增加约1倍,文献未明确样本量,基于图表趋势推测),FSn与细胞伸长率呈显著正相关(P<0.0005),且与S/G2/M期细胞比例呈显著正相关(Pearson相关系数=0.9,P<0.0025)。
核心成果方面,FSn可作为细胞伸长率与细胞周期的标记物,SSn可作为细胞体积的定量标记物;首次发现NGF在血清存在下可提高PC12细胞活力但抑制其增殖能力,这一结论通过单细胞培养实验独立验证了活力与增殖的调控关系;该无标记分选方法的创新性在于,首次同时使用四个光散射参数实现活单细胞的精准分选,分选细胞保持完整生物学功能,为单细胞分析提供了标准化的样本前处理方案,且可推广至多种细胞系的单细胞分析前处理。
