1. 领域背景与文献引入
文献英文标题:Canine intestinal organoids as a platform for studying MHC class II expression in epithelial cells;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:兽医免疫学/犬肠道免疫病理。
肠道上皮细胞(IECs)、免疫系统与肠道微生物组的相互作用是维持胃肠道稳态、介导抗原应答的核心环节。主要组织相容性复合体(MHC)II类分子(犬中称为犬白细胞抗原,DLA)是调控CD4+T细胞免疫应答的关键分子,传统观点认为其仅在巨噬细胞、B淋巴细胞等专职抗原呈递细胞上表达,近年研究证实IECs在炎症细胞因子如干扰素-γ(IFN-γ)诱导下也可表达MHC II类分子,参与肠道免疫调控,这一机制在炎症性肠病(IBD)等病理状态下尤为重要。在兽医领域,犬类IBD等肠道免疫疾病的发病率逐年上升,DLA基因多态性与疾病易感性相关,但犬IECs上MHC II类分子的表达调控机制仍未明确,现有研究存在样本量有限、缺乏合适体外模型的问题——犬源细胞系稀缺,小鼠模型无法完全模拟犬的生理代谢与肠道环境,导致基础研究与临床应用存在明显断层。肠道类器官作为新兴的体外模型,可从活检样本构建并模拟肠道上皮的细胞组成与功能,为解析犬肠道免疫机制提供了新途径。本研究旨在利用犬肠道类器官模型,探究MHC II类分子的表达动态及其调控机制,填补犬肠道免疫病理研究的空白。
2. 文献综述解析
作者以物种(人、小鼠、犬)、研究模型(体内/体外)、病理状态(健康/炎症)为核心分类维度,系统梳理了MHC II类分子在肠道上皮细胞中的表达调控研究。现有研究的关键结论显示,人、小鼠的IECs可在IFN-γ诱导下通过II类反式激活因子(CIITA)调控MHC II类分子表达,参与CD4+T细胞应答与肠道炎症调控;犬类中仅少量研究发现健康或炎症肠道组织中存在DLA表达,但未明确其调控机制与功能意义。技术方法层面,传统体外细胞系模型缺乏犬源体系,小鼠模型虽能揭示部分保守机制,但无法还原犬的生理特征;肠道类器官模型可从临床样本构建,保留原组织的细胞组成与遗传特征,适合开展个性化研究,但此前尚未应用于犬MHC II类分子的研究。现有研究的核心局限性在于,犬肠道上皮细胞分化状态对MHC II类分子表达的影响尚未被探究,缺乏系统的体外实验验证细胞因子的调控作用。本研究的创新价值在于,首次将犬肠道类器官作为模型,明确了分化状态对IFN-γ诱导的DLA表达的调控作用,证明分化后的IECs具有更强的MHC II类分子表达能力,为犬肠道免疫疾病的机制研究与药物筛选提供了新的平台。
3. 研究思路总结与详细解析
本研究的整体框架为:以健康犬结肠活检样本构建肠道类器官模型,通过分化培养基诱导类器官成熟,结合促炎细胞因子处理,从mRNA与蛋白水平解析MHC II类分子(DLA-DRA)的表达调控机制,核心科学问题是犬IECs的分化状态如何影响IFN-γ诱导的DLA表达及CIITA的调控作用,技术路线遵循“样本获取→模型构建→分化诱导→刺激处理→检测验证→统计分析”的闭环逻辑。
3.1 犬结肠类器官的构建与分化验证
实验目的:构建稳定的健康犬结肠类器官模型,并验证分化培养基对类器官向成熟肠道上皮细胞分化的诱导作用。
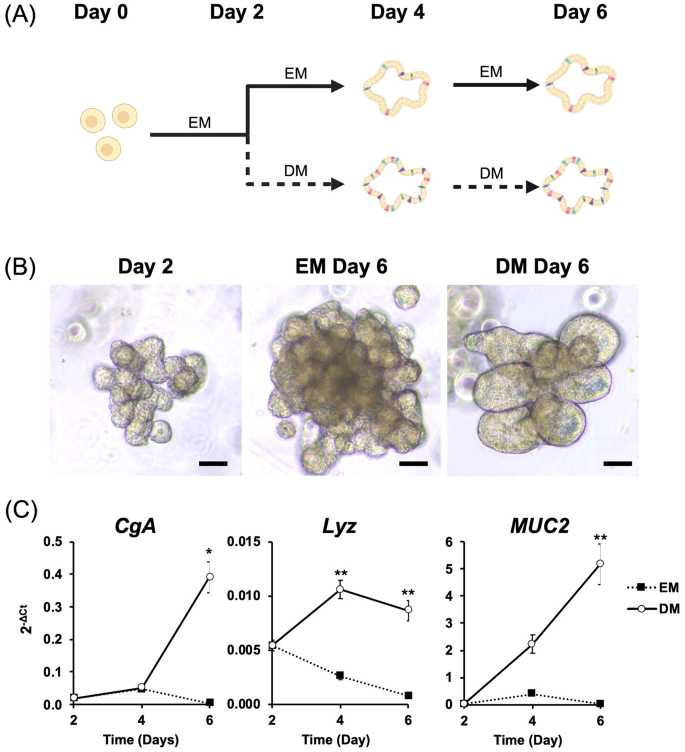
方法细节:从3只健康犬的结肠活检样本中分离肠隐窝,将隐窝重悬于Matrigel后接种于48孔板,加入含Wnt-3a、烟酰胺等成分的扩增培养基(EM)培养,每6-8天用Cell Recovery Solution溶解Matrigel并传代;诱导分化时,将培养2天的类器官更换为不含Wnt-3a、烟酰胺、SB202190的分化培养基(DM),培养4天,以持续培养于EM的类器官为对照;采用实时定量反转录PCR(qRT-PCR)检测嗜铬粒蛋白A(CgA,肠内分泌细胞标志物)、溶菌酶(Lyz,潘氏细胞标志物)、粘蛋白2(MUC2,杯状细胞标志物)的mRNA表达水平。
结果解读:形态学观察显示,DM培养的类器官与EM组均保持芽状结构,无明显差异(图1b);qRT-PCR结果显示,DM组的CgA表达在第4-6天显著高于EM组(n=2,P=0.017),Lyz表达在第4、6天显著高于EM组(n=2,P=0.002),MUC2表达随培养时间递增,第6天显著高于EM组(n=2,P=0.002)(图1c),证实DM可有效诱导类器官分化为成熟的肠道上皮细胞。
产品关联:实验所用关键产品:Corning的Matrigel、Thermo Fisher Scientific的DMEM/F12培养基、GultaMAX、HEPES、青霉素/链霉素、TrypLE Express、High-Capacity cDNA Reverse Transcription Kit、PowerUp SYBR Green Master Mix,Qiagen的RNeasy Mini Kit,PeproTech的重组小鼠Wnt-3a、EGF,Sigma-Aldrich的胃泌素、A-83-01、SB202190、烟酰胺,R&D Systems的N-2 MAX培养基补充剂等。
3.2 促炎细胞因子对DLA-DRA表达的诱导作用
实验目的:筛选可诱导犬结肠类器官DLA-DRA表达的促炎细胞因子,并明确IFN-γ的剂量与时间依赖调控作用。
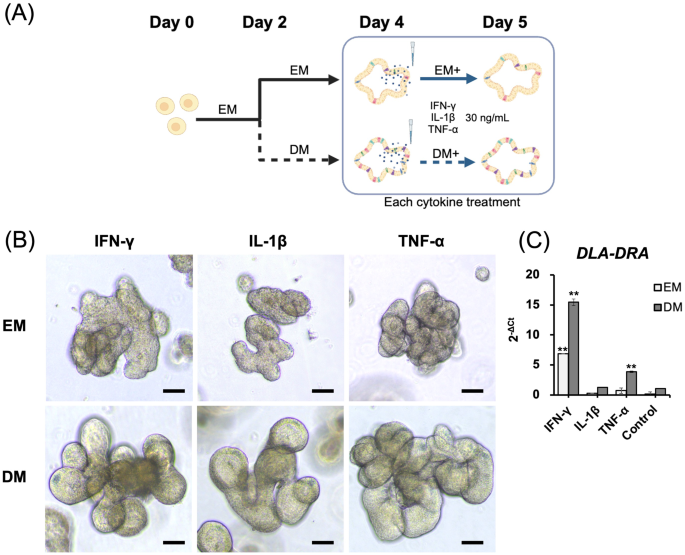
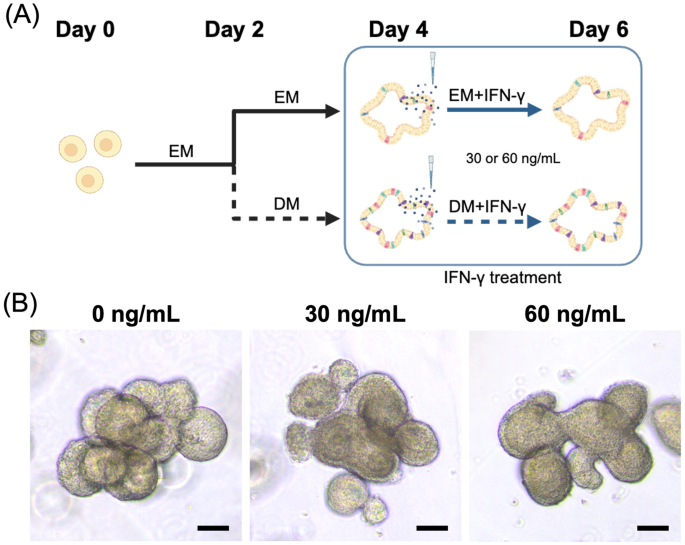
方法细节:类器官先在EM中培养2天,更换为DM培养2天,随后分别用30 ng/mL的重组犬IFN-γ、肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)处理24小时,以PBS处理为对照;进一步设置30、60 ng/mL两种IFN-γ剂量,在处理后0、24、48小时收集样本,采用qRT-PCR检测DLA-DRA与CIITA的mRNA表达水平。
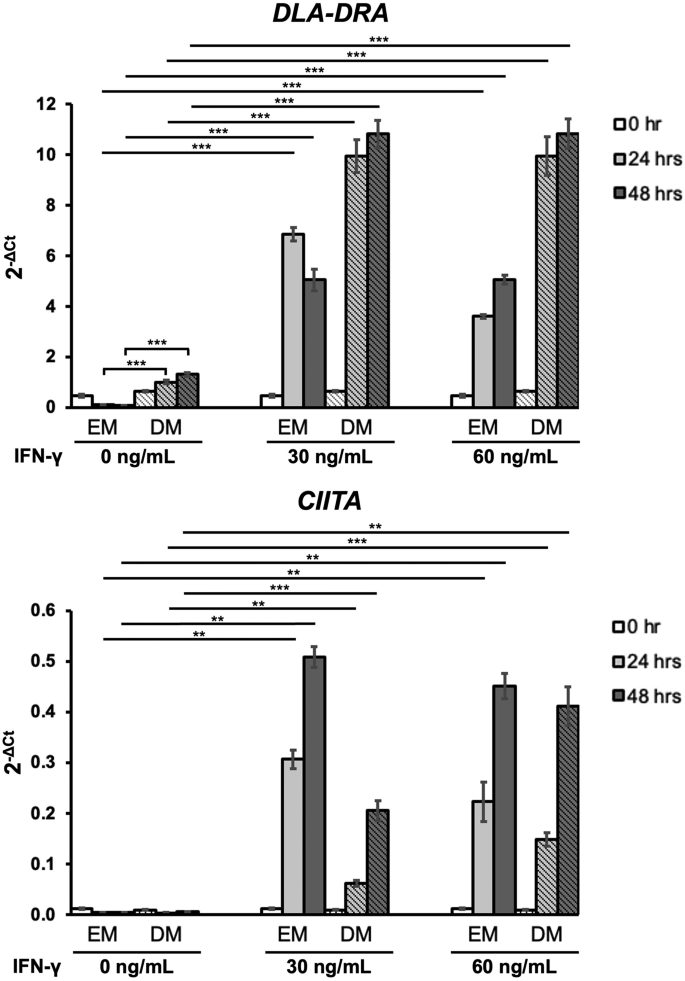
结果解读:形态学观察显示,各细胞因子处理组的类器官形态无明显变化(图2b);qRT-PCR结果显示,EM组中仅IFN-γ处理可显著上调DLA-DRA表达,DM组中IFN-γ与TNF-α处理均能诱导表达上调,但IFN-γ的诱导作用最强(图2c);剂量与时间依赖实验显示,DM对照组的DLA-DRA表达在24、48小时显著高于EM对照组(n=3,P<0.001),IFN-γ处理后,DM组的DLA-DRA表达在24、48小时均显著高于未处理组(n=3,P<0.001),且上调幅度显著高于EM组(n=3,P<0.001);CIITA mRNA表达在DM组中随IFN-γ剂量与处理时间递增,24小时时30 ng/mL组P=0.002、60 ng/mL组P<0.001,48小时时30 ng/mL组P<0.001、60 ng/mL组P=0.008(图4),证实IFN-γ通过激活CIITA通路调控DLA-DRA表达,且分化后的IECs对IFN-γ的响应更强。
产品关联:实验所用关键产品:R&D Systems的重组犬IFN-γ、TNF-α、IL-1β,Bio-Rad的CFX96 Touch实时PCR检测系统等。
3.3 IFN-γ对DLA-DR蛋白表达的调控验证
实验目的:从蛋白水平验证IFN-γ对犬结肠类器官DLA-DR表达的诱导作用。
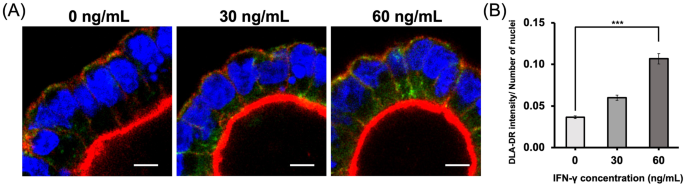
方法细节:用0、30、60 ng/mL的IFN-γ处理DM培养的类器官48小时,采用免疫荧光染色检测DLA-DR蛋白表达:以犬外周血单个核细胞(PBMCs)为阳性对照,同型抗体为阴性对照,用抗HLA-DR抗体(交叉识别犬DLA-DR)标记蛋白,结合DAPI核染色与F-actin细胞骨架染色,通过共聚焦显微镜观察并采集图像;用ImageJ软件分析荧光强度,以细胞核数量归一化处理。
结果解读:免疫荧光图像显示,DM培养的类器官在IFN-γ处理后,DLA-DR的荧光强度随剂量增加而升高(图5a);定量分析显示,60 ng/mL IFN-γ处理组的荧光强度显著高于0 ng/mL对照组(n=2,P=0.001)(图5b),EM组中60 ng/mL处理组的荧光强度也显著高于对照组(n=2,P=0.021),进一步证实IFN-γ可剂量依赖性地上调DLA-DR蛋白表达,分化状态增强了这种诱导效应。
产品关联:实验所用关键产品:Abcam的抗HLA-DR抗体(TAL1B5)、山羊抗小鼠IgG H&L(DyLight 488),Thermo Fisher Scientific的DAPI、Alexa Fluor™ 647 Phalloidin、Prolong Gold抗淬灭试剂,Leica的SP8-X共聚焦显微镜等。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究的核心Biomarker是犬白细胞抗原DR alpha(DLA-DRA,MHC II类分子的α亚基),筛选逻辑基于其无遗传多态性、表达稳定的特征,可作为MHC II类分子表达的通用标志物;验证逻辑为:通过细胞因子处理类器官,从mRNA与蛋白水平验证其表达调控,结合分化状态分析表达差异,完整链条为“理论筛选→细胞模型验证→mRNA/蛋白水平定量”。
研究过程详述
该Biomarker的来源为健康犬结肠类器官的上皮细胞;验证方法包括qRT-PCR定量检测DLA-DRA与CIITA的mRNA表达,免疫荧光染色结合图像分析检测DLA-DR蛋白表达;特异性与敏感性数据显示,IFN-γ处理后,DM组的DLA-DRA mRNA表达在24小时显著上调(n=3,P<0.001),蛋白水平60 ng/mL处理组的荧光强度较对照组升高约2.1倍(n=2,P=0.001),表明DLA-DRA可特异性响应IFN-γ的诱导,分化状态能显著增强其表达敏感性。
核心成果提炼
该Biomarker的功能关联在于,可作为犬肠道上皮细胞免疫激活的标志物,反映IECs作为非专职抗原呈递细胞的功能状态,为评估肠道免疫激活程度提供量化指标;创新性在于,首次在犬肠道类器官模型中明确了分化状态对IFN-γ诱导的DLA表达的调控作用,证明分化后的IECs具有更强的MHC II类分子表达能力,为犬IBD等免疫介导肠道疾病的机制研究提供了新的靶点与模型;核心统计学结果包括:DM组DLA-DRA mRNA表达在24小时较EM组上调1.8倍(n=3,P<0.001),60 ng/mL IFN-γ处理后DM组的DLA-DR蛋白荧光强度较对照组升高2.1倍(n=2,P=0.001),CIITA mRNA表达在48小时较对照组上调3.2倍(n=3,P<0.001)。
