1. 领域背景与文献引入
文献英文标题:Transcriptome analysis reveals an important candidate gene involved in both nodal metastasis and prognosis in lung adenocarcinoma;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:肺腺癌转录组学与肿瘤转移预后研究
肺腺癌是非小细胞肺癌最常见的组织学亚型,约占所有肺癌的40%,起源于肺外周区域的健康细胞恶性转化,早期多沿细支气管生长,进展相对缓慢,但一旦发生淋巴结转移,治疗难度将大幅提升。领域共识:肺癌淋巴结转移是导致患者预后恶化的核心因素之一,转移性肺癌患者的5年生存率仅约1%,当前临床缺乏同时兼具转移预测与预后评估价值的特异性生物标志物,现有研究多聚焦单一维度的标志物筛选,未实现转移与预后的整合分析。针对这一研究空白,本研究通过整合TCGA数据库的转录组数据与临床信息,开展全景式差异基因筛选与功能验证,旨在发现同时关联肺腺癌淋巴结转移和患者预后的关键基因,为肺腺癌的精准诊疗提供新的生物标志物与理论依据。
2. 文献综述解析
作者按“肺腺癌临床特征→转移机制研究现状→现有生物标志物局限性”的逻辑维度展开综述评述。现有研究已明确肺腺癌易发生淋巴结转移,转移后患者预后极差,转录组学技术的发展为大规模筛选转移相关基因提供了技术支撑,TCGA等公共数据库的开放也为全景式分析提供了样本基础,但多数研究存在明显局限性:一是仅关注转移或预后单一维度,未筛选同时兼具双重功能的标志物;二是未对淋巴结转移的梯度变化(如N0到N2的连续过程)进行分析,难以揭示转移的动态调控机制;三是缺乏独立数据集的验证,结论的临床转化价值有限。本研究的创新价值在于,首次通过整合淋巴结转移梯度变化分析与生存分析,筛选出同时关联转移和预后的长链非编码RNA假基因RN7SL494P,并通过CCLE细胞系数据集进行独立验证,弥补了现有研究在标志物双重功能及验证体系上的不足,为肺腺癌的精准诊疗提供了新的潜在靶点。
3. 研究思路总结与详细解析
本研究的核心目标是筛选肺腺癌中同时关联淋巴结转移和患者预后的关键生物标志物,核心科学问题是明确RN7SL494P在肺腺癌转移及预后中的作用及潜在调控机制,技术路线遵循“TCGA数据挖掘→差异基因筛选→梯度变化与生存分析→Cox回归验证→CCLE数据集独立验证”的完整闭环,逻辑严谨,验证体系完善。
3.1 TCGA数据库转录组与临床数据整合分析
实验目的是获取肺腺癌组织与正常组织的转录组差异特征,以及淋巴结转移、TNM分期相关的差异表达基因,为后续筛选核心标志物奠定基础。方法细节为从TCGA数据库下载515例肺腺癌患者的RNA-seq数据及对应的临床信息,使用edgeR软件进行差异基因表达分析,以平均每百万读数(CPM)作为基因表达水平的纳入标准,筛选具有统计学意义的差异表达基因。结果解读显示,共鉴定出13118个肺腺癌与正常组织的差异表达基因,其中2800个基因表达下调,10318个基因表达上调,GO分析显示上调基因显著富集于细胞外囊泡、细胞膜、线粒体等组分(
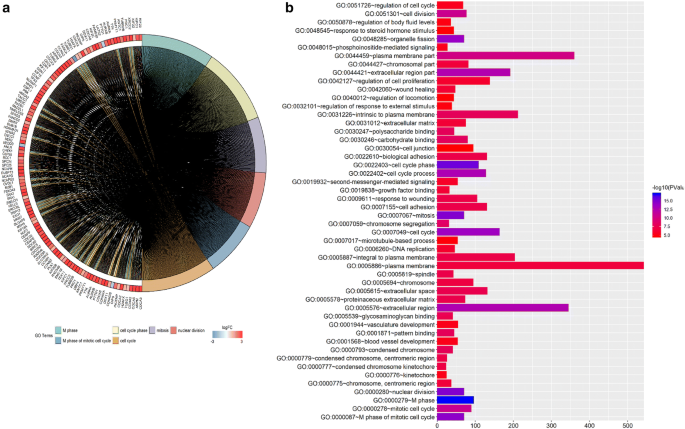
);针对淋巴结转移(N0-N2)筛选出406个差异基因,TNM分期筛选出439个差异基因,韦恩图分析显示两者存在296个重叠基因(
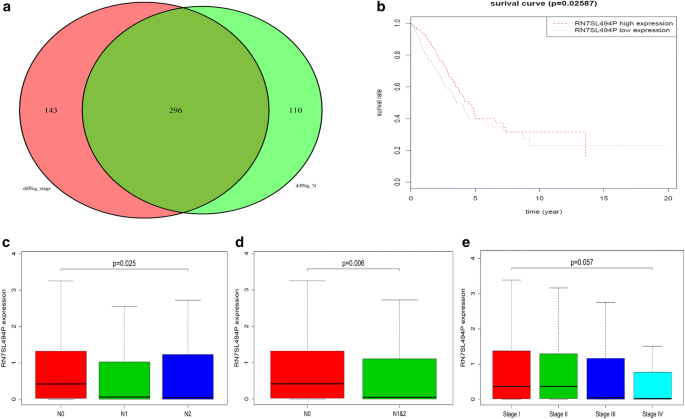
)。文献未提及具体实验产品,领域常规使用生物信息学分析软件(如edgeR、DAVID等)及公共数据库(TCGA、CCLE)。
3.2 差异基因的梯度变化与生存分析
实验目的是筛选随淋巴结转移梯度及TNM分期梯度动态变化的基因,并进一步关联患者生存时间,锁定兼具转移预测与预后评估价值的核心基因。方法细节为采用Kruskal-Wallis检验分析差异基因在淋巴结转移梯度(N0、N1、N2)及TNM分期(I-IV)中的表达变化,通过Kaplan-Meier检验分析基因表达与患者生存时间的相关性。结果解读显示,112个基因与淋巴结转移或TNM分期的梯度变化相关,其中仅RN7SL494P的表达与患者生存时间显著相关(

),且其表达随淋巴结转移梯度升高呈现显著变化,N0 vs N1 vs N2的P值为0.02587,N0 vs N1+N2的P值为0.006,但与TNM分期的梯度变化无显著相关性(P=0.057)。文献未提及具体实验产品,领域常规使用生存分析软件(如R语言的survival包)。
3.3 Cox回归模型验证RN7SL494P的独立预后价值
实验目的是验证RN7SL494P是否为肺腺癌患者预后的独立影响因素,排除其他临床因素的干扰。方法细节为将患者年龄、性别、放疗史、化疗史、病理分级、T分期、N分期及RN7SL494P表达水平纳入单因素及多因素Cox回归分析,评估各因素对患者生存的影响。结果解读显示,单因素Cox分析显示RN7SL494P高表达可显著降低患者死亡风险(风险比HR=0.78,P=0.020);多因素Cox分析显示RN7SL494P仍为独立预后因素(HR=0.78,P=0.028),同时年龄、T分期、N分期也是独立风险因素,放疗可能降低治疗疗效,而化疗可显著延长患者生存时间(
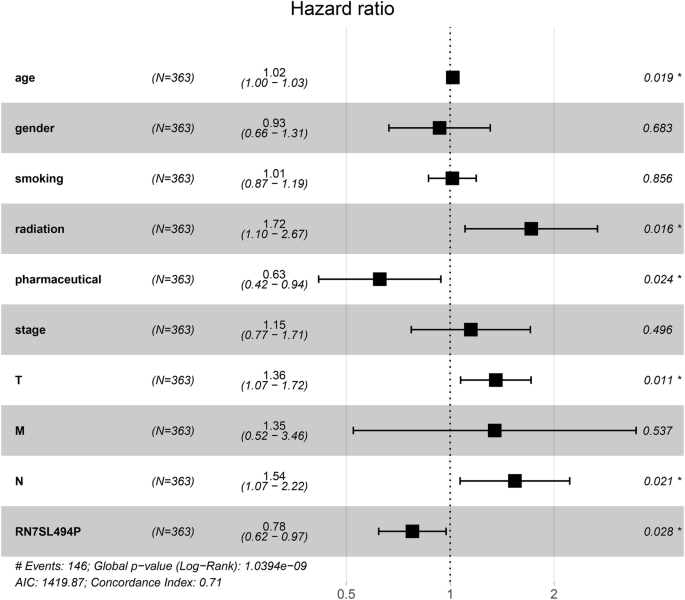
)。文献未提及具体实验产品,领域常规使用Cox回归分析软件(如R语言的survival包)。
3.4 CCLE数据集的独立验证与功能富集分析
实验目的是在独立数据集上验证RN7SL494P的功能,并分析其共表达基因的生物学通路,探索其潜在调控机制。方法细节为从CCLE数据库下载肺癌细胞系的RNA-seq数据,计算RN7SL494P的共表达基因(共表达系数阈值设为0.2),对筛选出的共表达基因进行GO及KEGG功能富集分析。结果解读显示,共筛选出30个上调共表达基因和30个下调共表达基因(
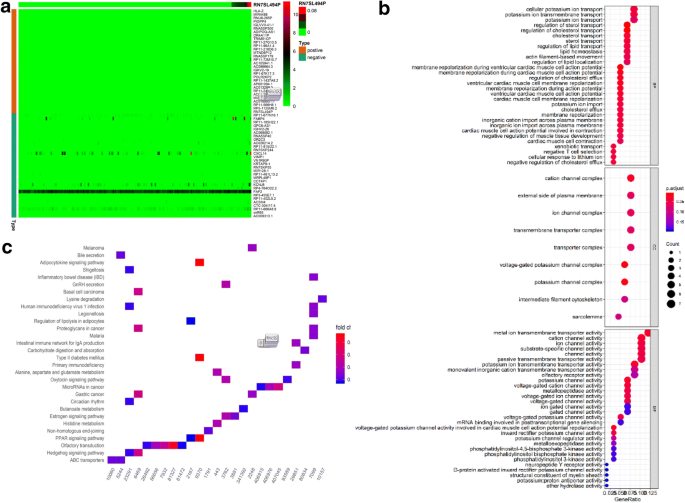
),GO分析显示这些基因显著富集于胆固醇与脂质转运、细胞膜转运功能等生物学过程;KEGG分析显示富集于ABC转运体、Hedgehog信号通路、PPAR信号通路及非同源末端连接等通路(P<0.05),提示RN7SL494P可能通过调控这些通路参与肺腺癌的发生发展与转移过程。文献未提及具体实验产品,领域常规使用功能富集分析工具(如DAVID、clusterProfiler)。
4. Biomarker研究及发现成果解析
本研究鉴定的Biomarker为长链非编码RNA假基因RN7SL494P,其筛选与验证逻辑形成了完整链条:首先通过TCGA数据库的差异基因筛选锁定候选基因,随后通过淋巴结转移梯度变化分析确认其与转移的关联,再通过生存分析关联患者预后,经Cox回归验证其独立预后价值,最后通过CCLE数据集进行独立验证,确保结论的可靠性。
该Biomarker来源于TCGA数据库中515例肺腺癌患者的肿瘤组织转录组数据,验证方法包括Kruskal-Wallis检验分析表达梯度变化、Kaplan-Meier生存分析、Cox回归模型验证,以及CCLE细胞系数据集的共表达分析。文献未明确提供ROC曲线的特异性与敏感性数据,但生存分析显示RN7SL494P高表达组患者生存率为41.80%,低表达组为39.70%(

),Cox回归分析显示其作为预后标志物的风险比HR=0.78(P=0.028)。
核心成果方面,RN7SL494P是首个被发现同时关联肺腺癌淋巴结转移和患者预后的长链非编码RNA假基因,其高表达可显著降低患者死亡风险,兼具转移预测与预后评估的双重功能,创新性在于突破了现有研究单一维度的局限,建立了“梯度变化-生存分析-独立验证”的标志物筛选体系。推测:RN7SL494P可能通过调控脂质转运、Hedgehog等信号通路影响肺腺癌的转移过程,需进一步通过细胞实验与动物实验验证其具体功能与机制。
