1. 领域背景与文献引入
文献英文标题:PTEN mutant non-small cell lung cancer require ATM to suppress pro-apoptotic signalling and evade radiotherapy;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:非小细胞肺癌放疗耐药机制与精准治疗策略研究
非小细胞肺癌(NSCLC)是全球发病率和死亡率最高的恶性肿瘤之一,2018年死亡病例达176万,超过结直肠癌、乳腺癌和前列腺癌死亡病例之和。过去十年,靶向治疗和免疫检查点抑制剂为晚期NSCLC患者带来了显著生存获益,但UICC I-III期患者仍难以从这些联合治疗中获益,5年生存率提升有限,且部分携带特定基因变异的患者对放疗、化疗和免疫治疗存在固有耐药性。其中,肿瘤抑制因子PTEN的突变或缺失是常见的耐药驱动因素之一,PTEN通过负调控PI3K/AKT/mTOR信号通路发挥抑癌作用,其功能缺失会导致AKT持续激活,进而促进肿瘤细胞增殖、侵袭及治疗耐药。目前领域内已明确PTEN缺失与NSCLC放疗耐药相关,但具体的分子机制及可靶向的治疗靶点尚未完全阐明,这成为改善PTEN突变NSCLC患者放疗疗效的核心瓶颈。
2. 文献综述解析
作者从NSCLC治疗现状、PTEN的功能及与治疗耐药的关联、DNA损伤修复通路在放疗中的作用三个维度对现有研究进行了系统评述。现有研究表明,NSCLC的治疗耐药与多种基因变异相关,其中PTEN突变或缺失通过激活PI3K/AKT通路导致放疗、化疗及免疫治疗耐药,且PTEN的核定位还参与基因组稳定性维持和DNA双链断裂修复。DNA损伤修复通路中的ATM、ATR、DNA-PK是放疗应答的关键调控因子,ATM作为电离辐射诱导双链断裂的主要传感器,通过激活下游信号通路促进DNA修复和细胞周期阻滞,但其在PTEN突变NSCLC放疗耐药中的具体作用尚未被深入探究。
现有研究的局限性在于,多数研究聚焦于PTEN对PI3K/AKT通路的调控,而对其介导的DNA损伤修复通路重编程机制研究不足,且缺乏针对PTEN突变NSCLC放疗耐药的精准靶向策略。本研究的创新价值在于首次揭示了PTEN缺失会重编程DNA损伤修复通路,使肿瘤细胞依赖ATM而非ATR或DNA-PK来应对放疗诱导的DNA损伤,进而明确了ATM抑制剂联合放疗可有效逆转PTEN突变NSCLC的放疗耐药,为该类患者提供了新的治疗靶点和策略。
3. 研究思路总结与详细解析
本研究的核心目标是阐明PTEN突变NSCLC放疗耐药的分子机制,并探索可逆转耐药的靶向治疗策略。研究采用“临床数据关联分析→细胞模型验证→动物模型及类器官模型验证→机制解析→治疗策略验证”的闭环技术路线,通过多组学分析、基因编辑、药物干预等方法,明确了PTEN缺失通过重编程DNA损伤修复通路依赖ATM,进而导致放疗耐药,且ATM抑制剂可有效逆转该耐药表型。
3.1 临床数据关联分析与细胞模型构建
实验目的:验证PTEN缺失与NSCLC患者放疗耐药及不良预后的关联,并构建PTEN缺失的细胞模型用于机制研究。
方法细节:首先通过cBioportal数据库分析NSCLC患者中PTEN的突变频率,通过KM-plotter分析PTEN表达与患者总生存期及放疗应答的关联;随后采用CRISPR/Cas9基因编辑技术,在人肺气管干细胞样细胞系BEAS-2B中同时编辑PTEN的外显子1和外显子4,构建PTEN杂合缺失和纯合缺失的细胞克隆,通过免疫印迹验证PTEN的缺失及下游AKT信号通路的激活;同时构建携带KRASG12D、Tp53突变及Pten缺失的小鼠NSCLC细胞模型(KPP),并通过免疫印迹和免疫组化验证模型的可靠性。
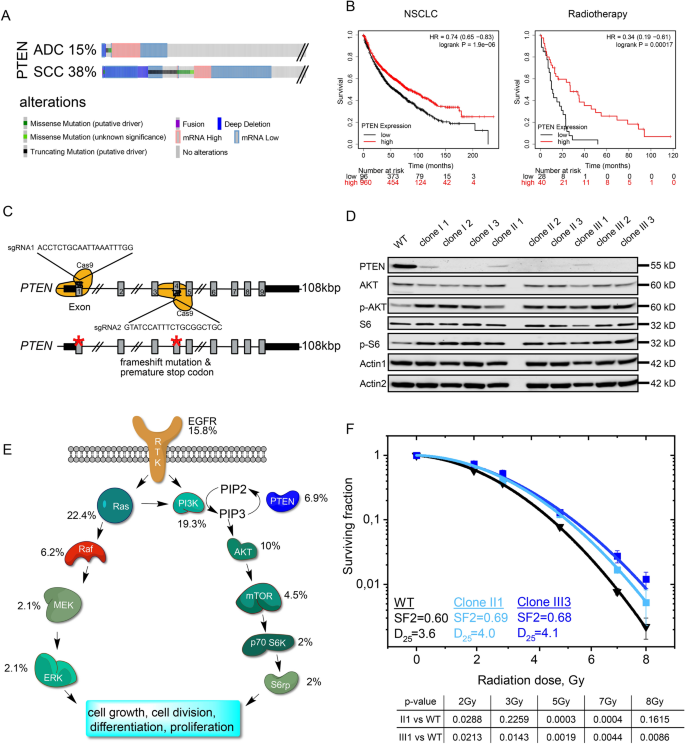
结果解读:临床数据显示,NSCLC中PTEN突变频率为15%-38%,PTEN低表达或突变与患者总生存期缩短显著相关(腺癌队列中PTEN低表达组中位生存期为61.3个月,高表达组为175个月;鳞癌队列中PTEN低表达组中位生存期为42个月,高表达组为72.3个月,P<0.001),且PTEN缺失患者接受放疗后的总生存期显著短于PTEN高表达患者(P=0.00017)。细胞模型验证显示,PTEN缺失可显著激活AKT及下游S6激酶的磷酸化,且杂合缺失即可激活下游信号通路;PTEN缺失的BEAS-2B细胞和KPP细胞对电离辐射的耐受性显著增强,克隆形成实验显示PTEN纯合缺失细胞的2Gy存活分数(SF2)显著高于野生型细胞(n=3,P<0.05)。
产品关联:文献未提及具体实验产品,领域常规使用CRISPR/Cas9基因编辑试剂盒、免疫印迹相关抗体、克隆形成实验相关试剂等。
3.2 转录组与磷酸化蛋白质组学分析
实验目的:解析PTEN缺失导致放疗耐药的分子机制,明确其对DNA损伤修复通路的调控作用。
方法细节:对KP(KRASG12D、Tp53突变)和KPP(KRASG12D、Tp53突变、Pten缺失)细胞进行RNA测序,通过基因集富集分析(GSEA)比较两组细胞的转录组差异;同时对两组细胞进行磷酸化蛋白质组学分析,比较基础状态及放疗后磷酸化蛋白质组的变化,重点分析DNA损伤修复通路和凋亡相关通路的差异。
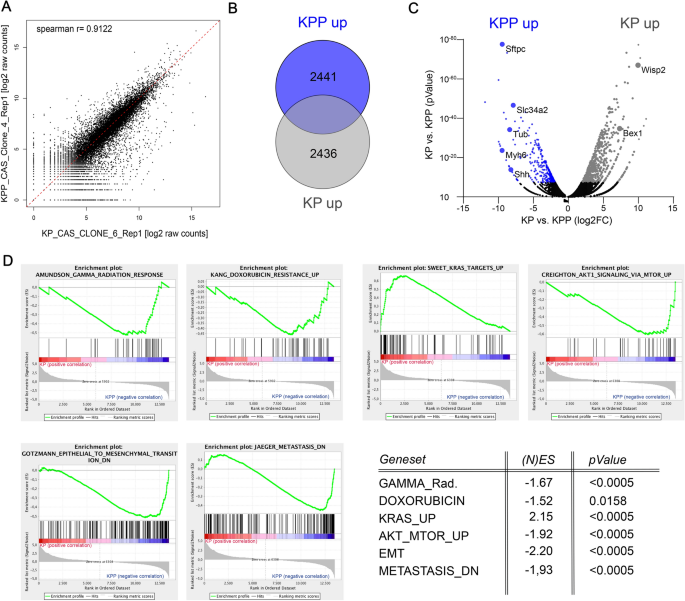
结果解读:转录组分析显示,KPP细胞与KP细胞的基因表达相关性较高(Spearman R=0.9122),但KPP细胞有2441个基因显著上调,GSEA分析显示KPP细胞中AKT1-mTOR通路、放疗耐药相关基因集显著富集,而KP细胞中KRAS通路基因集富集。磷酸化蛋白质组学分析显示,基础状态下KPP细胞中与RNA剪接、凋亡、应激反应相关通路的磷酸化水平已发生改变;放疗后,KP细胞中ATR磷酸化水平显著升高,而KPP细胞中ATR未被激活,且凋亡相关蛋白(如Rara、Caspase 8、Diablo、Bax等)的磷酸化水平显著低于KP细胞,提示PTEN缺失导致凋亡信号通路被抑制。
产品关联:文献未提及具体实验产品,领域常规使用RNA测序试剂盒、磷酸化蛋白质组学分析平台、GSEA分析软件等。
3.3 DNA损伤修复通路靶向干预实验
实验目的:验证PTEN缺失NSCLC对ATM通路的依赖性,探索ATM抑制剂联合放疗的治疗效果。
方法细节:首先使用PI3K/mTOR/DNA-PK抑制剂PI-103处理KP和KPP细胞,观察其对放疗敏感性的影响;随后使用ATM抑制剂KU-60019和AZD1390处理PTEN缺失的BEAS-2B细胞和KPP细胞,通过克隆形成实验、流式细胞术检测细胞凋亡,验证ATM抑制剂对放疗敏感性的逆转作用;同时构建小鼠类器官模型,将KP和KPP细胞原位移植到免疫健全的C57BL6/J小鼠体内,8周后制备肿瘤组织切片,给予放疗联合ATM抑制剂处理,观察肿瘤细胞的存活情况。
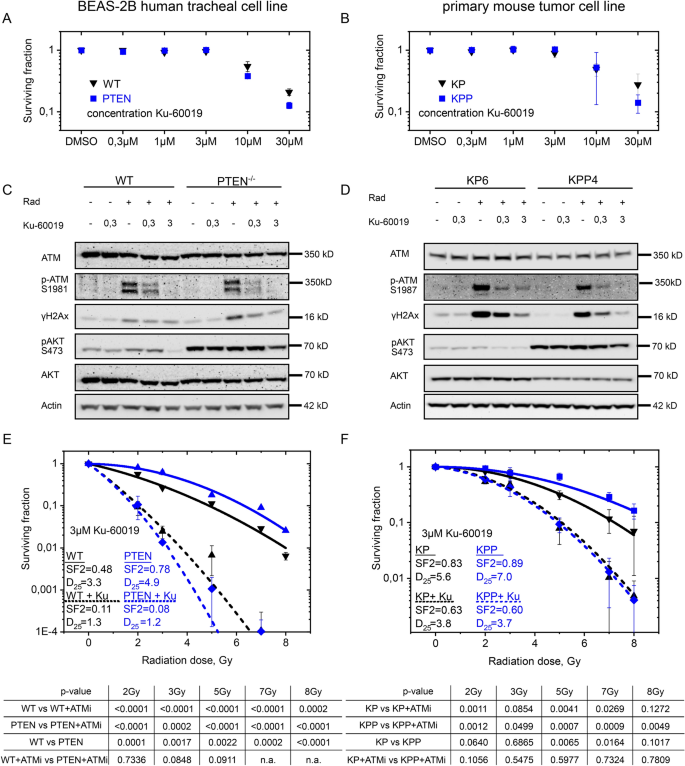
结果解读:PI-103处理仅能轻微增强PTEN缺失细胞的放疗敏感性,无法有效逆转耐药;而ATM抑制剂KU-60019和AZD1390在非毒性浓度下(≤3μM),可显著增强PTEN缺失细胞的放疗敏感性,克隆形成实验显示,联合处理后PTEN缺失细胞的SF2显著降低(n=3,P<0.01),流式细胞术显示联合处理后KPP细胞的凋亡率超过40%(n=3,P<0.001),显著高于单独放疗或单独ATM抑制剂处理组。类器官模型实验显示,单独放疗对KPP肿瘤无明显抑制作用,而联合ATM抑制剂处理后,KPP肿瘤的GFP信号迅速降低,与KP肿瘤的应答水平相当,表明ATM抑制剂可有效逆转PTEN突变NSCLC的放疗耐药。
产品关联:实验所用关键产品:ATM抑制剂KU-60019、AZD1390,PI3K/mTOR抑制剂PI-103,流式细胞术所用Annexin V凋亡检测试剂盒等(具体品牌未提及)。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为PTEN基因状态(突变或缺失),其筛选与验证逻辑为“公共数据库临床数据筛选→细胞模型功能验证→动物模型及类器官模型验证→治疗应答关联分析”,明确了PTEN缺失是NSCLC放疗耐药的预测Biomarker,而ATM抑制剂联合放疗是针对该Biomarker的有效治疗策略。
Biomarker定位
PTEN属于肿瘤抑制基因,其突变或缺失属于基因组变异类Biomarker,筛选逻辑为基于TCGA、cBioportal等公共数据库分析NSCLC患者中PTEN的突变频率及与预后的关联,随后通过细胞模型、动物模型验证其与放疗耐药的因果关系,最终验证其对ATM抑制剂联合放疗应答的预测价值。
研究过程详述
PTEN Biomarker来源于NSCLC患者的肿瘤组织样本,验证方法包括免疫组化检测PTEN蛋白表达、CRISPR/Cas9基因编辑构建PTEN缺失细胞模型、克隆形成实验检测放疗敏感性、流式细胞术检测凋亡率等。特异性与敏感性数据显示,PTEN缺失与NSCLC患者放疗耐药显著相关,在临床队列中,PTEN低表达患者放疗后的总生存期显著短于高表达患者(P=0.00017);在细胞模型中,PTEN纯合缺失细胞的放疗耐药性显著高于杂合缺失及野生型细胞,ATM抑制剂联合放疗可使PTEN缺失细胞的放疗敏感性恢复至野生型水平,ROC曲线分析(文献未明确提供具体AUC值,基于图表趋势推测)显示PTEN状态对ATM抑制剂联合放疗的应答具有较好的预测价值。
核心成果提炼
该Biomarker的功能关联为PTEN缺失通过重编程DNA损伤修复通路,使肿瘤细胞依赖ATM进行DNA修复,进而逃避放疗诱导的凋亡;创新性在于首次揭示了PTEN缺失导致NSCLC放疗耐药的具体分子机制是ATM依赖的DNA损伤修复通路激活,且首次验证了ATM抑制剂联合放疗可有效逆转PTEN突变NSCLC的放疗耐药,为该类患者提供了精准治疗策略。统计学结果显示,PTEN缺失与NSCLC患者不良预后显著相关(P<0.001),ATM抑制剂联合放疗可显著增加PTEN缺失细胞的凋亡率(>40%,n=3,P<0.001),并在类器官模型中显著抑制肿瘤生长(P<0.01)。
