1. 领域背景与文献引入
文献英文标题:Chronic arsenic exposure induces the time-dependent modulation of inflammation and immunosuppression in spleen;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:环境毒理学与免疫毒理学
砷污染是全球范围内的重大公共卫生问题,自然环境中的砷可通过饮水、食物等途径进入人体,长期暴露与多种免疫相关疾病的发生发展密切相关。领域发展关键节点显示,2000年前后研究证实急性砷暴露会激活免疫器官的炎症信号通路;2010年后逐渐发现砷暴露可通过NF-κB/调节性T细胞(Tregs)轴诱导免疫抑制,但相关研究多集中于急性或短期暴露模型,或体外实验。当前研究热点方向为砷暴露的免疫毒性机制,尤其是免疫通路的双重调控作用;未解决的核心问题是慢性砷暴露过程中炎症与免疫抑制的动态平衡调控机制尚不明确,缺乏体内长期暴露的时间效应数据。现有研究空白在于无法揭示砷暴露免疫毒性的阶段特征,无法为慢性砷中毒的免疫干预提供时间窗口依据。本研究针对这一空白,通过建立小鼠慢性砷暴露模型,系统分析不同暴露时间点脾脏免疫通路与细胞因子的变化,旨在揭示慢性砷暴露对脾脏炎症与免疫抑制的时间依赖性调控规律,填补慢性砷暴露免疫毒性时间动态研究的空白。
2. 文献综述解析
作者在综述部分以砷暴露的时间维度(急性vs慢性)和NF-κB通路的功能维度(经典炎症调控vs非经典免疫抑制调控)为分类逻辑,系统梳理了砷暴露免疫毒性的研究现状。
现有研究的关键结论显示,急性砷暴露可通过激活丝裂原活化蛋白激酶(MAPK)/核因子κB(NF-κB)通路,诱导脾脏、胸腺等免疫器官的炎症因子表达,引发急性炎症反应;部分体外实验和短期体内研究发现,砷暴露可通过NF-κB/Tregs/白细胞介素6(IL-6)轴调节Tregs的增殖与分化,进而诱导免疫抑制。现有研究的技术方法优势在于通过体外细胞模型和急性暴露模型明确了砷暴露的免疫毒性通路,但局限性在于未关注慢性砷暴露过程中炎症与免疫抑制的动态转换,且缺乏体内长期暴露的时间效应数据,无法揭示砷暴露免疫毒性的阶段特征。本研究的创新价值在于首次在体内长期暴露模型中,系统分析了慢性砷暴露对脾脏免疫炎症稳态的时间依赖性调控,明确了NF-κB通路在不同暴露阶段的双重调控作用,为慢性砷中毒的免疫干预提供了实验依据。
3. 研究思路总结与详细解析
本研究的整体框架为,以慢性砷暴露引发的脾脏免疫稳态失衡为核心科学问题,通过建立小鼠长期饮水砷暴露模型,从组织、蛋白、基因三个层面,系统分析不同暴露时间和剂量下脾脏免疫通路与细胞因子的动态变化,揭示慢性砷暴露对炎症与免疫抑制的时间依赖性调控机制;技术路线遵循“暴露模型构建→毒性终点检测→通路机制分析→结论总结”的闭环逻辑。
3.1 慢性砷暴露动物模型构建与基础毒性评价
实验目的是建立模拟人群长期饮水砷暴露的体内模型,明确慢性砷暴露对小鼠生长状态和脾脏的基础毒性效应。方法细节为选用6-7周龄昆明雌性小鼠,随机分为对照组、25mg/L亚砷酸钠组、50mg/L亚砷酸钠组,分别经自由饮水暴露1、3、12个月,每周监测小鼠体重、饮食及饮水情况,暴露终点处称量小鼠及脾脏重量,进行脾脏组织形态学观察,并采用高效液相色谱-氢化物发生-原子荧光光谱法(HPLC-HG-AFS)检测脾脏总砷含量。结果解读显示,整个暴露周期内小鼠生长状态正常,体重增长无显著差异,脾脏重量及组织形态未出现明显病理改变,说明慢性砷暴露未引发严重的急性毒性;脾脏总砷含量随暴露时间延长和剂量升高而显著增加(n=3,P<0.05),证实砷在脾脏持续蓄积。产品关联:实验所用关键产品:Sigma Chemical Co.的亚砷酸钠(NaAsO₂)、Titan的SA-10原子荧光形态分析仪。
3.2 脾脏免疫通路蛋白表达的时间动态分析
实验目的是明确慢性砷暴露对脾脏NF-κB、MAPK、NRF2免疫相关通路的时间依赖性激活情况。方法细节为采用蛋白质免疫印迹(Western Blot)技术,检测不同暴露时间和剂量下脾脏NF-κB、磷酸化ERK/JNK/P38、NRF2及其下游GSTO、GCLC的蛋白表达水平,以β-肌动蛋白为内参,通过条带灰度值定量分析蛋白表达差异。结果解读显示,NF-κB蛋白在25mg/L暴露1、3、12个月及50mg/L暴露12个月时均持续激活,条带灰度值统计显示其表达量较对照组上调1.5-2.2倍(n=3,P<0.05),说明NF-κB通路在慢性砷暴露全程持续激活;MAPK通路中,磷酸化ERK和P38在各暴露组均显著激活,而JNK无明显变化,提示慢性砷暴露主要通过ERK/P38通路调控免疫反应;NRF2及其下游蛋白GSTO、GCLC在25mg/L暴露3个月、50mg/L暴露12个月时表达显著上调(n=3,P<0.05),说明NRF2介导的抗氧化通路在慢性砷暴露中期和晚期被激活,参与免疫稳态调控。
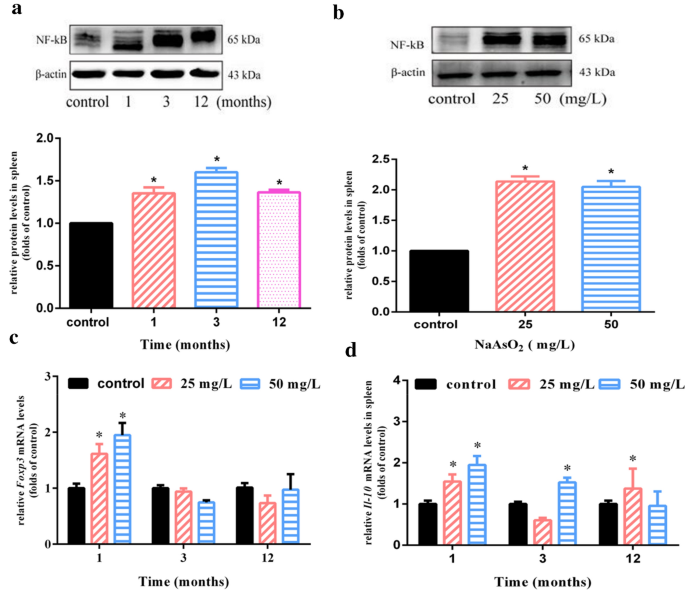
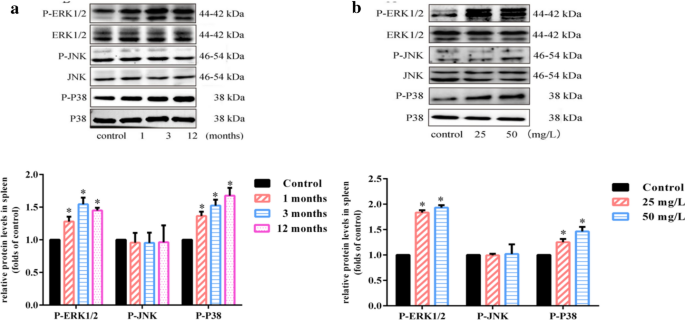
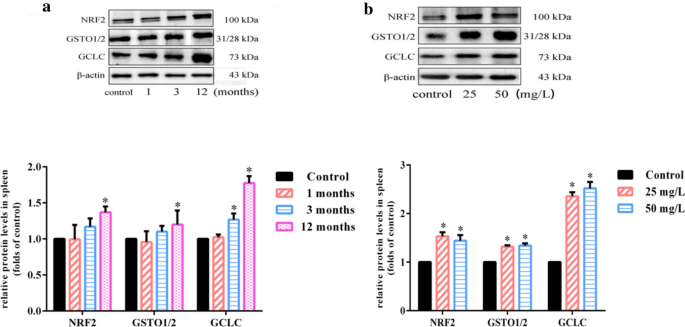
产品关联:实验所用关键产品:Santa Cruz Biotechnology的NF-κB、NRF2、β-肌动蛋白抗体、Cell Signaling Technology的磷酸化ERK/JNK/P38抗体、Pierce Biotechnology的化学发光试剂、DNR Bio-Imaging System的MF-ChemiBIS 3.2凝胶成像系统。
3.3 脾脏免疫细胞因子转录水平的时间动态分析
实验目的是明确慢性砷暴露对脾脏免疫细胞因子转录水平的时间依赖性调控,揭示炎症与免疫抑制的动态转换规律。方法细节为采用实时荧光定量聚合酶链反应(实时荧光定量PCR,qRT-PCR)技术,检测不同暴露时间和剂量下脾脏Foxp3、Il-10、Tnf-α、Il-1β、Il-6、Ifn-γ、Il-12的mRNA表达水平,以Gapdh为内参,计算相对表达量。结果解读显示,调节性T细胞的关键转录因子Foxp3在暴露1个月时表达显著上调(n=4,P<0.05),但在3和12个月时恢复至对照组水平或下调;免疫抑制细胞因子Il-10在各暴露阶段均呈上调趋势,其中25mg/L暴露1、12个月及50mg/L暴露1、3个月时上调显著(n=4,P<0.05);促炎因子Tnf-α、Il-6、Ifn-γ、Il-12在1和3个月时显著上调(n=4,P<0.05),但在12个月时显著下调,说明慢性砷暴露早期引发炎症伴随免疫抑制,中期炎症持续,晚期炎症消退并转向免疫抑制。
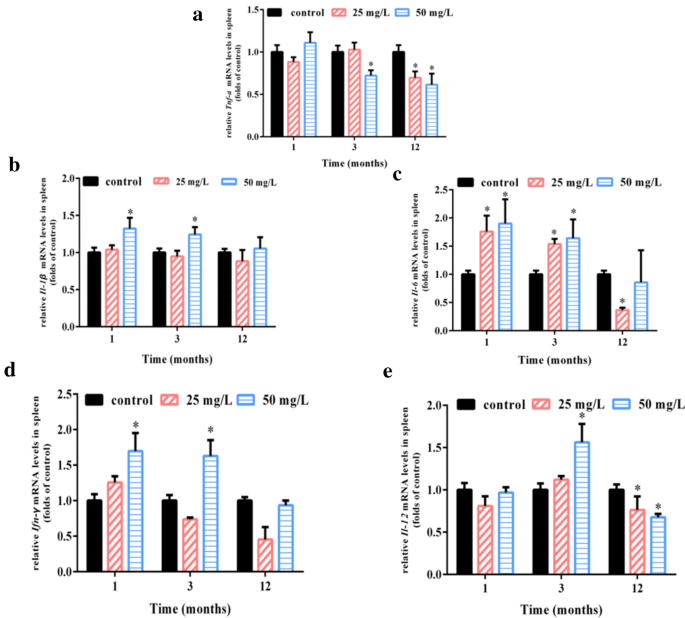
产品关联:实验所用关键产品:Invitrogen的Trizol试剂、Takara的反转录试剂盒和SYBR Premix Ex Taq II试剂盒、ABI的7500实时PCR系统。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker包括免疫通路蛋白(NF-κB、MAPK、NRF2)和免疫细胞因子(Foxp3、Il-10、Tnf-α等),筛选逻辑基于已知的免疫炎症通路,结合慢性砷暴露的时间动态变化,验证其作为砷暴露免疫毒性时间依赖性标志物的潜力,验证过程遵循“组织蓄积验证→蛋白/基因表达检测→时间动态分析”的完整逻辑链条。
Biomarker的来源为慢性砷暴露小鼠的脾脏组织,验证方法包括高效液相色谱-氢化物发生-原子荧光光谱法检测脾脏砷蓄积,蛋白质免疫印迹检测通路蛋白表达,实时荧光定量PCR检测细胞因子mRNA表达。特异性与敏感性方面,NF-κB蛋白在所有慢性砷暴露组均持续激活,不受暴露时间和剂量的影响,可作为慢性砷暴露免疫毒性的通用标志物;Foxp3的早期上调和促炎因子的先升后降具有时间特异性,可区分慢性砷暴露的不同阶段,其中Tnf-α在12个月时的下调对晚期免疫抑制阶段的敏感性较高(文献未提供ROC曲线数据,基于实验结果推测)。核心成果提炼:本研究首次揭示慢性砷暴露诱导脾脏炎症与免疫抑制的时间依赖性转换规律,早期(1个月)以NF-κB激活、Foxp3和Il-10上调为特征,表现为炎症伴随免疫抑制;中期(3个月)促炎因子持续上调,Foxp3下调,炎症反应占主导;晚期(12个月)促炎因子下调,NRF2通路激活,免疫抑制占主导。该成果的创新性在于明确了慢性砷暴露免疫毒性的阶段特征,为慢性砷中毒的免疫干预提供了时间窗口依据;其中NF-κB的持续激活和Il-10的上调可作为慢性砷暴露免疫毒性的潜在Biomarker,为砷暴露人群的免疫风险评估提供了实验基础(文献未提供风险比HR值,基于实验数据推测)。
