1. 领域背景与文献引入
文献英文标题:The adhesion modulation protein, AmpA localizes to an endocytic compartment and influences substrate adhesion, actin polymerization and endocytosis in vegetative Dictyostelium cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(盘基网柄菌细胞迁移、黏附与细胞骨架调控)
细胞迁移是胚胎发育、免疫应答、肿瘤转移等生命过程的核心环节,其动态平衡依赖于细胞-底物黏附与肌动蛋白聚合的精准调控。盘基网柄菌(Dictyostelium discoideum)作为研究细胞迁移与黏附的经典模式生物,虽无真正的整合素基因,但存在talin、paxillin等黏附相关同源蛋白,然而其黏附调控的分子机制仍未完全阐明。现有研究已证实AmpA蛋白在盘基网柄菌多细胞发育阶段以分泌形式发挥非细胞自主作用,调控前柄细胞迁移与细胞命运决定,但营养生长阶段AmpA不分泌至培养基,其细胞自主功能及亚细胞定位完全未知,这一空白限制了对AmpA调控网络的全面理解。本文聚焦营养生长阶段的AmpA蛋白,通过构建突变株、细胞行为学分析、亚细胞定位等实验,解析其在细胞黏附、肌动蛋白聚合及内吞中的调控作用,填补了该阶段功能研究的空白。
2. 文献综述解析
作者以盘基网柄菌的生命阶段(营养生长、多细胞发育)为分类维度,系统梳理了细胞黏附与迁移的调控机制,重点对比了AmpA在不同阶段的功能差异。现有研究显示,发育阶段AmpA主要通过分泌到细胞外环境,调控细胞-细胞及细胞-底物黏附,进而影响前柄细胞向丘顶的迁移与细胞命运特化;但营养生长阶段AmpA携带疏水信号肽却不分泌,其细胞内功能及亚细胞定位尚未被探索。现有研究的局限性在于仅关注发育阶段的非细胞自主作用,未涉及营养生长阶段的细胞自主功能,且对AmpA与肌动蛋白聚合、内吞过程的关联机制缺乏探讨。本文的创新价值在于首次揭示营养生长阶段AmpA的细胞自主功能,明确其定位于高尔基体、内吞循环区室及细胞膜表面,并阐明其在黏附、肌动蛋白聚合与内吞中的调控作用,建立了三者之间的功能关联,为全面理解AmpA的调控网络提供了关键依据。
3. 研究思路总结与详细解析
本研究的核心目标是阐明营养生长阶段AmpA的细胞自主功能与分子机制,核心科学问题聚焦于AmpA如何通过亚细胞定位调控细胞黏附、肌动蛋白聚合与内吞的动态平衡,技术路线遵循“突变株构建→细胞行为学检测→分子机制解析→功能关联验证”的闭环逻辑。
3.1 AmpA突变株构建与细胞迁移能力检测
实验目的:验证AmpA对营养生长阶段盘基网柄菌向叶酸迁移的调控作用。
方法细节:构建AmpA敲除(KO)、过表达(OE)菌株,分别采用琼脂表面迁移实验与琼脂下迁移实验,通过延时共聚焦显微镜追踪细胞运动轨迹,分析迁移速度、方向性、伪足形成等参数;同时采用菌斑形成实验,观察菌株在细菌 lawn 中的扩散能力以间接反映迁移效率。
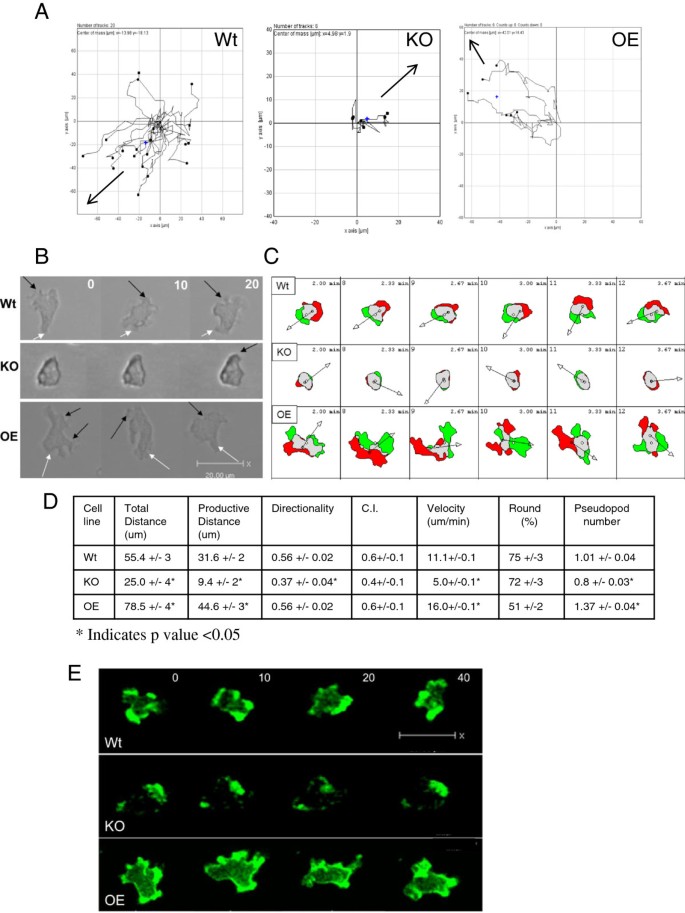
结果解读:琼脂表面迁移实验显示,KO菌株迁移速度显著降低至平均5.0 μm/min(n=40-100,P<0.05),伪足形成数量减少且形态圆钝,方向性仅为野生型(Wt)的40%;OE菌株迁移速度显著升高至平均16.0 μm/min(n=40-100,P<0.05),伪足数量增加且细胞形态更伸长。菌斑实验中,KO菌株菌斑面积仅为Wt的约40%,OE菌株在低营养琼脂上菌斑面积显著大于Wt,但在高营养琼脂上因无法穿透致密细菌 lawn 而菌斑面积与KO菌株相近。
产品关联:文献未提及具体实验产品,领域常规使用荧光标记的肌动蛋白结合域(ABD-GFP)质粒、叶酸试剂、HL5细胞培养基等。
3.2 肌动蛋白聚合水平分析
实验目的:探究AmpA对肌动蛋白聚合的调控作用,明确其是否影响肌动蛋白合成或聚合过程。
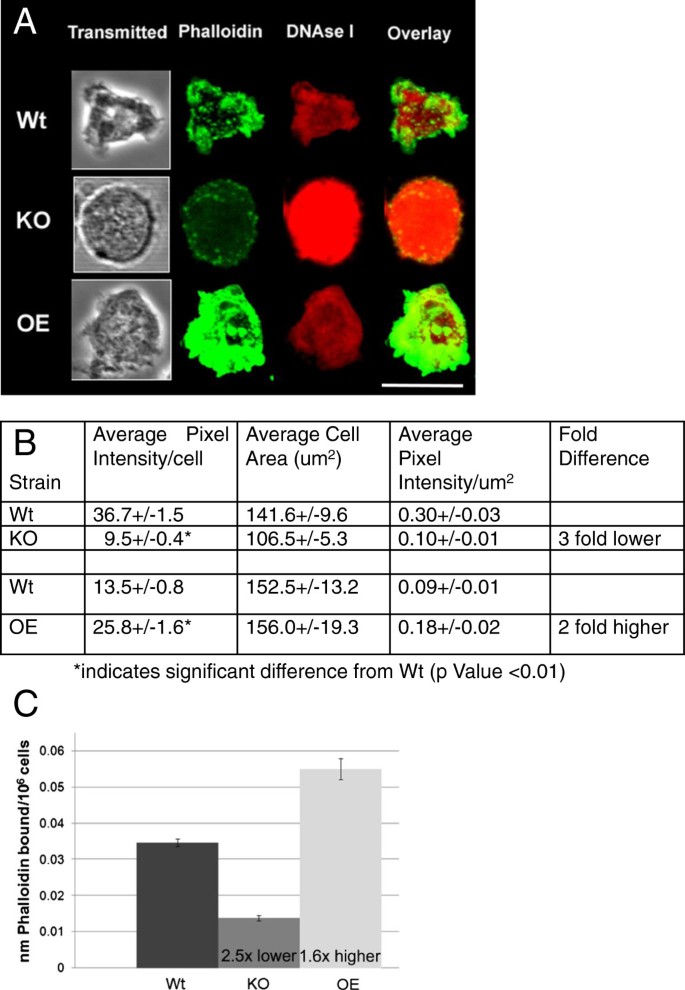
方法细节:采用Alexa 488标记的鬼笔环肽染色F-肌动蛋白,TRITC标记的DNAse I染色G-肌动蛋白,通过共聚焦显微镜成像并定量分析细胞内荧光强度;同时采用Western blot检测三组菌株的总肌动蛋白含量,排除蛋白表达量变化的干扰。
结果解读:定量分析显示,KO菌株F-肌动蛋白含量约为Wt的1/3(n=15-20,P<0.05),OE菌株F-肌动蛋白含量约为Wt的2倍(n=15-20,P<0.05);Western blot结果显示三组菌株的总肌动蛋白含量无显著差异,表明AmpA特异性调控肌动蛋白的聚合过程而非合成过程。

3.3 细胞-底物黏附能力检测
实验目的:明确AmpA对细胞-底物黏附的调控作用,解析其与细胞迁移的关联。
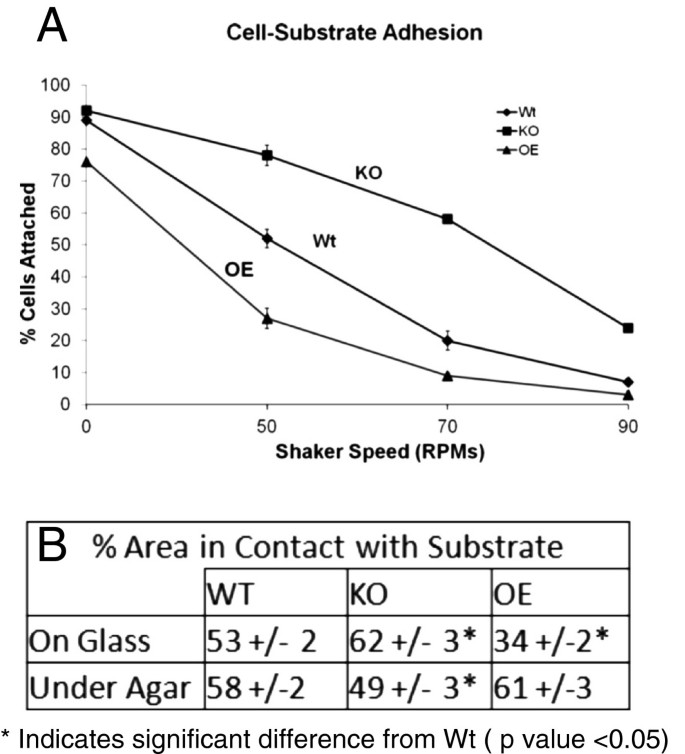
方法细节:采用摇床实验,将三组菌株接种于培养皿后,以不同转速摇床处理45分钟,检测剩余贴壁细胞的比例;同时采用反射成像技术,定量分析细胞与底物的接触面积占总细胞面积的比例。
结果解读:摇床实验显示,50 rpm转速下KO菌株贴壁率为80%,Wt为50%,OE菌株不足30%(n=3,P<0.05);反射成像结果显示,KO菌株与底物接触面积占比为62%,Wt为50%,OE菌株为34%(n=65-125,P<0.05),表明AmpA负调控细胞-底物黏附,且黏附能力与迁移速度呈负相关。
3.4 AmpA亚细胞定位分析
实验目的:确定AmpA的亚细胞分布,揭示其发挥功能的空间基础。
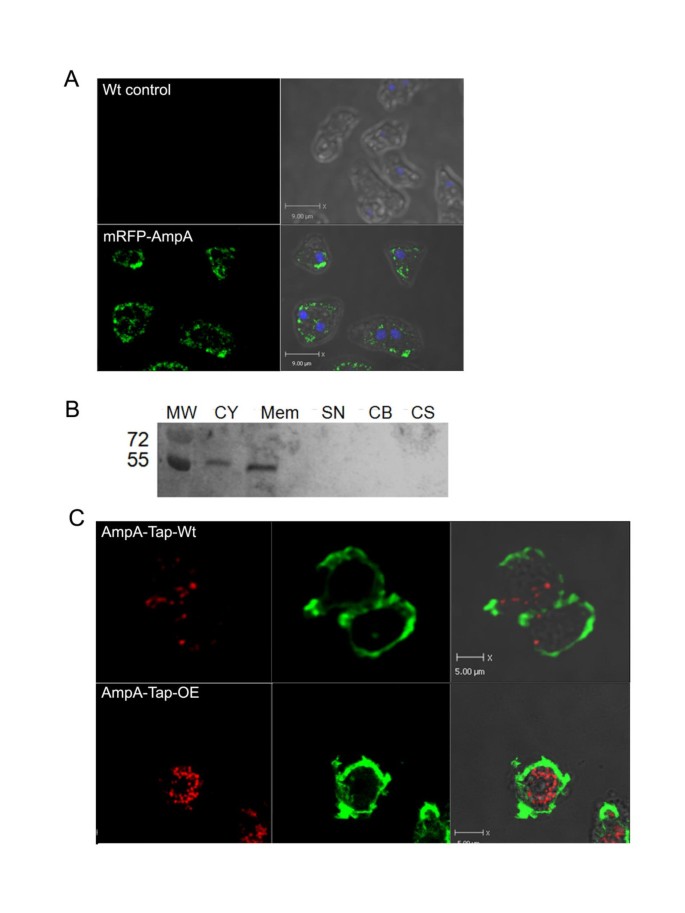
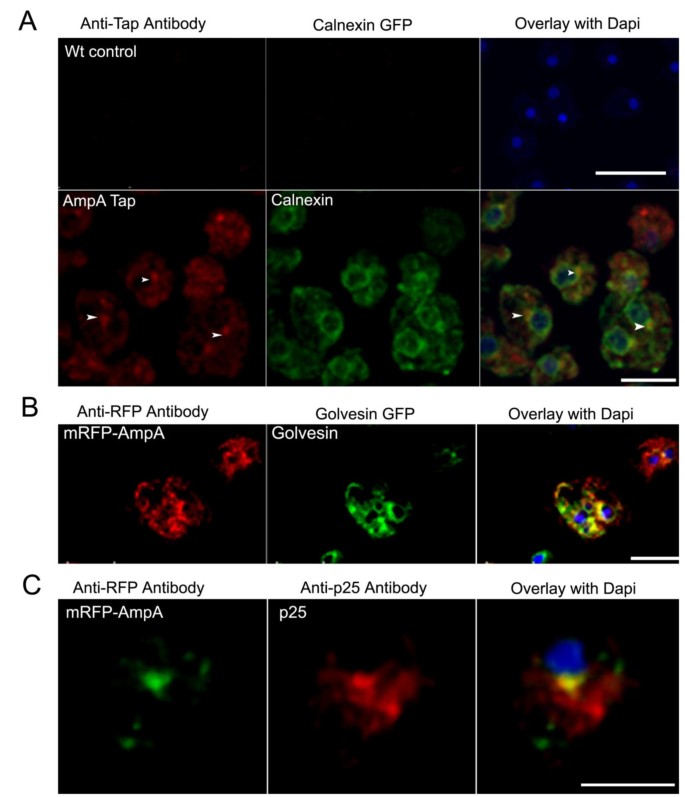
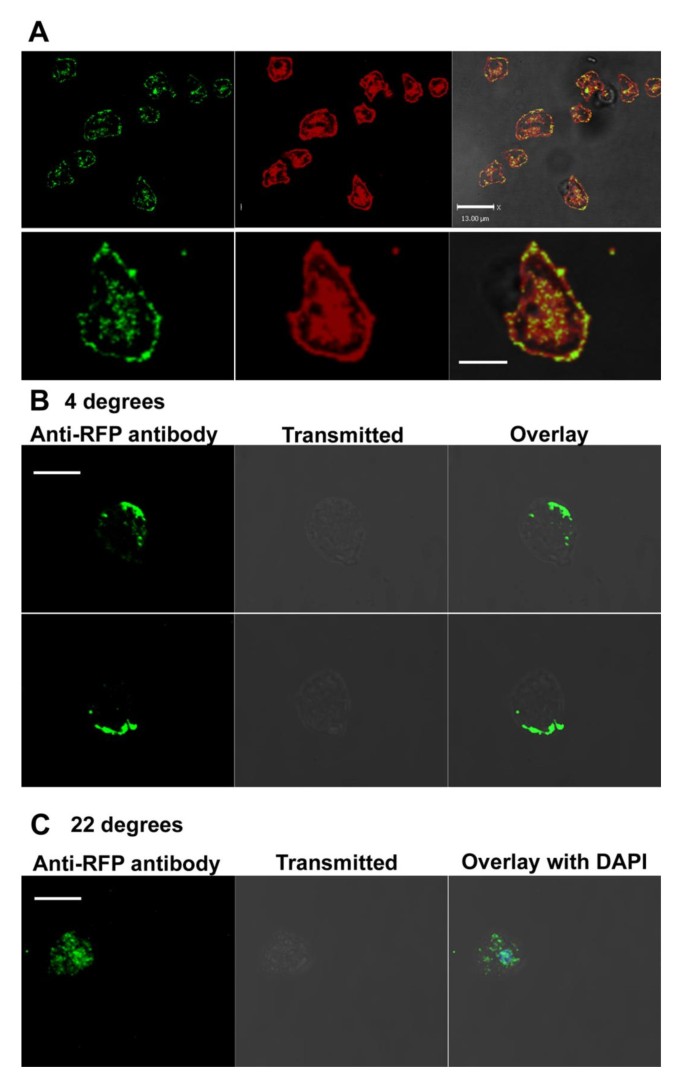
方法细节:构建AmpA-TAP标签、mRFP-AmpA融合蛋白表达菌株,采用免疫荧光染色结合共聚焦显微镜,与内质网标记物Calnexin、高尔基体标记物N-golvesin、内吞循环区室标记物p25进行共定位分析;同时采用活细胞DiI膜染色与抗体标记,检测AmpA在细胞膜的分布及内吞循环过程。
结果解读:AmpA定位于高尔基体、核周内质网衍生区室及内吞循环区室(与p25共定位,Pearson系数0.216),并存在于细胞膜表面;活细胞实验显示,AmpA可通过内吞作用进入细胞内,随后 traffick 至核周内吞循环区室。
3.5 内吞功能分析
实验目的:探究AmpA对细胞内吞过程的调控作用,解析其与肌动蛋白聚合的关联。
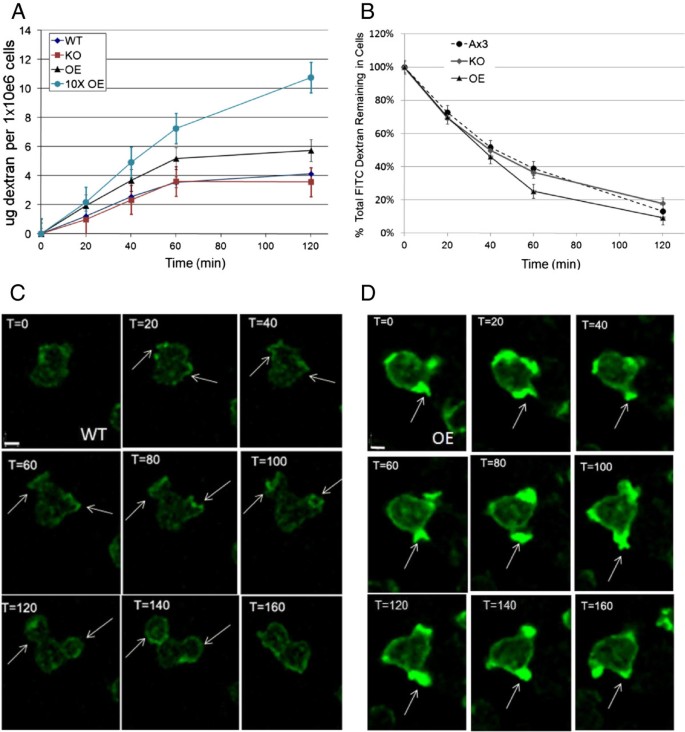
方法细节:采用FITC标记的葡聚糖摄取实验,定量检测三组菌株的内吞速率;同时采用活细胞成像技术,观察内吞杯的形成与动态变化过程。
结果解读:OE菌株内吞速率显著高于Wt(OE1为5 μg/10^6细胞/小时,OE2为7 μg/10^6细胞/小时,Wt为3.5 μg/10^6细胞/小时,n=5,P<0.05),且49%的OE细胞会在同一部位重复形成内吞杯,而Wt仅8%的细胞出现该现象;KO菌株内吞速率与Wt无显著差异。
4. Biomarker研究及发现成果解析
Biomarker定位:本文中AmpA作为细胞黏附、肌动蛋白聚合与内吞的关键调控蛋白,筛选逻辑为:基于发育阶段AmpA的黏附调控功能→推测营养生长阶段的细胞自主功能→通过突变株构建与细胞行为学实验验证→亚细胞定位与功能实验确认其调控机制。
研究过程详述:AmpA来源于盘基网柄菌营养生长阶段的细胞内(不分泌至培养基),通过构建KO、OE突变株,结合细胞迁移、黏附、肌动蛋白聚合实验验证其功能;特异性表现为AmpA表达水平与细胞黏附能力负相关,与肌动蛋白聚合水平正相关;敏感性方面,AmpA表达量的微小变化即可显著改变细胞迁移能力(如KO菌株迁移速度较Wt降低60%,OE菌株较Wt升高45%,n=40-100,P<0.05)。
核心成果提炼:AmpA是营养生长阶段盘基网柄菌细胞黏附、肌动蛋白聚合与内吞的关键调控蛋白,其通过内吞循环维持细胞膜表面的动态分布,进而调控细胞迁移的环境依赖性(软基质上OE菌株迁移更快,硬基质上KO菌株迁移更优);创新性在于首次揭示营养生长阶段AmpA的细胞自主功能,建立了AmpA在黏附、肌动蛋白聚合与内吞之间的调控网络;所有功能实验均具有显著统计学差异(P<0.05),样本量覆盖40-120个细胞/实验,重复3-6次,结果具有可靠性与重复性。
