1. 领域背景与文献引入
文献英文标题:Stringent requirement for spatial arrangement of extracellular matrix in supporting cell morphogenesis and differentiation;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞外基质生物学与干细胞组织工程交叉领域
细胞外基质(ECM)是构成细胞微环境的核心组成部分,其研究发展历经多个关键阶段:20世纪90年代明确整合素家族作为ECM细胞表面受体的核心作用,奠定了ECM-细胞互作的分子基础;2000年后,三维ECM模型的建立推动了对ECM组分浓度与细胞功能调控关系的研究;近年,ECM空间拓扑结构对干细胞命运的精准调控成为领域热点。当前研究的核心未解决问题在于,多数人工构建的ECM模型无法模拟体内天然ECM的精确空间排布,导致ECM空间结构对细胞功能的阈值调控效应及机制仍不明确,这一局限制约了组织工程支架的精准设计。本研究针对这一空白,利用天然牛跟腱的不同角度切片构建了组分一致但胶原纤维空间排布存在差异的细胞培养底物,系统探究了ECM空间排布对人间充质干细胞(MSCs)形态发生与分化的严格调控作用,为组织工程的支架设计提供了关键的实验依据。
2. 文献综述解析
作者将现有ECM研究分为“组分功能调控”“浓度效应”“空间结构影响”三个维度,系统评述了不同研究方向的进展与局限。
现有研究的关键结论显示,ECM的特定组分可精准调控细胞命运,例如乳腺来源ECM可影响乳腺上皮细胞的导管形成,特定ECM组合可诱导神经前体细胞向神经元或胶质细胞分化;技术方法上,人工ECM模型(如胶原凝胶、电纺纤维支架)可精准控制ECM的组分类型与浓度,便于开展分子机制研究,但这类模型的核心局限性在于无法模拟体内天然ECM的精确空间拓扑结构,难以揭示空间排布对细胞功能的阈值调控效应。本研究的创新价值在于,首次利用天然肌腱的不同角度切片构建了组分完全一致但空间排布存在梯度差异的ECM模型,通过系统对比不同空间结构下的细胞行为,明确了ECM空间排布的精确性对细胞形态与分化的严格要求,弥补了人工ECM模型的不足,为ECM空间生物学的研究提供了新的实验范式。
3. 研究思路总结与详细解析
本研究的核心目标是阐明ECM胶原纤维空间排布对MSCs形态发生与肌腱分化的调控作用,核心科学问题是ECM空间结构如何通过整合素-黏着斑通路调控细胞行为,技术路线遵循“天然ECM模型构建→细胞形态与黏着斑分析→分化标志物验证→机制推论”的闭环逻辑,通过多维度成像与定量分析系统揭示了ECM空间排布的阈值效应。
3.1 天然ECM模型构建与结构验证
实验目的为构建组分一致但胶原纤维空间排布存在梯度差异的细胞培养底物,并对比天然ECM与人工ECM的结构差异。方法细节上,研究人员选取牛跟腱组织,沿与肌腱主轴线呈0°、12°、20°、30°、45°、75°、90°的不同角度制备25μm厚的冷冻切片,同时制备人工自组装I型胶原凝胶的冷冻切片作为对照;利用二次谐波生成(SHG)显微镜、微分干涉差(DIC)显微镜、扫描电子显微镜(SEM)对不同底物的胶原纤维结构进行观察与定量分析。结果解读显示,SHG显微镜成像表明,0°跟腱切片中的胶原纤维呈长程平行紧密排列,而人工胶原凝胶中的胶原纤维短且排列无规则,仅形成局部有序的纤维束(图1);不同角度跟腱切片的胶原纤维片段长度随切割角度增大而逐渐缩短,0°切片中纤维片段最长,90°切片中则呈现胶原纤维的圆形横截面(图2、3),定量统计显示不同角度组的纤维片段长度存在显著差异(P<0.05,n=3),证明该方法可精准构建空间结构梯度差异的天然ECM模型。产品关联:实验所用关键产品:Leica Jung CM 1500冷冻切片机、FEI/Philips XL30环境扫描电子显微镜、Leica TCS SP5激光扫描共聚焦显微镜;抗体包括兔抗肌腱调蛋白(Santa Cruz,货号SC-98875)、小鼠抗纽蛋白(Millipore,货号MAB3574)等。
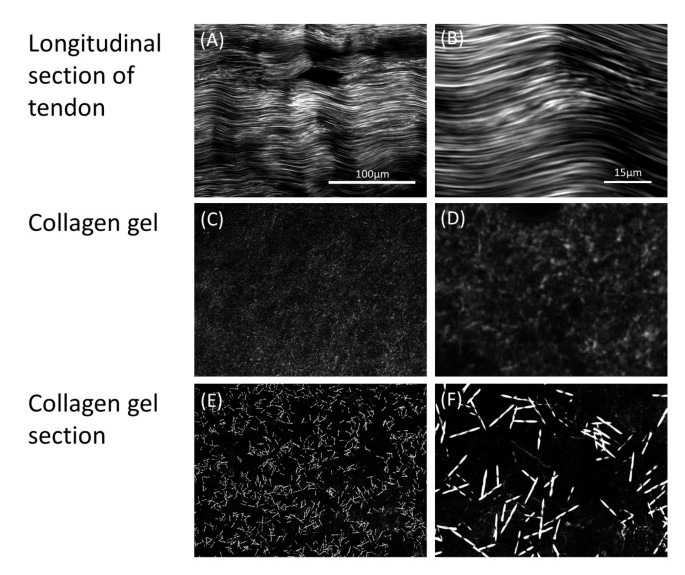
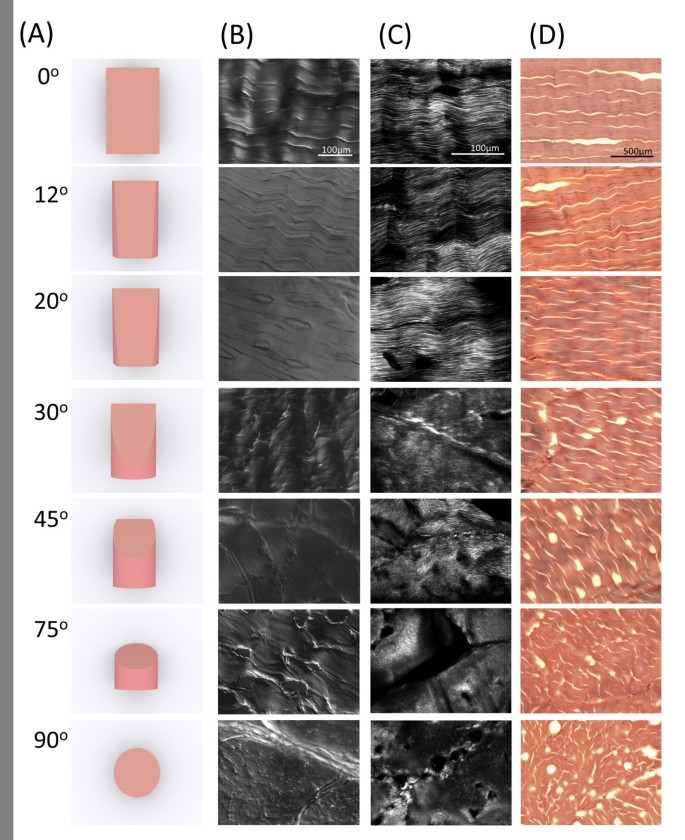
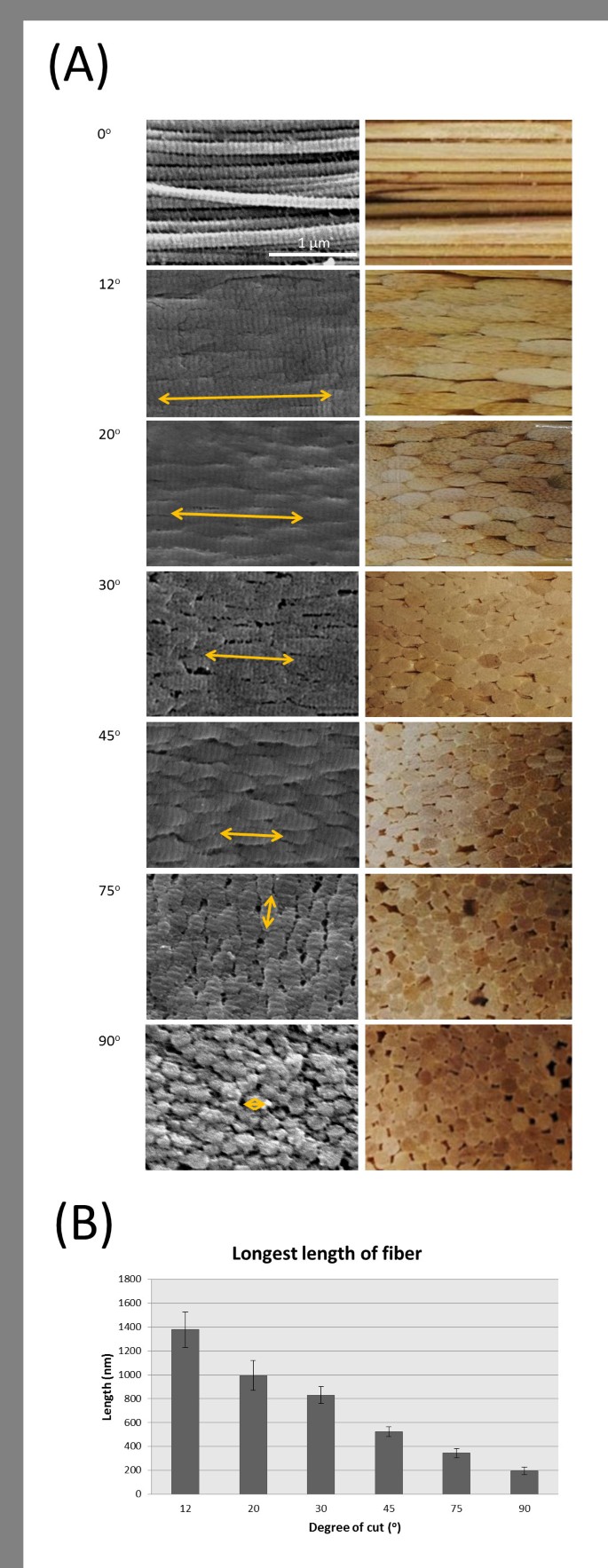
3.2 间充质干细胞形态与黏着斑分析
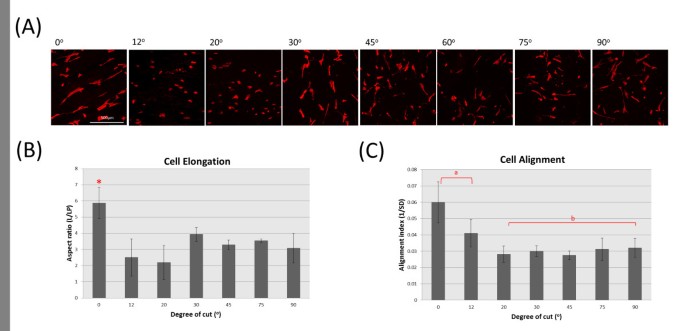
实验目的为检测不同ECM空间排布对MSCs形态与黏着斑形成的调控作用。方法细节上,将稳定表达GFP的人MSCs以1×10^4 cells/cm²的密度接种于不同角度的跟腱切片上,常规培养3天后,采用罗丹明-鬼笔环肽染色标记细胞肌动蛋白骨架,Hoechst染色标记细胞核,免疫荧光染色纽蛋白以定位黏着斑;利用ImageJ软件定量分析细胞的伸长率(长轴/短轴比值)与相对排列度。结果解读显示,接种于0°和12°跟腱切片上的MSCs呈现高度伸长且沿胶原纤维平行排列的形态,细胞伸长率显著高于其他角度切片(n=50,P<0.05);当切片角度超过12°后,MSCs的伸长与排列能力显著下降,20°及以上角度切片上的细胞形态趋于圆形或不规则形(图5);黏着斑分析显示,0°、12°、45°切片上的细胞形成清晰的纽蛋白阳性黏着斑,而20°、30°、75°、90°切片上的细胞仅显示弥散的纽蛋白信号(图4),表明ECM空间排布可通过调控黏着斑的形成影响细胞形态。
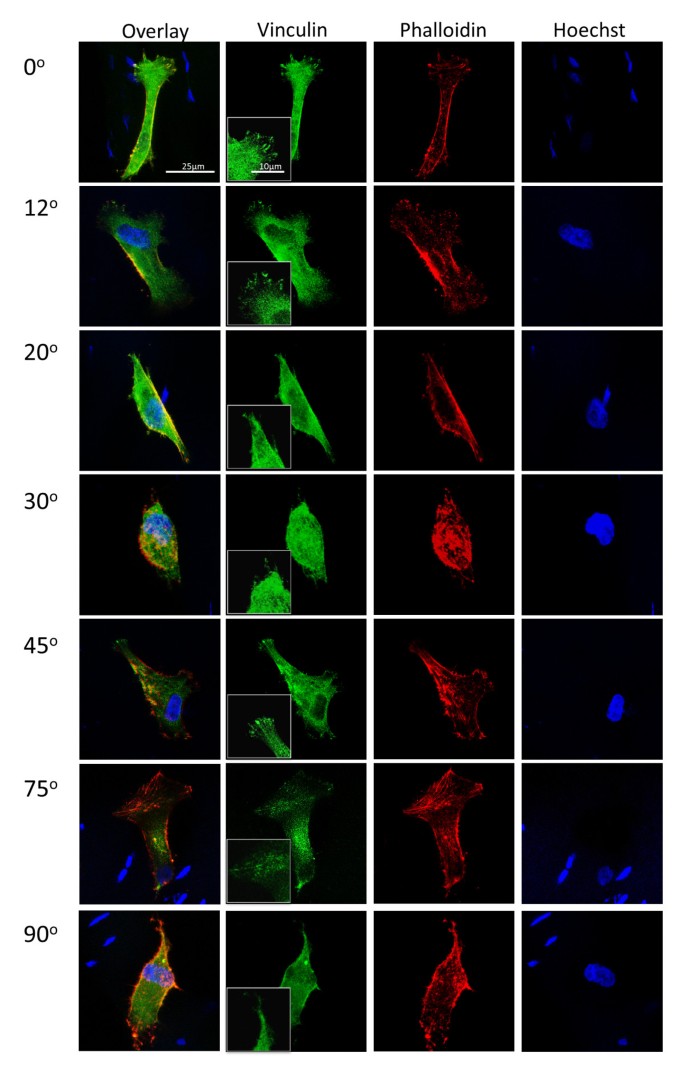
3.3 间充质干细胞肌腱分化标志物检测
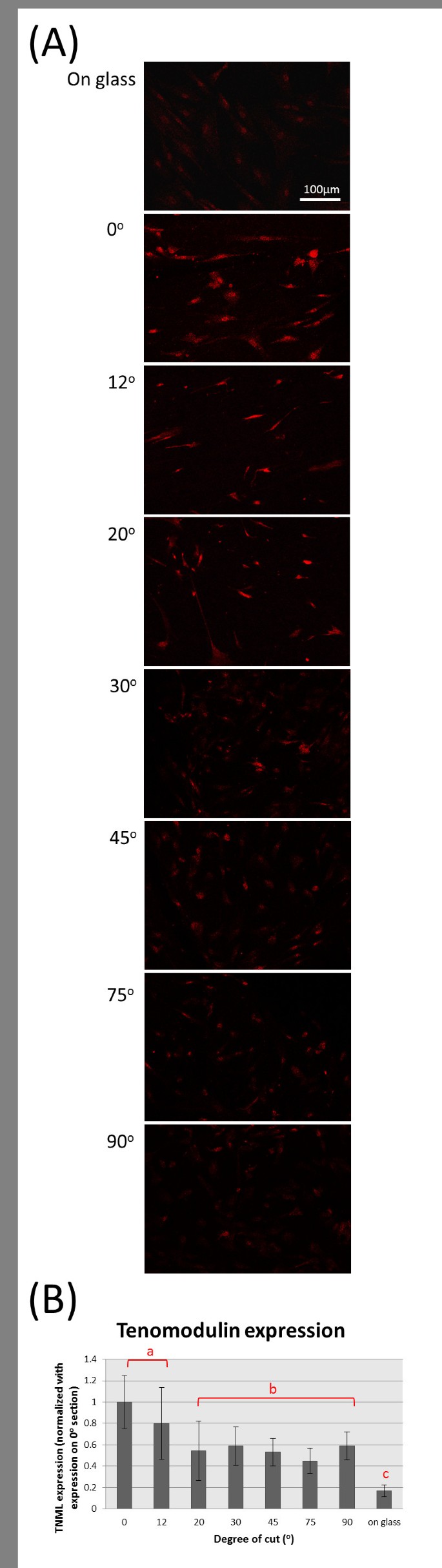
实验目的为探究ECM空间排布对MSCs肌腱分化的调控作用。方法细节上,MSCs在不同角度跟腱切片上培养12天后,采用免疫荧光染色标记肌腱分化特异性标志物肌腱调蛋白,利用ImageJ软件定量分析细胞内肌腱调蛋白的染色强度。结果解读显示,0°和12°切片上的MSCs肌腱调蛋白染色强度显著高于其他角度切片及玻璃对照组(n=50,P<0.05),而20°及以上角度切片上的肌腱调蛋白表达水平显著降低,与玻璃对照组无显著差异(图6),表明仅当ECM胶原纤维呈长程平行排布时,才能有效诱导MSCs向肌腱细胞分化,角度偏差超过12°后分化诱导效应完全丧失。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker为肌腱调蛋白(Tenomodulin),属于肌腱细胞特异性分化标志物,研究通过“天然ECM模型筛选→细胞形态关联→免疫荧光定量验证”的完整逻辑链,明确了该标志物表达对ECM空间排布的严格依赖性。
Biomarker定位方面,该标志物为肌腱分化的特异性功能标志物,筛选与验证逻辑为:首先利用不同空间排布的天然ECM模型筛选可诱导MSCs分化的拓扑结构,随后通过细胞形态分析与黏着斑检测关联结构与细胞行为,最后通过免疫荧光定量验证标志物的表达水平,形成完整的验证链条。研究过程详述显示,该标志物的来源为培养12天的人MSCs细胞,验证方法为免疫荧光染色结合图像定量分析,特异性数据显示0°和12°切片上的MSCs肌腱调蛋白表达强度是玻璃对照组的2.1倍(n=50,P<0.05),敏感性方面,仅当ECM胶原纤维呈长程平行排布(0°、12°)时,才能有效诱导该标志物表达,角度偏差超过12°后表达水平显著下降至对照组水平。核心成果提炼方面,该标志物的功能关联为作为MSCs肌腱分化的特异性指标,其表达严格依赖于ECM胶原纤维的精确空间排布;创新性为首次揭示了ECM空间排布的阈值效应(12°为临界角度)对干细胞分化标志物表达的调控作用,为组织工程支架的拓扑结构设计提供了量化的实验依据,统计学结果显示不同角度组间的表达强度差异具有显著性(P<0.05),为后续研究ECM空间结构与干细胞命运的调控机制奠定了基础。
