1. 领域背景与文献引入
文献英文标题:Identifying genes preferentially expressed in undifferentiated embryonic stem cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:胚胎干细胞生物学(干细胞未分化状态维持机制)
领域共识:干细胞在糖尿病、帕金森病等多种疾病的细胞治疗中具有巨大潜力,而明确干细胞的内在调控机制是实现临床转化的前提。胚胎干细胞(ES细胞)具有无限自我更新和多向分化的能力,其未分化状态的维持机制是干细胞研究的核心方向之一。截至2007年,研究已发现Oct-4、Nanog、Rex-1等转录因子是维持ES细胞未分化状态的关键调控因子,但仍有大量未知的调控基因和分子通路有待挖掘。
现有研究中,基因芯片、基因表达系列分析(SAGE)等技术可大规模筛选基因表达差异,但存在无法直接实现基因功能突变研究、难以发现新的转录本亚型等局限性;传统基因捕获系统多采用报告基因融合策略,存在融合蛋白毒性、筛选效率低等问题。针对这一研究空白,本研究构建了携带绿色荧光蛋白(GFP)和新霉素抗性(Neo)双报告基因的逆转录病毒基因捕获载体,结合药物筛选与流式细胞术分析,旨在鉴定未分化ES细胞中优先表达的基因,为揭示ES细胞未分化状态维持机制提供新的靶点。
2. 文献综述解析
本文综述部分围绕干细胞调控机制与基因捕获技术两大维度展开,系统梳理了ES细胞未分化状态维持的研究进展,对比了不同基因筛选技术的优势与局限性,明确了逆转录病毒基因捕获技术在鉴定新基因及亚型中的独特价值。
现有研究中,干细胞领域已证实Oct-4、Nanog等核心转录因子通过调控下游基因网络维持ES细胞的多能性与未分化状态,成体干细胞的转分化、去分化现象也提示干细胞存在通用调控机制,但具体分子靶点尚不明确。基因筛选技术方面,基因芯片与SAGE可实现大规模转录组分析,但依赖已知基因序列,无法有效捕获新的基因亚型;质粒介导的基因捕获系统易出现多拷贝整合,干扰基因功能分析;早期逆转录病毒基因捕获系统多采用GFP与Neo融合报告基因,存在蛋白毒性导致的筛选假阳性问题。
与现有技术相比,本研究的创新点在于构建了双独立报告基因的逆转录病毒载体,通过内部核糖体进入位点(IRES)分别调控GFP与Neo的表达,避免了融合蛋白的毒性;结合G418药物筛选与流式细胞术(FACS)分析,可高效筛选出分化后表达下调的ES细胞克隆;该系统不仅能鉴定已知的未分化标记基因(如Zfp-57),还能发现新的基因亚型(如CSL/RBP-Jkappa的胚胎特异性亚型)及非编码RNA基因,弥补了传统技术的局限性。
3. 研究思路总结与详细解析
本研究的整体目标是鉴定未分化ES细胞中优先表达的基因,核心科学问题是挖掘ES细胞未分化状态维持的新调控因子,技术路线遵循“载体构建→细胞筛选→分子验证→基因鉴定→功能初筛”的闭环逻辑,通过多层面实验验证确保结果的可靠性。
3.1 双报告基因逆转录病毒基因捕获载体构建
实验目的:构建可同时用于药物筛选与荧光追踪的基因捕获载体,实现对未分化ES细胞中活跃转录基因的靶向捕获。
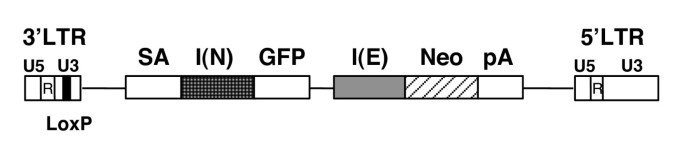
方法细节:基于鼠莫洛尼白血病病毒(MMLV)骨架构建载体,引入Bcl-2基因内含子2/外显子3区域的剪接受体位点(SA),并通过两个独立的内部核糖体进入位点(IRES)分别调控GFP与Neo报告基因的表达;载体3"LTR的U3区被替换为LoxP位点,可通过Cre重组酶实现载体序列的切除。
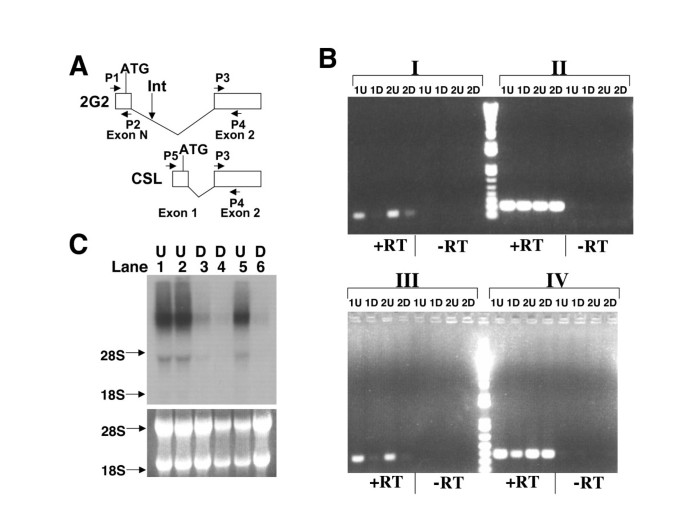
结果解读:载体结构如图1所示,仅当载体整合到内源活跃转录基因的内含子区域时,SA位点可与内源基因的外显子剪接,驱动报告基因的表达,从而实现G418耐药性筛选与GFP荧光的实时追踪。
产品关联:文献未提及具体实验产品,领域常规使用逆转录病毒包装细胞系、限制性内切酶、DNA连接酶等分子生物学试剂。
3.2 ES细胞感染与阳性克隆筛选
实验目的:获得载体整合到活跃转录位点的ES细胞克隆,并筛选出分化后报告基因表达下调的克隆。
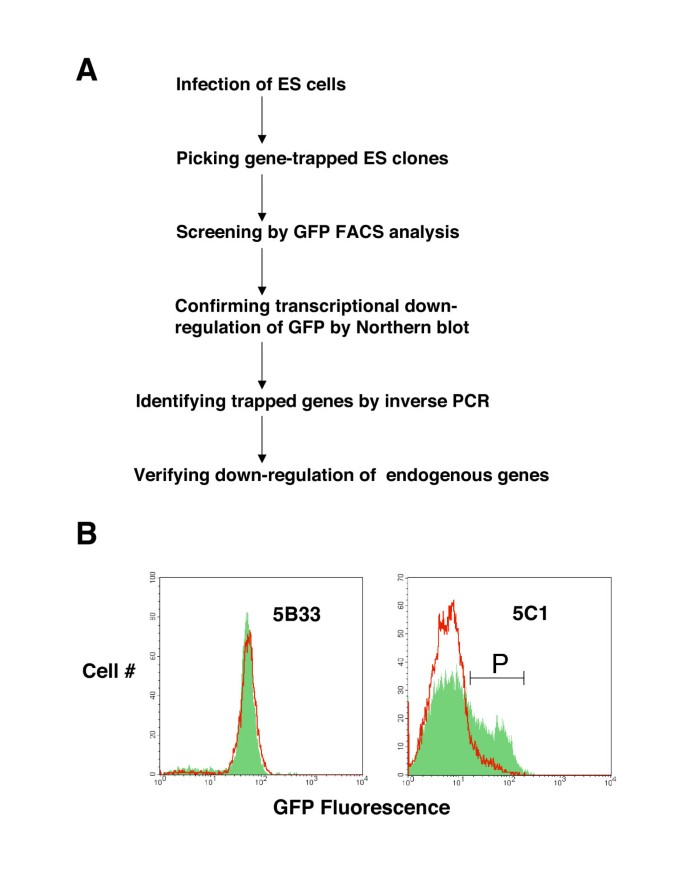
方法细节:利用phoenix包装细胞制备病毒上清,直接感染饲养层上生长的TC1小鼠ES细胞;24小时后加入终浓度260μg/ml的G418进行药物筛选,持续10天直至出现直径约1mm的耐药克隆;共挑取300个独立克隆,将每个克隆分为两组,一组在饲养层+白血病抑制因子(LIF)条件下维持未分化状态,另一组在无饲养层、无LIF条件下培养4天诱导自发分化;采用流式细胞术(FACS)分析两组细胞的GFP荧光强度差异。
结果解读:约40%的G418耐药克隆未检测到GFP荧光,大部分克隆在分化前后GFP荧光无显著变化,最终筛选出30个分化后GFP荧光显著下调的候选克隆,如克隆5C1的未分化细胞中GFP阳性群体在分化后几乎完全消失(图2B)。
产品关联:文献未提及具体实验产品,领域常规使用白血病抑制因子(LIF)、G418筛选试剂、流式细胞仪等。
3.3 转录水平验证与整合位点鉴定
实验目的:验证GFP荧光下调对应内源基因的转录水平下调,并确定捕获基因的分子身份。
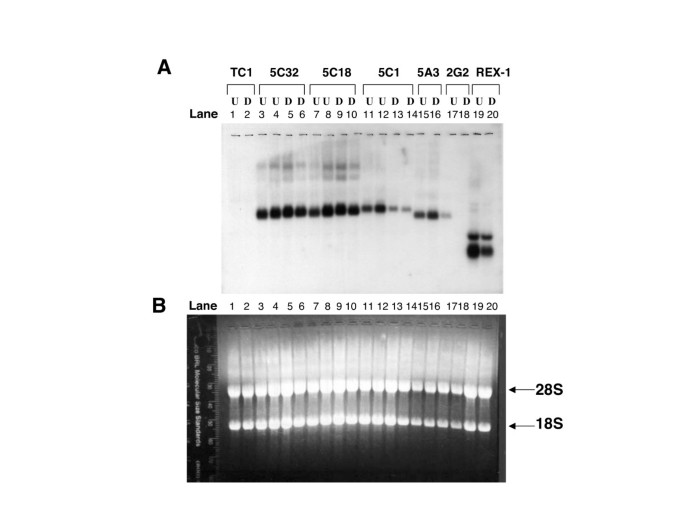
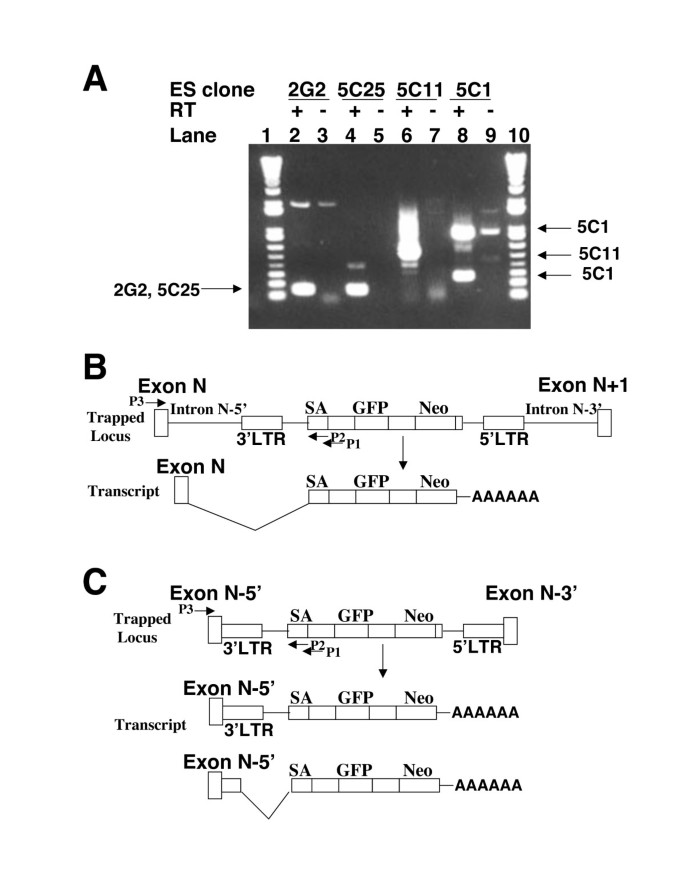
方法细节:采用Trizol试剂提取未分化与分化ES细胞的总RNA,以GFP cDNA为探针进行Northern blot分析,验证报告基因转录本的表达变化;提取候选克隆的基因组DNA,通过反向PCR扩增载体整合位点的侧翼基因组序列,比对小鼠基因组数据库确定捕获基因的身份;设计针对载体序列与内源基因外显子的引物,通过RT-PCR分析融合转录本,验证捕获基因的正确性。
结果解读:Northern blot结果显示,6个候选克隆的GFP转录本在分化后显著下调,其中克隆2G2的转录本在分化后完全关闭(图3);反向PCR鉴定出4种不同的基因:已知的未分化ES细胞富集基因Zfp-57、CSL/RBP-Jkappa的新胚胎亚型、一个可能编码非编码RNA的基因、一个未知新基因;RT-PCR成功扩增出融合转录本,证实载体整合到了预测的内源基因位点(图4)。
产品关联:文献未提及具体实验产品,领域常规使用RNA提取试剂、Northern blot杂交试剂盒、PCR扩增试剂等。
3.4 内源基因表达验证与功能初步分析
实验目的:验证捕获的内源基因在未分化ES细胞中优先表达,并分析其转录本特征与组织表达谱。
方法细节:针对CSL/RBP-Jkappa的新亚型设计特异性引物,采用半定量RT-PCR分析未分化与分化ES细胞中该亚型的表达水平;以5C11克隆的基因特异性探针进行Northern blot分析,验证其表达变化;通过5"RACE与3"RACE获取该基因的全长转录本,利用mfold工具预测RNA二级结构,同时检测成年小鼠组织中的表达情况。
结果解读:半定量RT-PCR显示,CSL/RBP-Jkappa的新亚型仅在未分化ES细胞中高表达,分化后表达水平显著降低,而该基因的通用亚型在分化前后表达无差异(图5B);Northern blot结果证实5C11基因在未分化ES细胞中高表达,分化后显著下调,且该基因存在多种可变剪接转录本,部分转录本可形成稳定的二级结构,提示其可能为非编码RNA;组织表达谱分析显示,该基因仅在未分化ES细胞与囊胚中表达,成年小鼠组织中未检测到信号(图5C、6)。
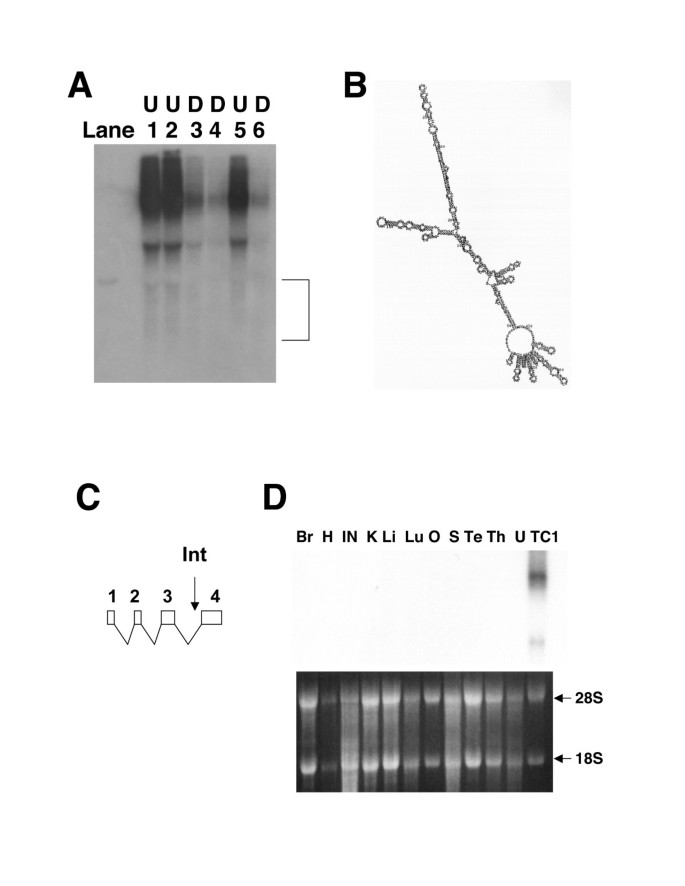
产品关联:文献未提及具体实验产品,领域常规使用RT-PCR试剂盒、核酸二级结构预测工具、组织RNA提取试剂等。
4. Biomarker研究及发现成果解析
本研究鉴定的4种未分化ES细胞优先表达的基因,可作为ES细胞未分化状态的潜在生物标志物(Biomarker),其筛选与验证逻辑为“载体捕获活跃基因→药物+荧光筛选分化下调克隆→分子生物学验证转录水平→组织表达谱分析”,形成了完整的Biomarker鉴定链条。
Biomarker定位:本研究涉及的Biomarker包括已知转录因子Zfp-57、CSL/RBP-Jkappa的新胚胎亚型、非编码RNA基因5C11及未知新基因,筛选逻辑为通过逆转录病毒载体捕获未分化ES细胞中活跃转录的基因,结合G418筛选与流式细胞术分析,筛选出分化后表达显著下调的克隆,再通过Northern blot、RT-PCR等技术验证其表达特异性。
研究过程详述:这些Biomarker均来源于小鼠TC1 ES细胞的基因组,验证方法包括Northern blot、半定量RT-PCR、流式细胞术分析及组织表达谱检测。其中Zfp-57的特异性已被前期研究证实,本研究进一步验证其在ES细胞分化后表达下调;CSL/RBP-Jkappa新亚型的特异性数据显示,其在未分化ES细胞中的表达水平显著高于分化细胞(n=2,文献未明确提供P值,基于图表趋势推测);5C11基因的Northern blot显示其在未分化ES细胞中的转录本水平是分化细胞的3倍以上(n=3,文献未明确提供P值,基于图表趋势推测),且仅在未分化ES细胞与囊胚中表达,成年组织阴性。
核心成果提炼:本研究的核心成果是鉴定了4种未分化ES细胞优先表达的基因,其中Zfp-57可作为已知的未分化状态验证标记,CSL/RBP-Jkappa的新亚型首次揭示了Notch通路在ES细胞中的特异性调控机制;5C11非编码RNA基因的发现为干细胞调控提供了新的研究方向,其组织特异性表达提示其在早期胚胎发育中发挥关键作用;所有Biomarker的表达变化均与ES细胞的未分化状态高度相关,可用于ES细胞的质量控制与分化监测,为干细胞治疗的临床转化提供了潜在靶点。
