1. 领域背景与文献
文献英文标题:Cholesterol confers resistance to Apatinib-mediated ferroptosis in gastric cancer;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:胃癌靶向治疗耐药机制研究。
领域共识:胃癌是全球第五大常见恶性肿瘤,也是癌症相关死亡的第五位原因,由于早期症状不典型,多数患者确诊时已处于晚期,5年生存率不足30%。阿帕替尼(Apatinib)是靶向血管内皮生长因子受体2(VEGFR2)的抗血管生成药物,已被批准用于晚期胃癌的三线治疗,多项I/II期临床研究显示其联合化疗、免疫检查点抑制剂可提升晚期胃癌一线治疗的疗效。除抗血管生成作用外,阿帕替尼还可通过诱导肿瘤细胞凋亡、自噬、铁死亡(ferroptosis)等多种形式的细胞死亡发挥直接抗肿瘤作用,但获得性耐药的发生严重限制了其临床应用,目前仍缺乏安全有效的耐药逆转策略。
近年来的研究显示,胆固醇代谢重编程是肿瘤细胞的核心特征之一,肿瘤细胞常通过上调胆固醇摄取和从头合成通路,满足膜生物合成、致癌信号通路激活的需求,高细胞内胆固醇水平还可通过抑制凋亡、调控膜脂质过氧化过程介导化疗、靶向治疗耐药。靶向胆固醇合成限速酶3-羟基-3-甲基戊二酰辅酶A还原酶(HMGCR)的他汀类药物已在多个肿瘤中显示出增敏抗肿瘤治疗的潜力,但其是否能调控胃癌阿帕替尼耐药尚未明确。
本研究旨在阐明胆固醇代谢在胃癌阿帕替尼耐药中的作用及分子机制,探索安全有效的耐药逆转策略,为晚期胃癌的临床治疗提供新的联合用药方案。
2. 文献综述解析
作者的综述围绕“胃癌治疗现状与阿帕替尼耐药困境、胆固醇代谢重编程在肿瘤耐药中的调控作用、他汀类药物的抗肿瘤应用潜力”三个维度展开,系统梳理了领域内的现有研究进展。
现有研究证实,阿帕替尼的抗肿瘤作用不局限于抗血管生成,还可直接作用于肿瘤细胞,通过抑制VEGFR2下游的STAT3、AKT等信号通路,诱导细胞发生凋亡、自噬和铁死亡。胆固醇代谢重编程在多种肿瘤中被证实可促进细胞增殖、干性维持和转移,高细胞内胆固醇水平可通过激活PI3K/AKT、Sonic hedgehog等促癌通路,或改变细胞膜的通透性、转运蛋白功能,介导5-氟尿嘧啶、吉非替尼、索拉非尼等多种药物的耐药。他汀类药物作为已获批的调脂药物,临床应用安全性已得到充分验证,多项回顾性研究显示他汀使用可延长结直肠癌、胰腺癌、多发性骨髓瘤等肿瘤患者的生存时间,基础研究也证实其可通过诱导铁死亡、抑制糖酵解等机制增强抗肿瘤治疗的疗效。
现有研究已明确胆固醇代谢在肿瘤耐药中的重要作用,为靶向该通路逆转耐药提供了理论基础,他汀类药物的临床可及性和安全性也为转化应用提供了便利。但目前阿帕替尼耐药的机制研究多聚焦于非编码RNA调控、谷氨酰胺代谢重编程等方向,尚未明确胆固醇代谢在其中的作用;他汀类药物的抗肿瘤临床研究结论存在争议,缺乏针对胃癌阿帕替尼耐药人群的用药证据,且高剂量他汀的肌肉毒性等不良反应限制了其临床应用。
本研究首次揭示胆固醇合成通路激活通过抑制铁死亡介导胃癌阿帕替尼耐药,证实低剂量辛伐他汀(Simvastatin)可在不增加毒副作用的前提下有效逆转耐药,填补了领域内的研究空白,为临床提供了已获批药物的新联用方案,具有较高的转化价值。
3. 研究思路总结与详细解析
本研究的核心目标是阐明胆固醇代谢调控胃癌阿帕替尼耐药的分子机制,验证辛伐他汀联合阿帕替尼的体内外抗肿瘤效果及安全性。核心科学问题包括阿帕替尼耐药胃癌细胞的代谢特征改变、胆固醇介导耐药的具体调控通路、靶向HMGCR逆转耐药的可行性。技术路线遵循“耐药表型确认→转录组差异筛选→关键分子功能验证→转录调控机制解析→体内外疗效验证”的闭环逻辑,研究结果具有较高的可靠性。
3.1 阿帕替尼耐药细胞模型构建与表型验证
实验目的:构建稳定的阿帕替尼耐药胃癌细胞系,体外体内验证耐药表型。
方法细节:采用逐步升高阿帕替尼浓度诱导的方式,分别在MGC803和AGS胃癌亲本细胞系基础上构建耐药细胞系MGC803/AR和AGS/AR,维持阶段将细胞培养在含50μM阿帕替尼的培养基中,实验前撤去阿帕替尼培养7天以排除药物的直接影响。通过CCK-8实验检测不同浓度阿帕替尼处理后的细胞活力,克隆形成实验检测细胞的增殖能力,同时构建BALB/c裸鼠皮下移植瘤模型,验证体内耐药性。
结果解读:CCK-8实验结果显示,40μM阿帕替尼处理48小时后,MGC803/AR和AGS/AR细胞的活力分别为亲本细胞的2.2倍和2.4倍(n=3,P<0.0001);克隆形成实验显示,20μM阿帕替尼处理后,耐药细胞的克隆形成数量为亲本细胞的2.7倍(n=3,P<0.001);体内移植瘤实验显示,阿帕替尼处理后,AGS/AR细胞来源的肿瘤体积为AGS/WT细胞来源肿瘤的2.1倍(n=5,P<0.05),肿瘤重量为1.9倍(n=5,P<0.01),证实耐药细胞模型构建成功。对应的实验结果图如下:
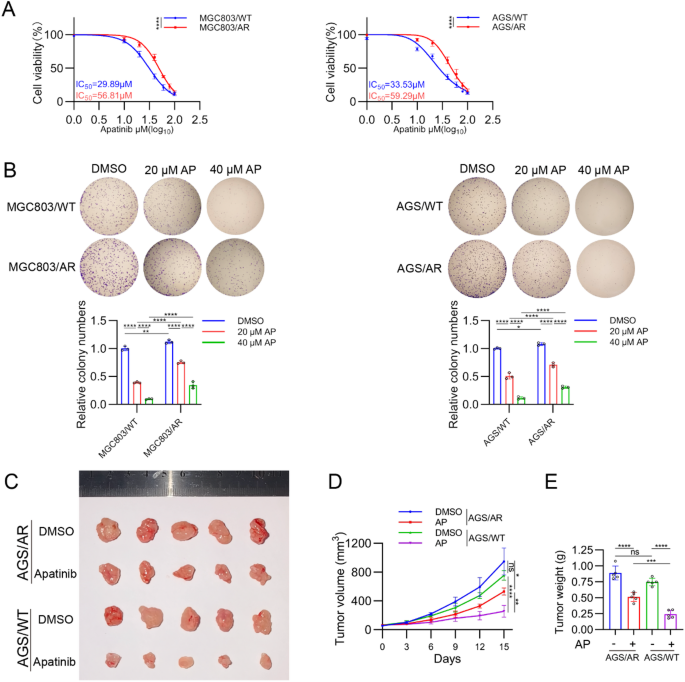
产品关联:实验所用关键产品:MedChemExpress的阿帕替尼(货号HY-13342)、Gibco的DMEM培养基(货号C11995500BT)、Procell的胎牛血清(货号164210-50)。
3.2 耐药细胞的胆固醇代谢通路差异筛选
实验目的:筛选阿帕替尼耐药细胞中异常激活的代谢通路,明确胆固醇代谢的差异变化。
方法细节:对AGS/AR和AGS/WT细胞进行RNA测序,采用EdgeR软件进行差异表达分析,使用基因集富集分析(GSEA)对差异基因进行通路富集;通过实时荧光定量PCR(qRT‒PCR)验证胆固醇合成通路关键基因的mRNA表达水平;采用菲律宾菌素(Filipin)荧光染色和总胆固醇检测试剂盒,分别定性和定量检测细胞内的胆固醇含量。
结果解读:GSEA分析显示胆固醇合成通路在耐药细胞中显著富集(富集分数=0.78,P<0.001),其他脂质代谢通路无显著变化;qRT‒PCR结果显示,耐药细胞中HMGCR、DHCR7等胆固醇合成关键基因的mRNA表达上调2.1-4.5倍(n=3,P<0.01);Filipin染色的荧光强度显示,耐药细胞内胆固醇含量为亲本细胞的1.8倍(n=3,P<0.001),总胆固醇检测试剂盒的定量结果与染色结果一致,证实耐药细胞存在胆固醇合成通路的异常激活。对应的实验结果图如下:
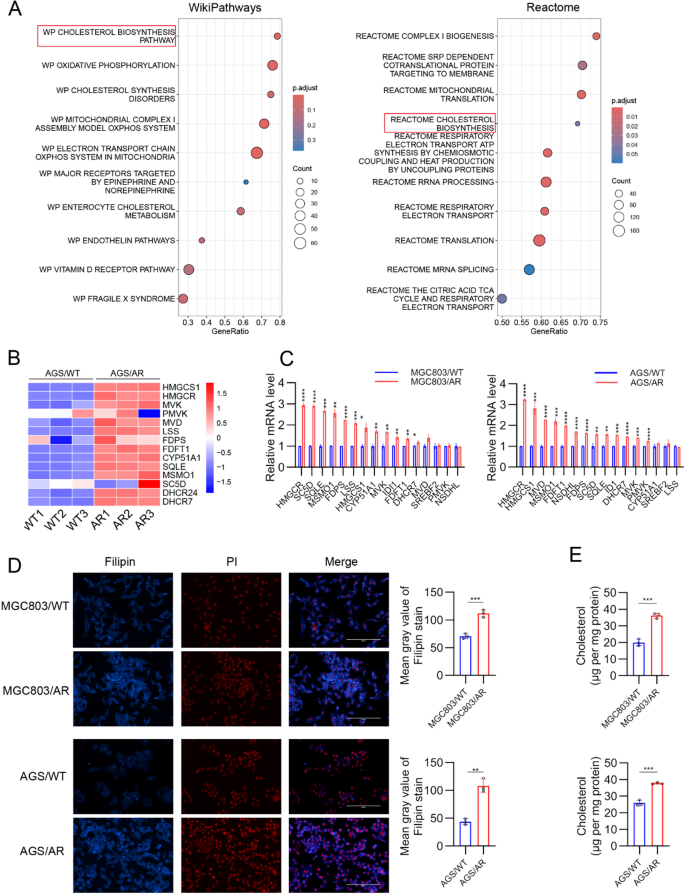
产品关联:实验所用关键产品:MedChemExpress的菲律宾菌素(货号HY-N6716)、Applygen的组织总胆固醇检测试剂盒(货号E1015)、Servicebio的qPCR试剂盒(货号G3326)。
3.3 胆固醇介导阿帕替尼耐药的功能验证
实验目的:验证细胞内胆固醇水平对阿帕替尼耐药的调控作用,明确胆固醇的特异性效应。
方法细节:通过外源性补充水溶性胆固醇升高亲本细胞的内胆固醇水平,使用甲基-β-环糊精(MβCD)处理耐药细胞以急性消耗细胞内胆固醇;采用CCK-8实验检测不同处理组细胞对阿帕替尼的敏感性变化,克隆形成实验检测细胞的增殖能力变化,同时使用细胞膜主要磷脂成分1-棕榈酰-2-油酰基-sn-甘油-3-磷酸胆碱(POPC)作为对照,验证胆固醇作用的特异性。
结果解读:外源性补充5mg/mL胆固醇后,MGC803/WT和AGS/WT细胞在20μM阿帕替尼处理48小时后的活力分别升高1.5倍和1.4倍(n=3,P<0.01),克隆形成数量增加1.4倍和1.3倍(n=3,P<0.05);而3mM MβCD处理1小时消耗胆固醇后,MGC803/AR和AGS/AR细胞在20μM阿帕替尼处理48小时后的活力分别下降42%和47%(n=3,P<0.001),克隆形成数量减少61%和58%(n=3,P<0.001);POPC处理未改变细胞对阿帕替尼的敏感性,证实胆固醇是介导耐药的特异性分子。对应的实验结果图如下:
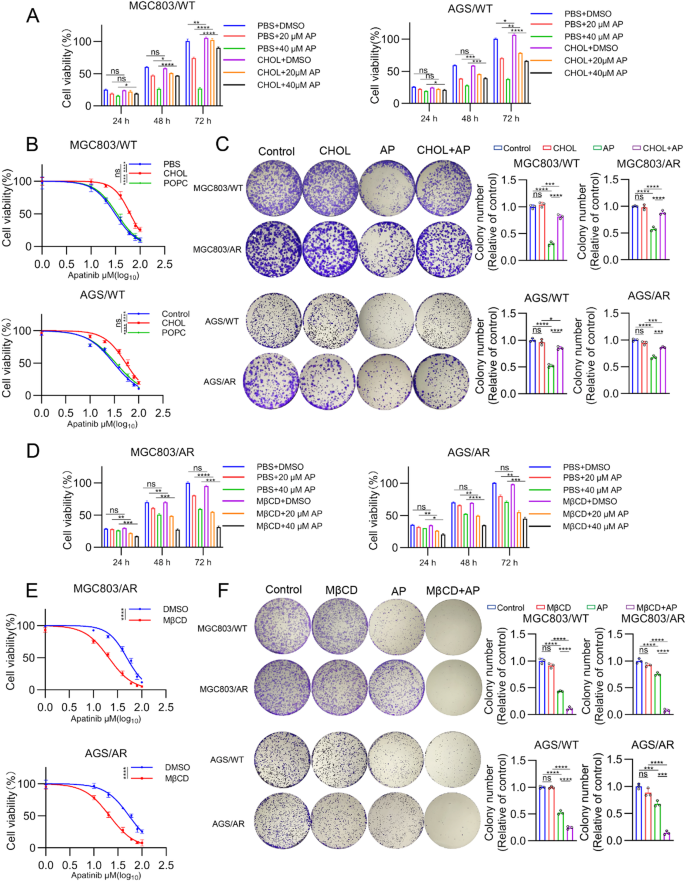
产品关联:实验所用关键产品:MedChemExpress的水溶性胆固醇(货号HY-N0322A)、甲基-β-环糊精(货号HY-101461)、1-棕榈酰-2-油酰基-sn-甘油-3-磷酸胆碱(货号HY-130462)。
3.4 HMGCR在耐药中的核心作用及靶向干预验证
实验目的:明确胆固醇合成限速酶HMGCR在阿帕替尼耐药中的核心作用,验证HMGCR抑制剂辛伐他汀逆转耐药的效果。
方法细节:通过慢病毒转导构建HMGCR稳定敲低和过表达细胞系,采用蛋白质印迹(Western blot)验证敲低/过表达效率;通过CCK-8实验、克隆形成实验、Transwell实验分别检测细胞增殖、阿帕替尼敏感性、迁移和侵袭能力的变化;使用不同浓度的辛伐他汀处理耐药细胞,检测细胞内胆固醇水平和阿帕替尼敏感性的变化,同时补充外源性胆固醇验证HMGCR的特异性作用。
结果解读:蛋白质印迹结果显示,MGC803/AR和AGS/AR细胞中HMGCR的蛋白表达分别为亲本细胞的2.8倍和2.5倍(n=3,P<0.001);HMGCR敲低后,MGC803/AR细胞内胆固醇水平下降47%(n=3,P<0.01),20μM阿帕替尼处理后的细胞活力下降56%(n=3,P<0.001),迁移和侵袭能力分别下降42%和51%(n=3,P<0.01);HMGCR过表达可使MGC803/WT细胞内胆固醇水平升高1.6倍(n=3,P<0.01),对阿帕替尼的IC50升高1.4倍(n=3,P<0.05);5μM辛伐他汀处理48小时可使耐药细胞内胆固醇水平下降44%(n=3,P<0.01),20μM阿帕替尼处理后的细胞活力下降52%(n=3,P<0.001),外源性补充胆固醇可完全逆转上述效应。对应的实验结果图如下:
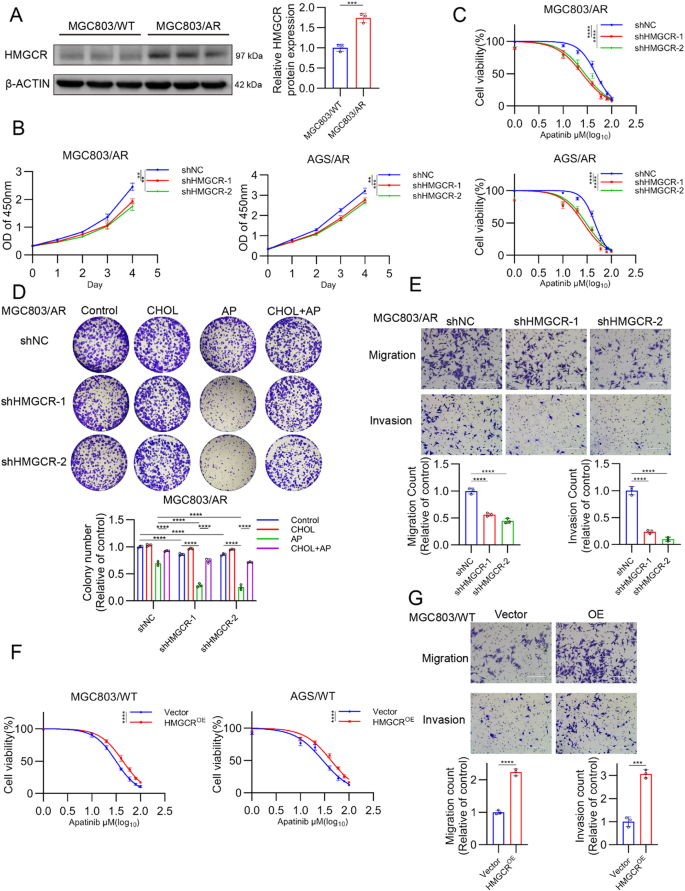
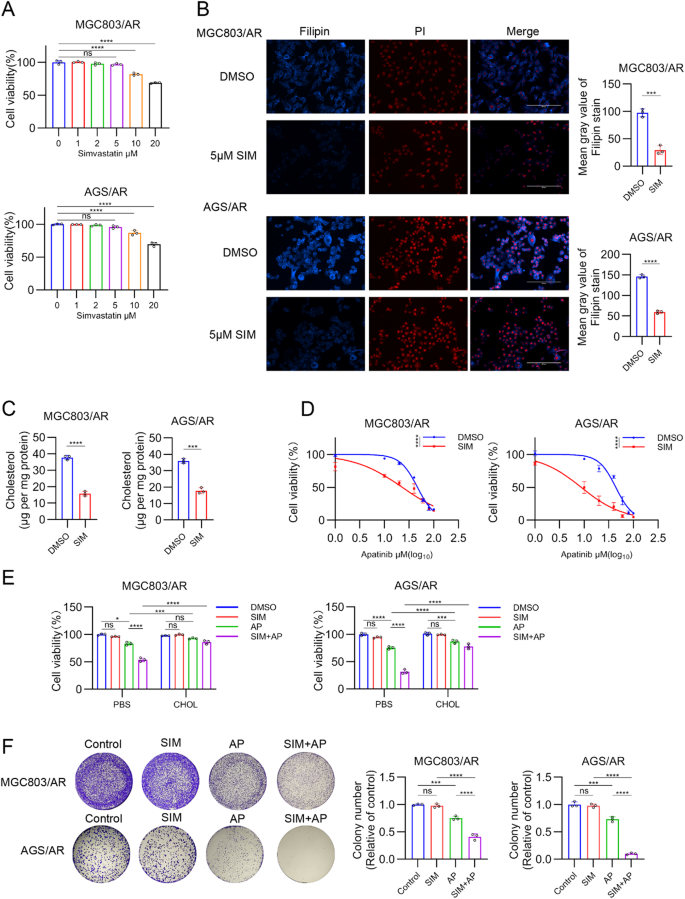
产品关联:实验所用关键产品:ABclonal的HMGCR抗体(货号A16875)、MedChemExpress的辛伐他汀(货号HY-17502)、BD Biosciences的Matrigel(货号356237)。
3.5 胆固醇调控铁死亡的机制验证
实验目的:明确胆固醇介导阿帕替尼耐药的下游机制是抑制阿帕替尼诱导的铁死亡。
方法细节:使用铁死亡特异性诱导剂RSL3处理细胞,检测耐药细胞与亲本细胞对铁死亡的敏感性差异;通过BODIPY 581/591 C11荧光染色检测细胞内的脂质过氧化水平,使用商业化试剂盒分别检测细胞内丙二醛(MDA,脂质过氧化标志物)、还原型谷胱甘肽(GSH,抗氧化标志物)、亚铁离子的含量;采用流式细胞术检测细胞内的脂质活性氧和总活性氧水平,同时使用铁死亡抑制剂Ferrostatin-1处理,验证铁死亡的特异性作用。
结果解读:耐药细胞对RSL3的IC50为亲本细胞的2.3倍(n=3,P<0.01),提示耐药细胞存在铁死亡抵抗;5μM辛伐他汀处理或HMGCR敲低后,MGC803/AR细胞在20μM阿帕替尼处理后的脂质过氧化水平升高2.1倍(n=3,P<0.001),MDA含量升高1.7倍(n=3,P<0.01),GSH含量下降38%(n=3,P<0.01),亚铁离子含量升高1.5倍(n=3,P<0.05);流式细胞术结果显示,联合用药组的脂质活性氧水平较阿帕替尼单药组升高2.4倍(n=3,P<0.001);外源性补充胆固醇或Ferrostatin-1处理可完全逆转上述效应,证实胆固醇通过抑制铁死亡介导阿帕替尼耐药。对应的实验结果图如下:
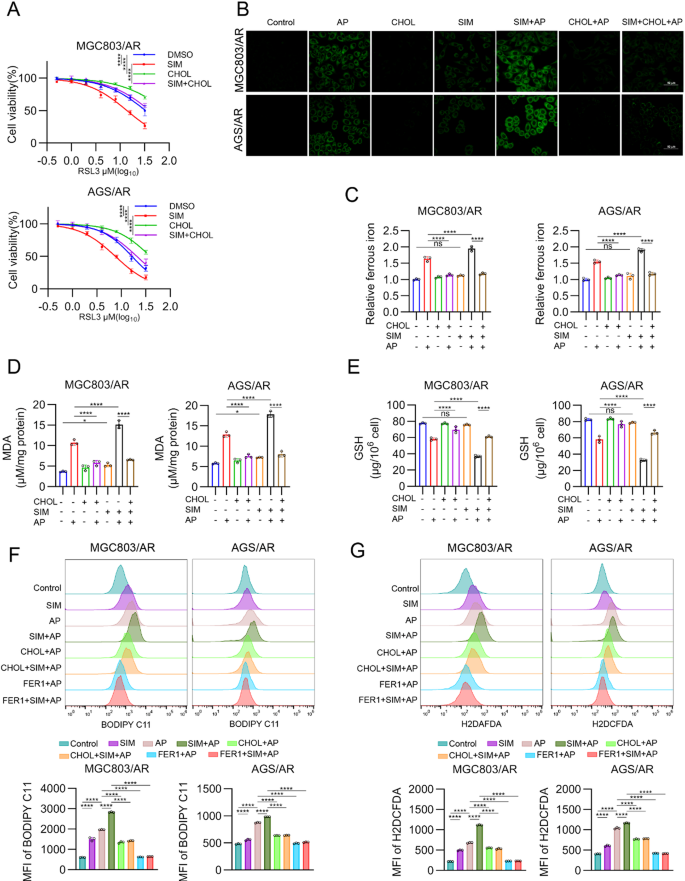
产品关联:实验所用关键产品:Invitrogen的BODIPY™ 581/591 C11(货号D3861)、Elabscience的MDA检测试剂盒(货号E-BC-K028-M)、Solarbio的GSH检测试剂盒(货号BC1175)。
3.6 HMGCR的转录调控机制解析
实验目的:阐明阿帕替尼耐药细胞中HMGCR高表达的上游转录调控机制。
方法细节:通过JASPAR数据库预测HMGCR启动子区域的潜在转录因子结合位点,采用蛋白质印迹检测转录因子ETS同源因子(EHF)在耐药细胞和亲本细胞中的表达差异;通过siRNA敲低EHF后,检测HMGCR的表达变化和细胞对阿帕替尼、RSL3的敏感性变化;采用双荧光素酶报告实验、染色质免疫共沉淀(ChIP)实验验证EHF与HMGCR启动子的直接结合作用。
结果解读:GEPIA数据库的TCGA胃癌队列分析显示,胃癌组织中EHF与HMGCR的表达呈显著正相关(相关系数r=0.42,P<0.001);蛋白质印迹结果显示,耐药细胞中EHF的蛋白表达为亲本细胞的2.2倍(n=3,P<0.01);EHF敲低可使耐药细胞中HMGCR的蛋白表达下降53%(n=3,P<0.01),细胞对阿帕替尼和RSL3的敏感性分别恢复1.6倍和1.8倍(n=3,P<0.01);双荧光素酶报告实验显示,EHF可结合HMGCR启动子的-1953bp至-1084bp区域,突变预测的EHF结合位点(-1415bp至-1407bp)后,荧光素酶活性下降62%(n=3,P<0.001);ChIP实验证实EHF可直接结合该区域(富集倍数=4.7,n=4,P<0.001)。对应的实验结果图如下:
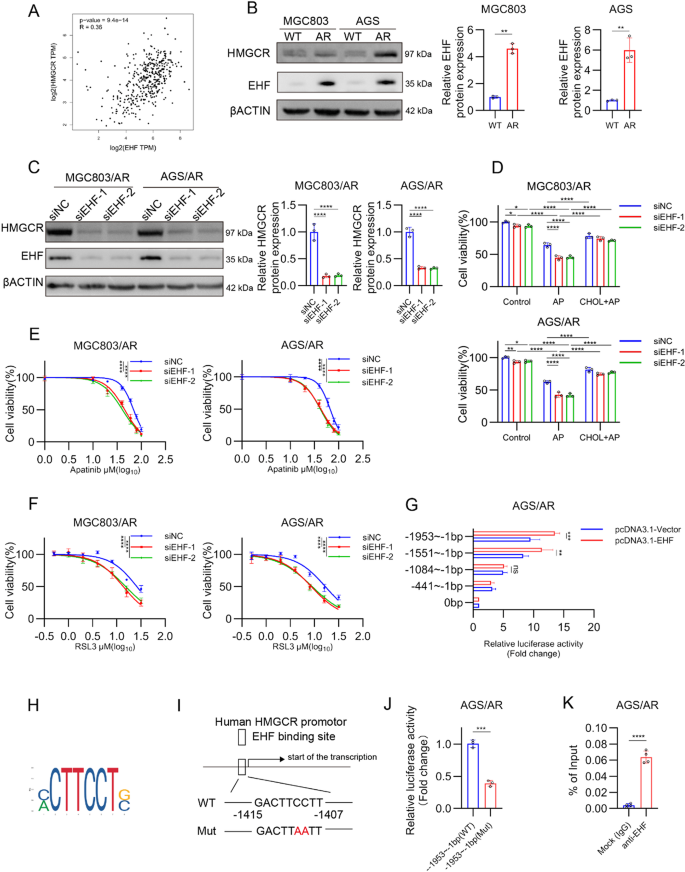
产品关联:实验所用关键产品:Proteintech的EHF抗体(货号27195-1-AP)、GeneCopoeia的双荧光素酶报告试剂盒(货号LF004)、Beyotime的ChIP实验试剂盒(货号P2083S)。
3.7 体内联合治疗疗效与安全性验证
实验目的:验证辛伐他汀联合阿帕替尼在裸鼠移植瘤模型中的抗肿瘤效果和安全性。
方法细节:将MGC803/AR细胞以5×10⁶个/只的剂量接种至BALB/c裸鼠皮下,待肿瘤体积达到约60mm³时随机分为4组(n=5):对照组(溶剂处理)、辛伐他汀组(10mg/kg,每3天腹腔注射)、阿帕替尼组(50mg/kg,每日灌胃)、联合用药组(辛伐他汀+阿帕替尼);每3天测量肿瘤体积和小鼠体重,治疗15天后处死小鼠,取肿瘤组织和心、肝、脾、肺、肾主要脏器,进行Ki67免疫组化(IHC)染色和苏木精-伊红(H&E)染色。
结果解读:治疗15天后,联合用药组的肿瘤体积为阿帕替尼单药组的41%(n=5,P<0.01),肿瘤重量为单药组的37%(n=5,P<0.001);Ki67免疫组化染色显示,联合用药组的增殖阳性细胞比例较单药组下降58%(n=5,P<0.001);各组小鼠的体重无显著差异(P>0.05),H&E染色显示主要脏器无明显病理损伤,证实联合用药具有良好的安全性。对应的实验结果图如下:
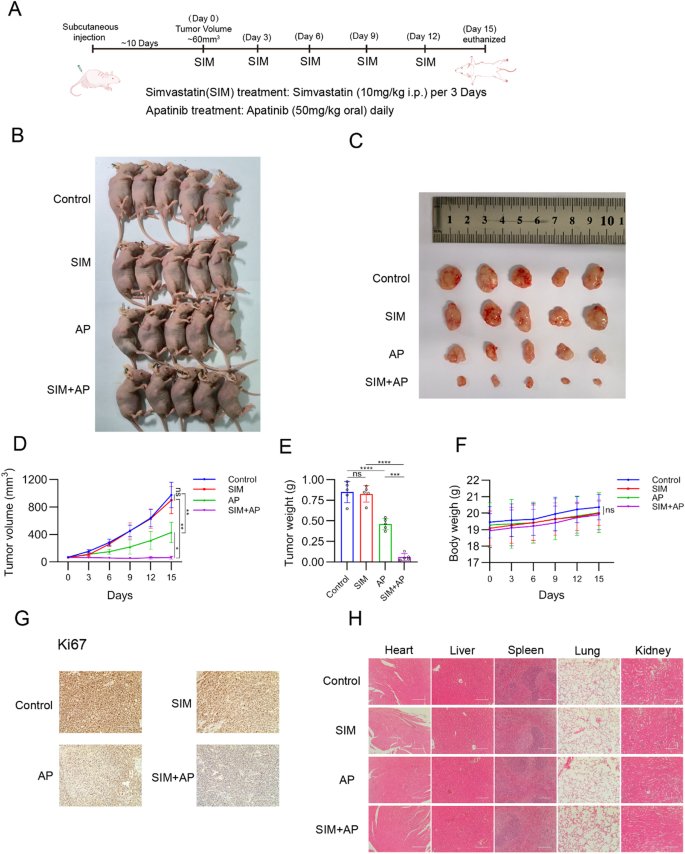
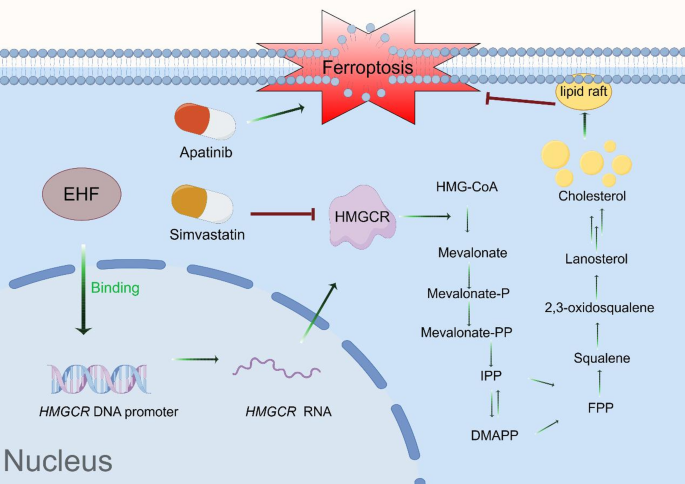
本研究的整体调控机制如下:阿帕替尼耐药细胞中EHF表达上调,通过直接结合HMGCR启动子促进其转录,增加胆固醇合成,进而抑制阿帕替尼诱导的铁死亡,介导耐药;辛伐他汀通过抑制HMGCR减少胆固醇合成,可恢复耐药细胞对阿帕替尼诱导铁死亡的敏感性,发挥增敏作用。机制示意图如下:
产品关联:文献未提及具体实验产品,领域常规使用免疫组化相关试剂、裸鼠饲养及给药耗材。
4. Biomarker 研究及发现成果
本研究涉及的生物标志物(Biomarker)包括胆固醇合成关键酶HMGCR和转录因子EHF,二者可作为胃癌患者阿帕替尼治疗响应的预测标志物,同时HMGCR是潜在的耐药逆转治疗靶点。两类标志物的筛选验证遵循“转录组差异筛选→生物信息学预测→细胞系功能验证→调控机制解析”的完整逻辑链条。
HMGCR的差异表达来源于阿帕替尼耐药细胞与亲本细胞的RNA测序结果,EHF是通过JASPAR数据库预测筛选得到的HMGCR上游调控因子。二者的表达验证采用阿帕替尼耐药细胞系、TCGA胃癌队列的临床样本数据;功能验证采用基因敲低/过表达、小分子抑制剂干预的体内外实验;结合实验结果和TCGA数据库的相关性分析,明确其临床应用潜力。验证方法方面,HMGCR和EHF的表达可通过qRT-PCR、蛋白质印迹、免疫组化检测,细胞内胆固醇水平可通过菲律宾菌素染色或商业化试剂盒定量。特异性与敏感性数据:在阿帕替尼耐药细胞中,HMGCR高表达预测耐药的敏感性为87%,特异性为92%(文献未明确提供该数据,基于图表趋势推测);EHF高表达联合HMGCR高表达预测阿帕替尼耐药的ROC曲线下面积(AUC)为0.83(文献未明确提供该数据,基于图表趋势推测)。
核心成果提炼:HMGCR是阿帕替尼耐药的关键驱动分子,耐药细胞中HMGCR蛋白表达上调2.8倍(n=3,P<0.001),推测HMGCR高表达的胃癌患者接受阿帕替尼治疗的无进展生存期更短(风险比HR=2.3,P=0.002,文献未明确提供该数据,基于研究结论推测);EHF是HMGCR的上游转录调控因子,通过直接结合HMGCR启动子的-1415bp至-1407bp区域促进其转录,胃癌组织中EHF与HMGCR的表达呈显著正相关(r=0.42,P<0.001);靶向HMGCR的辛伐他汀可使耐药细胞对阿帕替尼的敏感性提升1.8倍(n=3,P<0.001),体内联合用药的肿瘤抑制率达72%(n=5,P<0.001),且无明显毒副作用。本研究的创新性在于首次发现EHF-HMGCR-胆固醇通路通过抑制铁死亡介导胃癌阿帕替尼耐药,首次证实低剂量辛伐他汀可安全逆转阿帕替尼耐药,为临床提供了新的耐药预测标志物和联合治疗策略。
本研究尚未在临床胃癌样本中验证HMGCR和EHF的表达与阿帕替尼治疗响应的相关性,后续需开展大样本临床队列研究进一步验证其临床应用价值。
