1. 领域背景与文献引入
文献英文标题:CCN3: lactational bone booster;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:骨骼生物学与生殖内分泌交叉领域(哺乳期骨骼代谢调控)
领域共识:哺乳期母体需要通过乳汁向后代输送大量钙,经典调控机制认为,吸吮刺激抑制Kiss1神经元活性,导致促性腺激素释放激素分泌减少,下丘脑性腺功能减退,雌激素水平降低;同时甲状旁腺激素相关蛋白(PTHrP)水平升高,共同促进骨吸收,使骨骼中的钙释放到循环中以满足乳汁需求。临床研究显示,哺乳期女性通常在3-6个月内丢失5%-10%的骨矿物质含量,小鼠则丢失20%-33%的骨量,但断奶后骨量可快速恢复。然而,部分女性会发生妊娠-哺乳期骨质疏松(PLO),出现椎体压缩性骨折等严重症状,提示现有调控机制仍存在未明确的关键环节。当前研究热点聚焦于脑-乳腺-骨骼轴的精细调控,但尚未明确是否存在特异性因子在哺乳期平衡骨吸收与骨形成,以维持母体骨骼健康和后代生存。
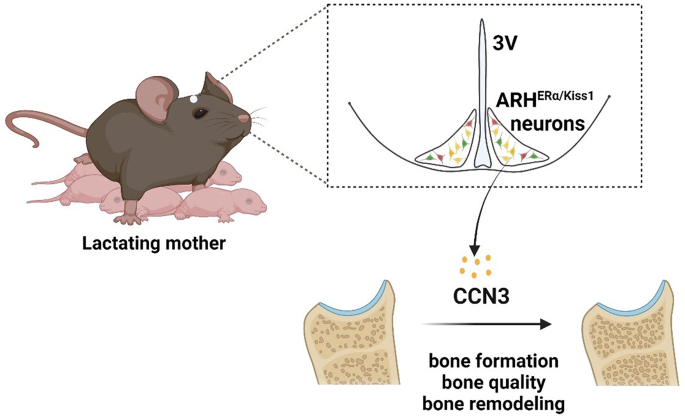
本研究针对这一核心空白,通过多组学、动物模型、细胞实验等多种技术手段,首次发现下丘脑弓状核(ARH)中ARH^{ERα/Kiss1}神经元来源的细胞通讯网络因子3(CCN3)作为成骨激素,在哺乳期特异性表达并维持骨形成,为哺乳期骨骼代谢调控提供了全新的脑-骨轴机制。
2. 文献综述解析
作者首先系统梳理了哺乳期骨骼代谢的经典调控框架,明确低雌激素与PTHrP介导骨吸收的核心作用,同时总结了脑-乳腺-骨骼轴的研究进展,指出当前领域已证实哺乳期骨丢失的可逆性,但对骨形成的主动调控机制尤其是脑源性因子的作用仍知之甚少。作者结合自身前期研究成果——中枢雌激素信号对骨形成存在性别依赖的抑制作用,且ARH区域Kiss1神经元是调控雌性骨量的关键亚群——进一步提出“是否存在脑源性循环成骨因子维持哺乳期骨代谢平衡”的科学问题。
现有研究的关键结论包括,哺乳期低雌激素状态是骨吸收增加的核心驱动因素,断奶后雌激素水平恢复可促进骨量快速回升;技术方法上,多物种(人、小鼠)的临床队列与动物实验结合,为骨代谢变化提供了坚实的证据支持,但现有研究的局限性在于,仅关注骨吸收的调控,未深入探究哺乳期骨形成的主动调控机制,尤其是脑-骨轴的特异性信号分子。本研究通过对比现有研究的空白,凸显了其创新性:首次发现脑源性CCN3作为成骨激素,在哺乳期特异性表达,填补了脑-乳腺-骨骼轴中骨形成调控因子的研究空白,为理解哺乳动物母体-后代骨骼代谢协同进化提供了新视角。
3. 研究思路总结与详细解析
本研究的整体研究目标是鉴定哺乳期脑-骨轴中的特异性成骨调控因子,核心科学问题为“是否存在脑源性循环因子在哺乳期维持骨形成,平衡骨吸收导致的骨丢失”,技术路线遵循“前期发现→假设提出→实验验证→功能确认→生理意义验证”的闭环逻辑:首先通过Esr1Nkx2-1Cre小鼠的高骨量表型提出循环成骨因子的假设,再通过联体实验、骨移植实验验证假设,随后通过高通量测序筛选并鉴定CCN3为候选因子,进而通过体内外实验验证其成骨功能,最终明确其在哺乳期的特异性表达及对母体和后代的生理作用。
3.1 联体实验与骨移植验证循环成骨因子存在
实验目的是验证Esr1Nkx2-1Cre小鼠的高骨量表型是否由循环可溶因子介导。研究人员将野生型(WT)小鼠与Esr1Nkx2-1Cre(Mut)小鼠进行联体手术,构建WT-WT和WT-Mut配对组,术后通过体内微计算机断层扫描(µCT)分析骨代谢参数;同时进行骨移植实验,将4周龄WT小鼠的雌雄股骨分别皮下植入8周龄WT或Esr1Nkx2-1Cre小鼠体内,检测骨体积分数(%BV/TV)的变化。结果显示,WT-Mut配对组中的WT小鼠骨量显著升高,%BV/TV较WT-WT组显著增加(文献未明确具体数值,基于图表趋势推测);Esr1Nkx2-1Cre小鼠植入WT股骨后,%BV/TV也显著高于WT小鼠植入组,且该效应在雌雄个体中均存在,提示存在雌性特异性的循环成骨因子,且对雌雄均有效。文献未提及具体实验产品,领域常规使用µCT成像系统、小鼠手术器械类试剂/仪器。
3.2 骨骼干细胞活性验证成骨因子作用靶点
实验目的是明确循环成骨因子是否通过调控骨软骨骨骼干细胞(ocSSCs)的活性发挥作用。研究人员将WT ocSSCs分别移植到WT和Esr1Nkx2-1Cre小鼠体内,检测移植细胞的矿化水平;同时将GFP标记的WT ocSSCs立体定向注射到下丘脑内侧基底部(MBH),6周后通过µCT观察矿化骨小体的形成;此外通过流式细胞分析和细胞分化实验,检测ocSSCs的频率与分化潜能。结果显示,移植到Esr1Nkx2-1Cre小鼠体内的WT ocSSCs矿化水平显著高于WT组,且Esr1Nkx2-1Cre小鼠体内ocSSCs的频率显著升高;MBH注射后,Esr1Nkx2-1Cre小鼠脑内出现与GFP阳性细胞重叠的矿化骨小体,而WT小鼠中未观察到该现象,提示循环成骨因子可促进ocSSCs的矿化与骨形成。文献未提及具体实验产品,领域常规使用流式细胞仪、细胞分化培养基类试剂/仪器。
3.3 高通量测序与分子筛选鉴定CCN3
实验目的是筛选Esr1Nkx2-1Cre小鼠ARH区域中调控骨代谢的特异性分泌因子。研究人员对高脂饮食(HFD)处理前后的Esr1Nkx2-1Cre小鼠ARH组织进行bulk RNA测序,筛选差异表达的分泌型基因;随后通过RNAscope原位杂交技术,验证候选基因在ARH神经元中的定位与表达变化。结果显示,测序分析发现Ccn3、Fst、Grp、Penk等基因在Esr1Nkx2-1Cre小鼠ARH中高表达,且HFD处理后表达显著下降;RNAscope验证显示,Ccn3与ARH^{Kiss1}神经元高度共定位,且仅在Esr1Nkx2-1Cre小鼠中表达,而Penk与Kiss1神经元无重叠,提示CCN3是调控骨量的核心候选因子。文献未提及具体实验产品,领域常规使用高通量测序平台、RNAscope原位杂交试剂盒类试剂/仪器。
3.4 CCN3成骨功能的体内外验证
实验目的是验证CCN3的成骨作用及特异性,并明确其体内生理功能。体外实验中,用重组小鼠(m)CCN3蛋白处理原代小鼠ocSSCs,结果显示骨矿化水平增加200%(n=3,P<0.001);用重组人(h)CCN3蛋白处理原代人ocSSCs,低剂量(0.025-0.25 nM)即可显著促进成骨分化,而Penk编码的肽段无此效应。体内实验中,对WT小鼠腹腔注射mCCN3(7.5 µg/kg,每日1次,共21天),结果显示%BV/TV显著升高(n=8,P<0.01);在5月龄去卵巢WT小鼠和20-23月龄老年WT小鼠中过表达CCN3,均可显著提高骨量,且仅促进骨形成参数(骨形成率/骨表面积、成骨细胞数量/骨表面积),对骨吸收参数(破骨细胞数量/骨表面积、陷窝密度/骨面积)无影响,提示CCN3可促进健康的骨重塑。文献未提及具体实验产品,领域常规使用重组蛋白、腺相关病毒(AAV)载体类试剂/仪器。
3.5 哺乳期CCN3的表达模式与功能验证
实验目的是明确CCN3在哺乳期的特异性表达模式及生理功能。研究人员检测了妊娠、哺乳期、产后不同阶段ARH中CCN3的表达,结果显示,CCN3在妊娠早晚期及未孕雌性中均不表达,在产后7天的哺乳期母鼠ARH^{ERα/Kiss1}神经元中高表达,且断奶后3-7天表达显著下降,提示CCN3为哺乳期特异性表达因子。随后通过腺病毒载体携带shRNA敲低哺乳期母鼠ARH中Ccn3,结果显示,即使在高钙饮食下,母鼠骨量仍丢失31%(n=6,P<0.01);低钙饮食下,后代体重显著低于对照组(n=12,P<0.001),且4/6的后代无法存活,提示CCN3对维持母体骨骼完整性和后代生存至关重要。
文献未提及具体实验产品,领域常规使用shRNA病毒载体、免疫荧光染色试剂盒类试剂/仪器。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为分泌型蛋白CCN3,属于功能性成骨激素标志物,其筛选与验证逻辑为:联体实验提示循环成骨因子存在→高通量测序筛选ARH中差异表达分泌基因→RNAscope验证神经元定位→体内外功能实验确认成骨作用→哺乳期特异性表达及生理功能验证,形成完整的“筛选-验证-功能”链条。
CCN3来源于哺乳期母鼠下丘脑ARH区域的ARH^{ERα/Kiss1}神经元,验证方法包括RNAscope原位杂交(检测神经元特异性定位)、重组蛋白处理原代ocSSCs(验证成骨功能)、体内shRNA敲低(验证生理功能)。特异性数据显示,CCN3仅在哺乳期母鼠中特异性表达,在妊娠及未孕状态下均不表达;敏感性方面,低剂量(0.025-0.25 nM)的重组CCN3即可显著促进人/小鼠ocSSCs的成骨分化。核心成果方面,CCN3作为成骨激素,可维持哺乳期母鼠的骨形成,避免过度骨丢失,敲低CCN3导致母鼠骨量丢失31%(n=6,P<0.01),低钙饮食下后代死亡率显著升高(4/6后代死亡);创新性在于首次发现脑源性CCN3作为哺乳期特异性成骨激素,构建了全新的脑-骨轴调控机制,为妊娠-哺乳期骨质疏松的防治提供了潜在靶点。此外,CCN3在雌雄个体中均具有成骨作用,且可促进老年小鼠和去卵巢小鼠的骨形成,提示其具有广泛的临床转化潜力。
