1. 领域背景与文献
文献英文标题:RUNX3 mediates keloid fibroblast proliferation through deacetylation of EZH2 by SIRT1;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:皮肤纤维化疾病分子机制与靶向治疗研究。
领域共识:瘢痕疙瘩是皮肤损伤后真皮层成纤维细胞过度增殖、细胞外基质过度沉积导致的良性纤维增生性疾病,具有侵袭性生长、超出原损伤边界、术后复发率高达50%~80%的临床特征,现有手术联合糖皮质激素注射、激光等治疗手段的长期应答率不足50%,缺乏特异性靶向治疗药物。领域发展关键节点包括2017年明确瘢痕疙瘩成纤维细胞具有类肿瘤增殖特性,2019年证实表观遗传调控是成纤维细胞异常增殖的核心发病机制,2021年以来组蛋白修饰、非编码RNA调控等方向成为研究热点。当前领域未解决的核心问题为瘢痕疙瘩成纤维细胞异常增殖的上游表观调控通路尚未完全阐明,缺乏可用于临床干预的特异性靶点。
本研究针对瘢痕疙瘩中SIRT1/EZH2/RUNX3调控轴的研究空白,探究该通路对成纤维细胞增殖及细胞周期的调控机制,明确三者的分子互作关系,为瘢痕疙瘩的靶向治疗提供新的理论依据与潜在干预靶点。
2. 文献综述解析
本文献综述部分按核心分子的功能维度进行分类评述,分别梳理RUNX家族的抑癌功能、EZH2的表观调控功能、SIRT1的去乙酰化调控功能三类研究的进展与局限。
现有研究的支持观点包括:RUNX家族成员RUNX3在多种肿瘤中发挥抑癌作用,可通过诱导细胞周期阻滞抑制细胞增殖,且已有研究证实RUNX3表达水平与瘢痕疙瘩光动力治疗敏感性呈正相关;EZH2作为多梳抑制复合物2的催化亚基,可通过组蛋白H3第27位赖氨酸三甲基化(H3K27me3)修饰沉默下游抑癌基因表达,其高表达与多种肿瘤的上皮间质转化进程密切相关;SIRT1作为烟酰胺腺嘌呤二核苷酸(NAD+)依赖的去乙酰化酶,可通过去乙酰化修饰调控多种转录因子的稳定性,参与细胞增殖、凋亡、自噬等生物学过程的调控。现有研究的技术方法优势为多采用临床样本验证、细胞功能实验结合分子互作分析的技术体系,可明确单分子在瘢痕疙瘩中的生物学功能。现有研究的局限性为多聚焦于单分子的功能验证,未明确SIRT1、EZH2、RUNX3三者的调控轴在瘢痕疙瘩中的作用,且EZH2的翻译后修饰在瘢痕疙瘩中的调控机制尚未见报道。
本研究的创新价值在于首次明确SIRT1介导的EZH2去乙酰化修饰可调控RUNX3表达,进而影响瘢痕疙瘩成纤维细胞增殖,填补了瘢痕疙瘩中该表观调控通路的研究空白,为瘢痕疙瘩的靶向干预提供了新的潜在靶点,学术必要性在于完善了瘢痕疙瘩成纤维细胞异常增殖的调控网络,为后续相关研究提供了新的方向。
3. 研究思路总结与详细解析
本研究的核心目标是明确SIRT1/EZH2/RUNX3轴对瘢痕疙瘩成纤维细胞异常增殖的调控机制,核心科学问题为SIRT1如何通过翻译后修饰调控EZH2稳定性,进而影响下游RUNX3表达及成纤维细胞细胞周期进程,技术路线遵循“临床样本表达相关性验证→RUNX3功能验证→SIRT1对EZH2的调控机制解析→SIRT1/EZH2轴功能回复验证”的闭环逻辑。
3.1 临床样本与细胞系的分子表达相关性分析
实验目的:明确SIRT1、EZH2、RUNX3在瘢痕疙瘩组织与正常皮肤组织中的表达差异及表达相关性,同时验证细胞系中三者的表达趋势与组织一致。方法细节:收集5例瘢痕疙瘩患者的手术切除瘢痕组织及配对的癌旁正常皮肤组织,采用苏木精-伊红染色(HE染色)观察组织病理形态变化;采用蛋白免疫印迹(Western blot)检测三个分子的蛋白表达水平;采用流式细胞术检测波形蛋白阳性的成纤维细胞中RUNX3的表达水平;采用Pearson相关性分析三个分子的表达相关性。同时提取人正常成纤维细胞(HF)和人瘢痕疙瘩成纤维细胞(HKF),验证细胞系中三个分子的表达差异及相关性。
结果解读:苏木精-伊红染色结果显示,瘢痕疙瘩组织真皮层增厚,浅层真皮可见成纤维细胞,胶原纤维束较浅层真皮明显增粗伴透明样变;中层真皮细胞浸润明显,深层真皮胶原纤维排列紊乱、细胞数量较少。
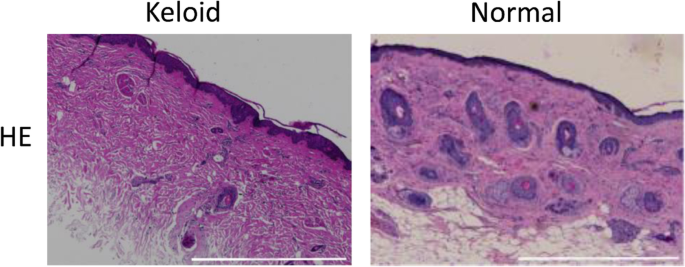
蛋白免疫印迹结果显示,瘢痕疙瘩组织中SIRT1表达较正常组织显著下调(n=5,P<0.05),RUNX3表达较正常组织显著下调(n=5,P<0.05),EZH2表达较正常组织显著上调(n=5,P<0.05);流式细胞术结果显示,正常皮肤成纤维细胞中RUNX3阳性比例显著高于瘢痕疙瘩组织(n=5,P<0.01)。相关性分析显示,SIRT1与EZH2表达呈负相关(P<0.05),EZH2与RUNX3表达呈负相关(P<0.05),SIRT1与RUNX3表达呈正相关(P<0.05)。

人瘢痕疙瘩成纤维细胞中三者的表达趋势及相关性与临床组织一致。
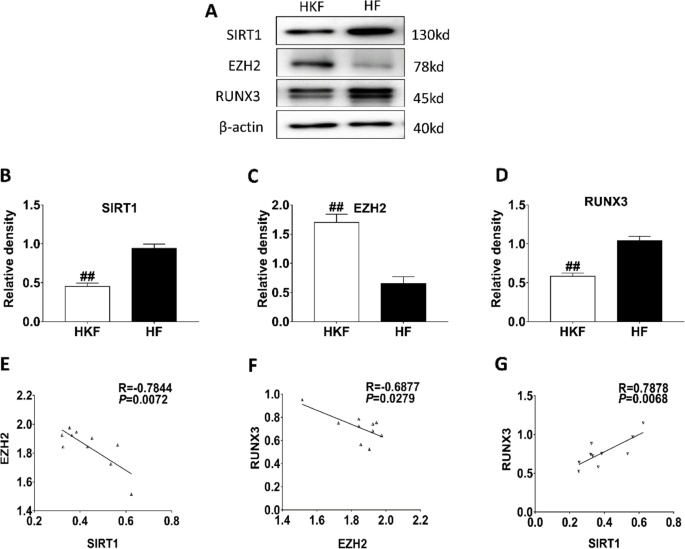
产品关联:实验所用关键产品:Abcam的RUNX3抗体、EZH2抗体、SIRT1抗体,贝克曼库尔特的流式细胞仪,湖南丰晖生物科技有限公司的人瘢痕疙瘩成纤维细胞。
3.2 RUNX3过表达对瘢痕疙瘩成纤维细胞增殖的功能验证
实验目的:验证RUNX3对瘢痕疙瘩成纤维细胞增殖、迁移及细胞周期的调控作用。方法细节:采用Lipofectamine 3000脂质体转染法在人瘢痕疙瘩成纤维细胞中转染RUNX3过表达质粒,转染24h后采用蛋白免疫印迹验证过表达效率;采用羧基荧光素二乙酸琥珀酰亚胺酯(CFSE)增殖实验检测转染后24h、48h的细胞增殖水平;采用细胞划痕实验检测细胞迁移能力;采用流式细胞术检测细胞周期分布;采用蛋白免疫印迹检测细胞周期相关蛋白CDK2、CDK4、细胞周期蛋白D1(CyclinD1)的表达水平。
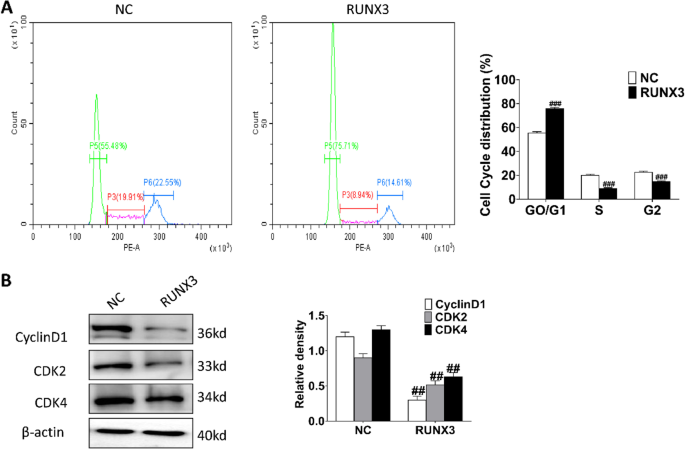
结果解读:RUNX3过表达质粒转染后,瘢痕疙瘩成纤维细胞中RUNX3表达水平较对照组显著升高(n=3,P<0.001),过表达效率符合实验要求。
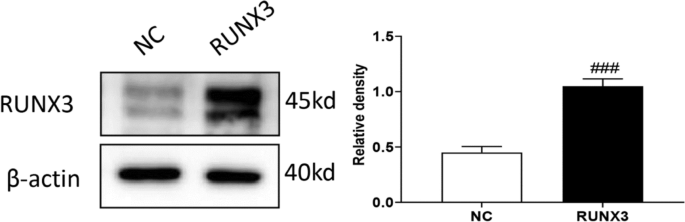
CFSE增殖实验结果显示,过表达RUNX3后瘢痕疙瘩成纤维细胞48h增殖率较对照组显著降低(n=3,P<0.01);细胞划痕实验结果显示,过表达RUNX3组细胞划痕愈合迁移距离较对照组明显缩短。
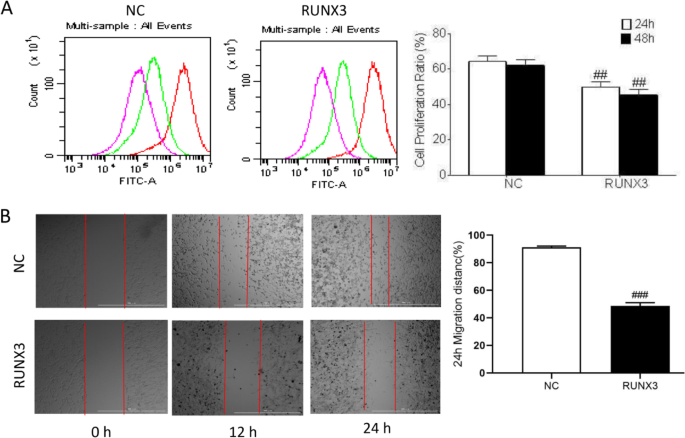
细胞周期检测结果显示,过表达RUNX3组G0/G1期细胞比例较对照组显著升高(n=3,P<0.001),S期、G2/M期细胞比例较对照组显著降低(n=3,P<0.001);蛋白免疫印迹结果显示,细胞周期相关蛋白CDK2、CDK4、细胞周期蛋白D1的表达水平较对照组显著下调(n=3,P<0.01)。
产品关联:实验所用关键产品:赛默飞世尔科技的Lipofectamine 3000转染试剂,碧云天生物技术的CFSE检测试剂盒,Abcam的CDK2、CDK4、细胞周期蛋白D1抗体。
3.3 SIRT1对EZH2乙酰化及稳定性的调控机制验证
实验目的:明确SIRT1对EZH2的翻译后修饰调控作用及对其蛋白稳定性的影响。方法细节:采用SIRT1特异性抑制剂EX527(10μM)处理人瘢痕疙瘩成纤维细胞24h,采用反转录聚合酶链式反应(RT-PCR)检测EZH2的mRNA表达水平;采用免疫共沉淀实验检测乙酰化EZH2的水平;采用蛋白合成抑制剂放线菌酮(CHX,0.1μg/mL)分别处理细胞0h、3h、6h、9h、12h,采用蛋白免疫印迹检测不同时间点EZH2的蛋白表达水平,计算蛋白半衰期,验证EX527处理后EZH2的蛋白稳定性变化。
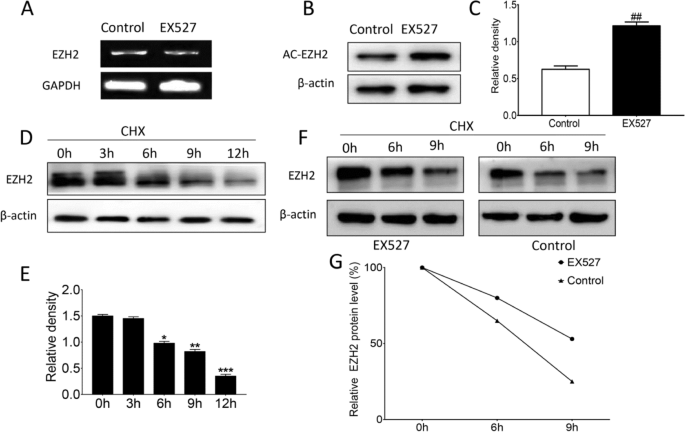
结果解读:EX527处理后,EZH2的mRNA表达水平较对照组无显著变化(n=3,P>0.05);免疫共沉淀结果显示,乙酰化EZH2水平较对照组显著升高(n=3,P<0.01);放线菌酮处理结果显示,EZH2蛋白半衰期约为6h,EX527处理后EZH2蛋白降解速率显著减慢,蛋白稳定性升高。
产品关联:实验所用关键产品:MedChemExpress的EX527抑制剂,Sigma-Aldrich的放线菌酮试剂,天根生化科技的RNA提取试剂盒、反转录PCR试剂盒,碧云天生物技术的免疫共沉淀试剂盒及蛋白A+G琼脂糖珠。
3.4 SIRT1/EZH2轴对成纤维细胞增殖的调控回复验证
实验目的:验证SIRT1/EZH2轴对RUNX3表达及成纤维细胞增殖的调控作用。方法细节:实验设置四组:对照组(正常培养的人瘢痕疙瘩成纤维细胞)、EX527处理组(10μM EX527处理24h)、EZH2敲低组(转染EZH2小干扰RNA24h)、EZH2敲低+EX527处理组(转染EZH2小干扰RNA24h后加入10μM EX527处理24h)。采用蛋白免疫印迹检测EZH2、RUNX3及细胞周期相关蛋白的表达水平;采用流式细胞术检测细胞周期分布;采用CFSE实验检测细胞增殖水平。
结果解读:蛋白免疫印迹结果显示,EX527处理组EZH2表达升高、RUNX3表达降低,细胞周期相关蛋白CDK2、CDK4、细胞周期蛋白D1表达较对照组显著升高(n=3,P<0.01);EZH2敲低组RUNX3表达较对照组显著升高,细胞周期相关蛋白表达较对照组显著降低(n=3,P<0.01);EZH2敲低+EX527处理组可逆转EZH2敲低的效应,RUNX3表达较EZH2敲低组显著降低,细胞周期相关蛋白表达较EZH2敲低组显著升高。

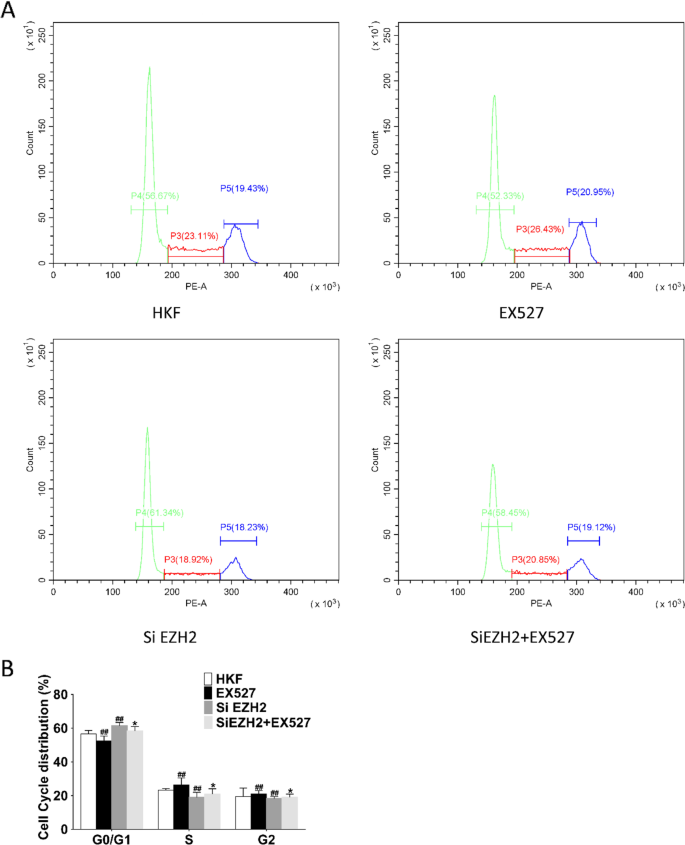
细胞周期检测结果显示,EX527处理组S期、G2/M期细胞比例较对照组显著升高(n=3,P<0.01);EZH2敲低组G0/G1期细胞比例较对照组显著升高(n=3,P<0.01);EZH2敲低+EX527处理组S期、G2/M期细胞比例较EZH2敲低组显著升高(n=3,P<0.05)。
CFSE增殖实验结果显示,EX527处理组48h细胞增殖率较对照组显著升高(n=3,P<0.01);EZH2敲低组48h细胞增殖率较对照组显著降低(n=3,P<0.01);EZH2敲低+EX527处理组48h细胞增殖率较EZH2敲低组显著回升(n=3,P<0.05)。

产品关联:实验所用关键产品:锐博生物的EZH2小干扰RNA,Abcam的乙酰化EZH2抗体。
4. Biomarker研究及发现成果
本研究涉及的Biomarker为Runt相关转录因子3(RUNX3),属于转录因子类瘢痕疙瘩增殖相关功能性Biomarker,其筛选验证逻辑遵循“临床组织差异表达筛选→细胞系功能验证→上游调控机制解析”的完整链条。
该Biomarker的样本来源为5例瘢痕疙瘩患者的手术切除瘢痕组织、配对的正常皮肤组织及体外培养的人瘢痕疙瘩成纤维细胞;验证方法包括蛋白免疫印迹检测蛋白表达水平、流式细胞术检测成纤维细胞中RUNX3的表达水平;文献未明确提供该Biomarker的诊断敏感性与特异性数据。
核心成果提炼:RUNX3在瘢痕疙瘩中发挥抑增殖功能,过表达RUNX3可使瘢痕疙瘩成纤维细胞G0/G1期阻滞比例显著升高(n=3,P<0.001),48h细胞增殖率显著降低(n=3,P<0.01);SIRT1通过去乙酰化EZH2降低其蛋白稳定性,进而上调RUNX3表达,抑制成纤维细胞增殖,SIRT1/EZH2/RUNX3轴为瘢痕疙瘩增殖调控的核心通路。统计学结果显示,EZH2与RUNX3表达呈负相关(P<0.05),SIRT1与RUNX3表达呈正相关(P<0.05)。创新性:首次在瘢痕疙瘩中明确SIRT1介导的EZH2乙酰化修饰调控RUNX3表达的分子机制,RUNX3可作为瘢痕疙瘩增殖评估及靶向干预的潜在Biomarker。
推测:SIRT1激动剂或EZH2抑制剂可通过上调RUNX3表达抑制瘢痕疙瘩成纤维细胞增殖,有望成为瘢痕疙瘩的潜在治疗药物,需进一步开展体内动物实验及临床前验证。本研究存在样本量较小的局限性,后续可扩大临床样本量验证分子表达相关性。